
【题目】下列说法正确的是
A. 石油的催化裂化可得到较多的轻质油
B. “西气东输”中输送的气体主要是乙烯
C. 煤间接液化的主要目的是获得各种芳香烃
D. 石油通过常压分馏可以得到石蜡等相对分子质量较大的烷烃
 名题训练系列答案
名题训练系列答案 期末集结号系列答案
期末集结号系列答案科目:高中化学 来源: 题型:
【题目】已知在热的碱性溶液中,NaClO发生如下反应:3NaClO![]() 2NaCl+NaClO3。在相同条件下NaClO2也能发生类似的反应,其最终产物是( )
2NaCl+NaClO3。在相同条件下NaClO2也能发生类似的反应,其最终产物是( )
A. NaCl、NaClO B. NaCl、NaClO3
C. NaClO、NaClO3 D. NaClO3、NaClO4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高氯酸铵(NH4ClO4)为白色晶体,具有不稳定性,在400 ℃时开始分解产生多种气体,常用于生产火箭推进剂。某化学兴趣小组同学利用下列装置对NH4ClO4的分解产物进行探究。(假设装置内药品均足量,部分夹持装置已省略。)
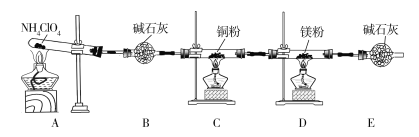
(1)在实验过程中发现C中铜粉由红色变为黑色,说明产物中有____________(填化学式)生成。
(2)实验完毕后,取D中硬质玻璃管中的固体物质于试管中,滴加蒸馏水,产生能使湿润的红色石蕊试纸变蓝色的气体,产生该气体的化学方程式为______________。
(3)通过上述实验现象的分析,某同学认为产物中还应有H2O,可能有Cl2。该同学认为可能有Cl2存在的理由是_________________________________。
(4)为了证明H2O和Cl2的存在,选择上述部分装置和下列提供的装置进行实验:
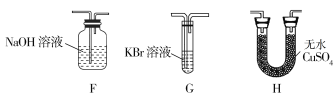
①按气流从左至右,装置的连接顺序为A→________→________→________。
②实验结束后发现G中液体变为橙黄色,用必要的文字和方程式解释出现该现象的原因:________________________。
③F中发生反应的离子方程式为___________________________。
(5)实验结论:NH4ClO4分解时产生了上述几种物质,则高氯酸铵分解的化学方程式为________________________________________________。
(6)在实验过程中仪器E中装有碱石灰的目的是________________;实验结束后,某同学拟通过称量D中镁粉质量的变化,计算高氯酸铵的分解率,会造成计算结果__________(填“偏大”“偏小”或“无法判断”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学欲配制80mL2.0mol/LNaOH溶液,其转移溶液的操作如图所示。
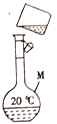
(1)图中操作上的错误是________。
(2)图中用到的仪器M是_______(填仪器名称和规格),下列关于仪器M的使用方法中,正确的是_______ (填字母)。
a.使用前应检查是否漏液 b.使用前必须烘干
c.不能用作物质反应或溶解的容器 d.可直接将热溶液转移到其中
(3)该同学称取NaOH固体的质量为________。
(4)下列操作会使配制的溶液浓度偏高的是______(填字母)。
a.所用过的烧杯未洗涤
b.转移过程中有少量溶液溅出
c.摇匀后,液面下降,再加入水至刻度线
d.定容时俯视刻度线
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】电子表所用的纽扣电池,两极材料为锌和氧化银,电解质溶液为KOH溶液,电池反应为 Ag2O + Zn + H2O═2Ag + Zn(OH)2,示意图如右。下列判断正确的是( )

A. 锌为负极,被还原
B. 纽扣电池工作时,OHˉ移向Ag2O
C. 每6.5 g 锌发生反应时,转移电子0.1 NA
D. 纽扣电池工作时,电解质溶液的碱性增强
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乌洛托品在合成、医药、染料等工业中有广泛用途,其结构式如图所示。将甲醛水溶液与氨水混合蒸发可制得乌洛托品。若原料完全反应生成乌洛托品,则甲醛与氨的物质的量之比为( )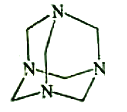
A. 1:1 B. 2:3 C. 3:2 D. 2:1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】【天津市和平区2017届第三次质量调查(三模)】A、B、C、D、E、F是分属三个短周期的主族元素,且原子序数依次增大。A、D同主族,B的氢化物水溶液呈碱性,C、E同主族,形成的化合物EC2是形成酸雨的主要物质之一。请化学用语回答下列问题:
(1)F在元素周期表中的位置为_______________。
(2)常温下,液态的B2A4与气态的BC2两者发生反应生成无毒物质,16g B2A4发生反应放热akJ,该反应的热化学方程式为_______________。
(3)D2E溶液在空气中长期放置发生反应,生成物之一为H。H与过氧化钠的结构和化学性质相似,其溶液显黄色。H的电子式为_______,写出在空气中长期放置生成H的化学反应方程式为:_________。H的溶液与稀硫酸反应产生的现象为_____________。
(4)化学家发现一种化学式为A4B4的离子化合物,一定条件下1mol A4B4熔融电离生成两种离子各1mol,则该物质熔融时的电离方程式为____________。
(5)向30mL某浓度由A、B、C、D中三种元素形成一元强碱溶液通入CO2气体后得溶液M,因CO2通入量的不同,溶液M的组成也不同。若向M中逐滴加入0.1mol/L盐酸,产生的气体V(CO2)与加入盐酸的体积V[HCl(aq)]的关系有下列图示两种情况(不计CO2的溶解)。
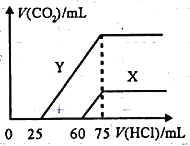
则曲线Y表明M中的溶质为________;原NaOH溶液的物质的量浓度为_______;由曲线X、Y可知,两次实验通入的CO2的体积比为_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有0.1 mol·L-1氨水10 mL,加蒸馏水稀释到1 L后,下列变化中正确的是( )
①电离程度增大 ②c(NH3·H2O)增大 ③NH![]() 数目增多 ④c(OH-)增大 ⑤导电性增强⑥
数目增多 ④c(OH-)增大 ⑤导电性增强⑥![]() 增大
增大
A. ①②③ B. ①③⑤ C. ①③⑥ D. ②④⑥
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com