
【题目】根据下列反应: (1) 2Fe3++2I-= 2Fe2++I2 (2) Br2 + 2Fe2+= 2Br-+2Fe3+,判断离子的还原性由强到弱的顺序是( )
A. Br- > I-> Fe2+ B. I- > Fe2+> Br- C. Fe2+> I-> Br- D. Br- > Fe2+> I-
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】在A、B、C三个烧杯中分别盛有相同浓度的稀硫酸,如图所示:
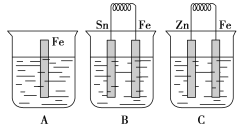
(1)A中反应的离子方程式为_____________________________。
(2)B中Sn极的电极反应式为____________________________,Sn极附近溶液的pH________(填“增大”、“减小”或“不变”)。C中被腐蚀的金属是________,总反应的离子方程式为________________,比较A、B、C中铁被腐蚀的速率,由快到慢的顺序是________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述正确的是( )
A. 反应AlCl3+4NaOH===NaAlO2+3NaCl+2H2O,可以设计成原电池
B. Zn和稀硫酸反应时,加入少量CuSO4溶液能加快产生H2的速率
C. 把Fe片和Cu片放入稀硫酸中,并用导线把二者相连,观察到Cu片上产生大量气泡,说明Cu与H2SO4能发生反应而Fe被钝化
D. Zn-Cu原电池工作过程中,溶液中H+向负极作定向移动
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2SO2(g) + O2(g)![]() 2SO3(g) ΔH = a kJ·mol-1,反应能量变化如图所示。下列说法中,不正确的是
2SO3(g) ΔH = a kJ·mol-1,反应能量变化如图所示。下列说法中,不正确的是

A.a<0
B.过程II可能使用了催化剂
C.使用催化剂可以提高SO2的平衡转化率
D.反应物断键吸收能量之和小于生成物成键释放能量之和
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用NA表示阿伏加德罗常数,下列叙述不正确的是( )
A. 常温常压下,7.8 gNa2O2含有的Na+数为0.2NA
B. 标准状况下,22.4 LCl2与水充分反应,转移的电子数为NA
C. 标准状况下,NA个CO2与SO2的混合气体分子占有的体积约为22.4 L
D. 50 ℃、1×105Pa下46g NO2与0 ℃、 2×105 Pa下46 g N2O4均含有3NA个原子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在2015年9月3日胜利日大阅兵中,八一飞行表演队首次使用高沸点的彩色拉烟剂,进行了绚丽的拉烟飞行.其原理是用氮气将拉烟剂带入飞机燃料燃烧后喷出的高温气体中,其中的水蒸气与气化后的彩色拉烟剂遇冷凝结形成“彩雾”.下列说法不正确的是( )

A.“彩雾”是一种混合物
B.上述过程中有物理变化
C.燃料燃烧产生的热量促使拉烟剂气化
D.“彩雾”的形成与焰色反应的原理相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】 下列有关电解质的说法中,不正确的是( )
A. 25℃时,任何水溶液中的Kw=1.0×10-14
B. 在0.1 mol·L-1的醋酸溶液中加入少量冰醋酸,电离平衡正向移动,醋酸的电离程度增大
C. 将pH=2的盐酸稀释10倍,所得溶液的pH=3
D. 25℃时,pH=12的氨水中,OH-的物质的量浓度为0.010 mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】水是一种重要的自然资源,是人类赖以生存不可或缺的物质,水质优劣直接影响人体健康。海水是人类资源宝库,若把海水淡化和化工生产结合起来,既可解决淡水资源缺乏的问题,又可充分利用海洋资源。
(1)天然水净化处理过程中需要加入混凝剂,常用的混凝剂有明矾、硫酸铝、硫酸铁等,写出明矾净水作用的原理是(用离子方程式及相关语言描述)___________________。
(2)目前,国际上使用的“海水淡化”主要技术之一是电渗析法,如图是利用电渗析法对海水进行淡化处理的原理图。已知海水中含Na+、Cl-、Ca2+、Mg2+、SO等离子,电极为惰性电极。
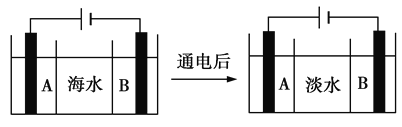
①阳离子交换膜(只允许阳离子通过)是________(填“A”或“B”);
②写出通电后阳极区的电极反应式:__________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com