
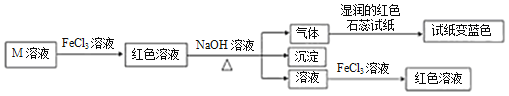
【题目】短周期主族元素W、X、Y、Z的原子序数依次增大,它们的原子最外层电子数总和等于Z的原子序数,由这四种元素组成一种化合物M具有如下性质下列推断正确的是( )
A.原子半径:Z>Y>X>W
B.最高价氧化物对应的水化物酸性:Y>X
C.简单阴离子的还原性: Z>W
D.W、Y、Z组成的化合物只含共价键
【答案】B
【解析】
M溶液中滴入氯化铁溶液变红,说明溶液中含有硫氰根离子,加入NaOH溶液后加热,生成的气体能够使湿润的红色石蕊试纸变蓝,说明原溶液中含有铵根离子,则M为NH4SCN,W、X、Y、Z的原子序数依次增大,则W为H元素,X为C元素,Y为N元素,Z为S元素,四种原子最外层电子数总和等于S的原子序数16,符合题意,据此分析解答。
由上述分析可知,W、X、Y、Z四种元素分别为H、C、N、S;M为NH4SCN。
A.同一周期,从左向右,原子半径逐渐减小,则原子半径X>Y,一般而言,电子层数越多,原子半径越大,原子半径大小为:Z>X>Y>W,故A错误;
B.非金属性:C<N,则最高价氧化物对应水化物的酸性:Y>X,故B正确;
C.非金属性越强,对应阴离子的还原性越弱,则简单阴离子的还原性:W>Z,故C错误;
D.W、Y、Z组成的化合物可能为NH4HS,其中含离子键、共价键,故D错误;
故选B。


科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值,下列说法正确的是( )
A.100ml18mol/L浓硫酸与足量铜加热充分反应转移电子数为3.6NA
B.0.1mol24Mg32S晶体中所含中子总数为2.8NA
C.标准状况下,22.4LCO2中含有的共用电子对数目为2NA
D.24.5gKClO3晶体中含有C1-的数目为0.2NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】芬太尼类似物L具有镇痛作用。它的合成方法如下:

已知:
I、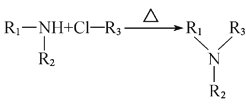 +HCl
+HCl
II、![]()
![]()
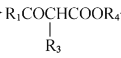 +R2OH;
+R2OH;
III、 (
(![]() 为氢或烃基)
为氢或烃基)
回答下列问题:
(1)A是一种烯烃,化学名称为______,其分子中最多有__________个原子共面。
(2) B中官能团的名称为_____、_____。②的反应类型为________
(3)③的化学方程式为________
(4)碳原子上连有4个不同的原子或基团时,该碳称为手性碳。指出F的结构简式中手性碳原子并用星号(*)标出F中的手性碳________。G的结构简式为________。
(5)已知④有一定的反应限度,反应进行时加入吡啶(一种有机碱),其作用是________。
(6)参照上述合成路线,写出以环已烯(![]() )和乙醇为起始原料经三步制备化合物
)和乙醇为起始原料经三步制备化合物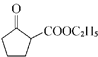 的合成路线________。
的合成路线________。
(已知:![]() 其他试剂任选)
其他试剂任选)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图电化学原理可用于治理水中硝酸盐的污染,下列说法不正确的是
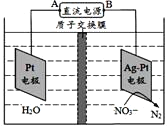
A. A为电源正极
B. 在Pt电极上发生氧化反应
C. 阴极电极反应式为2NO3-+6H2O+10e-=N2+12OH
D. 质子从Pt电极移向Ag-Pt电极
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某实验小组依据甲烷燃烧的反应原理,设计如图a所示的电池装置:
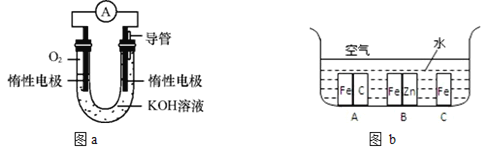
(1)该电池的能量转化形式为____________。
(2)该电池正极的电极反应为____________。
(3)工作一段时间后,测得溶液的pH______,该电池总反应的化学方程式为_________。
(4)在生产生活中,金属腐蚀所带来的损失非常严重,所以防止金属腐蚀已经成为科学研究和技术领域的重大问题。兴趣小组的同学在实验室对金属腐蚀进行了探究。如图b所示,铁处于A、B、C三种不同的环境中,铁被腐蚀的速率由大到小的顺序是(填序号)_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】火箭推进器中盛有强还原剂液态肼(N2H4)和强氧化剂液态双氧水。当把0.4mol液态肼和0.8mol H2O2混合反应,生成氮气和水蒸气,放出260 kJ的热量(相当于25℃、101kPa下测得的热量)。
(1)反应的热化学方程式为___________。
(2)又已知H2O(l) = H2O(g) ΔH= +44kJ/mol。则16g液态肼与液态双氧水反应生成液态水时放出的热量是_____kJ。
(3)此反应用于火箭推进,其优点是(至少答两点)________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】我国科研人员提出了由CO2和CH4转化为高附加值产品CH3COOH的催化反应历程。该历程示意图如下。

下列说法不正确的是
A. 生成CH3COOH总反应的原子利用率为100%
B. CH4→CH3COOH过程中,有C―H键发生断裂
C. ①→②放出能量并形成了C―C键
D. 该催化剂可有效提高反应物的平衡转化率
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Y是合成香料、医药、农药及染料的重要中间体,可由X在酸性条件下反应得到:

下列说法正确的是( )
A. X分子中所有碳原子可能共平面
B. X、Y分别与足量H2加成后的分子中均含有手性碳原子
C. Y可以发生显色、氧化和还原反应,还可以与甲醛发生缩聚反应
D. 等物质的量的X、Y分别与NaOH溶液反应,最多消耗NaOH的物质的量之比为4∶3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高铁酸钾(K2FeO4)是一新型高效无毒的多功能水处理剂。资料:K2FeO4为紫色固体,微溶于KOH溶液,具有强氧化性,在酸性或中性溶液中快速产生O2,在碱性溶液中较稳定。
(1)制备K2FeO4
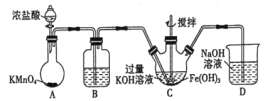
①写出A中发生反应的化学方程式______。
②除杂装置B中的试剂为____。
③C为制备K2FeO4装置,KOH溶液过量的原因是____。
④D为尾气处理装置,发生反应的离子方程式为____。
(2)探究K2FeO4的性质取C中紫色溶液,加入稀硫酸,产生黄绿色气体,得溶液a,经检验气体中含有Cl2。为证明K2FeO4能否氧化Cl而产生Cl2设计以下方案:
方案Ⅰ | 取少量溶液a,滴加KSCN溶液至过量,溶液呈红色 |
方案Ⅱ | 用KOH溶液充分洗涤C中所得固体,再用KOH溶液将K2FeO4溶出,得到紫色溶液b。取少量b,滴加盐酸,有Cl2产生 |
①由方案Ⅰ中溶液变红可知a中含有____。该离子的产生__(填“能”或“不能”)判断一定是由K2FeO4被Cl还原而形成的。
②方案Ⅱ用KOH溶液洗涤的目的是____,方案Ⅱ得出氧化性:Cl2 ___FeO42(填“![]() ”或“
”或“![]() ”)。
”)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com