
【题目】![]() 实验室欲用NaOH固体配制
实验室欲用NaOH固体配制![]() 的NaOH溶液
的NaOH溶液![]() 。
。
①本实验必须用到的仪器有天平、药匙、玻璃棒、烧杯、250mL容量瓶、还有_________;
②要完成本实验该同学应称出____________![]() ;
;
③若直接在天平的两个托盘上放两张质量相等的纸片进行称量,则会使得配制结果_______。![]() 偏低、偏高或无影响
偏低、偏高或无影响![]()
![]() 铁不能与冷、热水反应,但能与水蒸气反应。老师用如图所示实验装置,完成还原铁粉与水蒸气反应的演示实验。
铁不能与冷、热水反应,但能与水蒸气反应。老师用如图所示实验装置,完成还原铁粉与水蒸气反应的演示实验。

①反应一段时间后,有肥皂泡吹起时,用点燃的火柴靠近肥皂泡,当_________时![]() 填实验现象
填实验现象![]() ,说明“铁与水蒸气”能够进行反应;
,说明“铁与水蒸气”能够进行反应;
②写出该反应的化学方程式,并用单线桥表示出电子转移情况___________;
③为了研究一定时间内铁粉的消耗量,他们设计了如下实验:准确称量一定质量的铁粉进行反应,收集并测量反应后生成的气体体积![]() 已折算成标准状况
已折算成标准状况![]() 。收集并测量气体体积应选下图中的________装置;
。收集并测量气体体积应选下图中的________装置;

若称取![]() 铁粉,然后与水蒸气加热至无气体放出,最好选用__________规格的量筒
铁粉,然后与水蒸气加热至无气体放出,最好选用__________规格的量筒![]() 选填字母序号
选填字母序号![]() 。
。
A.100mL B.200mL C.500mL D.1000mL
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】已知25℃时,醋酸、氢硫酸、氢氰酸的电离平衡常数如下表:(单位省略)
醋酸 | 氢硫酸 | 氢氰酸 |
Ka=1.8×10-5 | Ka1=9.1×10-8 Ka2=1.1×10-12 | Ka=4.9×10-10 |
(1)体积相同、c(H+)相同的三种酸溶液a.CH3COOH;b.HCN;c.H2SO4分别与同浓度的NaOH溶液完全中和,消耗NaOH溶液的体积由大到小的排列顺序是(填字母)___________。
(2)25℃时,等浓度的三种溶液①NaCN 溶液、②Na2S溶液、③CH3COONa溶液,pH由大到小的顺序为_____________(填序号)。
(3)25℃时,浓度均为0.01mol/L的①NaCN、②CH3COONa、③NaCl 溶液中,阴离子总浓度由大到小的顺序为 _____________(填序号)。
(4)将浓度为0.02mol/L的HCN 与0.01mol/L NaOH 溶液等体积混合,测得混合溶液中c(Na+)>c(CN-),下列关系正确的是_______。
a.c(H+)<c(OH-) b.c(H+)+c(HCN)=c(OH-)+c(CN-) c.c(HCN)+c(CN-)=0.01mol/L
(5)25℃时,向NaCN溶液中通入少量H2S,反应的离子方程式为___________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化合物J是一种常用的抗组胺药物,一种合成路线如下:
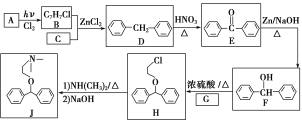
已知:①C为最简单的芳香烃,且A、C互为同系物。
②2ROH+NH3![]() HNR2+2H2O(R代表烃基)。
HNR2+2H2O(R代表烃基)。
请回答下列问题:
(1)A的化学名称是___________,H中的官能团名称是_________________。
(2)由D生成E的反应类型是________,G的结构简式为_______________。
(3)B+C―→D的化学方程式为_____________________________________。
(4)L是F的同分异构体,含有联苯(![]() )结构,遇FeCl3溶液显紫色,则L有_______种(不考虑立体异构)。其中核磁共振氢谱为六组峰,峰面积之比为3∶2∶2∶2∶2∶1的结构简式为___________________。
)结构,遇FeCl3溶液显紫色,则L有_______种(不考虑立体异构)。其中核磁共振氢谱为六组峰,峰面积之比为3∶2∶2∶2∶2∶1的结构简式为___________________。
(5)写出用氯乙烷和2氯1丙醇为原料制备化合物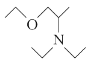 的合成路线(其他无机试剂任选)。________________
的合成路线(其他无机试剂任选)。________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验误差分析错误的是( )
A.用湿润的pH试纸测稀碱溶液的pH,测定值偏小
B.用容量瓶配制溶液,定容时俯视刻度线,所配溶液浓度偏小
C.容量瓶中含有少量蒸馏水对所配的溶液无影响
D.测定中和反应的中和热时,保温效果越好,测定误差越小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知草酸镍晶体(NiC2O4·2H2O)难溶于水,工业上从废镍催化剂(主要成分为Ni,含有一定量的Al2O3、FeO、SiO2、CaO等)制备草酸镍晶体的流程如图所示:

已知:①相关金属离子生成氢氧化物沉淀的pH见表中数据:
金属离子 | Fe3+ | Fe2+ | Al3+ | Ni2+ |
开始沉淀的pH | 1.1 | 5.8 | 3.0 | 6.8 |
完全沉淀的pH | 3.2 | 8.8 | 5.0 | 9.5 |
②Ksp(CaF2)=1.46×10-10;
③当某物质浓度小于1.0×10-5 mol·L-1时,视为完全沉淀。
请回答下列问题:
(1)请写出一种能提高“酸浸”速率的措施:_______________________________。
(2)试剂a是一种绿色氧化剂,写出“氧化”时反应的离子方程式:_____________。
(3)“调pH”时pH的调控范围为__________________。
(4)写出“沉镍”时发生反应的离子方程式:________________________________,证明Ni2+已经沉淀完全的实验步骤及现象是______________________________,当Ca2+沉淀完全时,溶液中c(F-)>____________mol·L-1(写出计算式即可)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关说法正确的是( )
A.在稀AgNO3溶液中加入过量 NaCl溶液,产生白色沉淀,再加入少量 Na2S溶液,出现黑色沉淀,则加入Na2S溶液后 c(Ag+) 更小了
B.吸热反应TiO2(s)+2Cl2(g) =TiCl4(g)+O2(g)一定条件下可自发进行,则该反应ΔS<0
C.实验室制氢气,为了加快反应速率,可向稀 H2SO4中滴加少量 Cu(NO3)2溶液
D.N2(g)+3H2(g)![]() 2NH3(g) ΔH<0,仅升高温度,达平衡时氢气转化率增大
2NH3(g) ΔH<0,仅升高温度,达平衡时氢气转化率增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在下列物质转化中,已知A是一种正盐,D的相对分子质量比C的相对分子质量大16,E是酸;当X无论是强酸还是强碱时,都有如下的转化关系:

说明:当X是强酸时A、B、C、D、E均含同一种元素;当X是强碱时,A、B、C、D、E均含另外同一种元素。(已知H2CO3、H2S、H2SO3、H2SiO3皆为二元弱酸)
请回答下列问题:
(1)A是___________,Y是___________,Z是____________(填化学式,下同)。
(2)当X是强酸时,E是_______________,写出B生成C的化学方程式:__________________。
(3)当X是强碱时,E是_______________,写出D生成E的离子方程式:________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将银边天竺葵(叶片边缘无叶绿体)的叶片在黑暗中放置48小时后,用锡箱纸遮蔽叶片两面,如下图所示。而后在日光下照光一段时间,去除锡箱纸,用碘液染色法处理叶片。不出现蓝色的部位是( )

A.a、b和dB.a、c和eC.c、d和eD.b、c和e
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:①2H2(g)+O2(g)===2H2O(l) ΔH=-570.0 kJ·mol-1;②CO(g)+![]() O2(g)===CO2(g) ΔH=-280 kJ·mol-1。某H2和CO的混合气体完全燃烧放出141 kJ热量,同时消耗标准状况下5.6 L O2,则原混合气体中H2和CO的物质的量之比为( )
O2(g)===CO2(g) ΔH=-280 kJ·mol-1。某H2和CO的混合气体完全燃烧放出141 kJ热量,同时消耗标准状况下5.6 L O2,则原混合气体中H2和CO的物质的量之比为( )
A.2∶1B.1∶2C.1∶1D.2∶3
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com