
(12分)进行中和热的测定的装置如图所示。回答下列问题:
(1)从实验装置中尚缺少的一种玻璃用品是 。
(2)烧杯间填满碎纸条的作用是 。
(3)利用该装置测得的中和热数值 (填“偏大、偏小、无影响”)
(4)某研究小组将装置完善后,把V1 mL 1.0 mol/LHCl溶液和V2 mL未知浓度的NaOH溶液混合均匀后测量并记录溶液温度,实验结果如下图所示
(实验中始终保持V1+V2=50 mL)。回答下列问题:
①研究小组做该实验时环境温度 (填“高于”、“低于”或“等于”)22 ℃。
②由题干及图形可知,V1/V2= : 时,酸碱恰好完全中和,此反应所用NaOH溶液的浓度应为 mol/L。
科目:高中化学 来源:江苏省前黄高级中学2007届高三年级第一学期期中考试、化学试卷 题型:022
(1)下列有关实验操作或判断不正确的是________(填有关序号,选错倒扣分).
A、用10mL量筒量取稀硫酸溶液8.0mL
B、用干燥的pH试纸测定氯水的pH
C、用碱式滴定管量取KMnO4溶液19.60mL
D、使用容量瓶配制溶液时,俯视液面定容后所得溶液的浓度偏大
E、圆底烧瓶、锥形瓶、蒸发皿加热时都应垫在石棉网上
F、测定硫酸铜晶体中结晶水含量时,将加热后的坩埚置于干燥器中冷却后再称量
G.用冰醋酸,蒸馏水和容量瓶等仪器配制pH为1的醋酸稀溶液
(2)实验室利用如右图装置进行中和热的测定.

回答下列问题:
①该图中有两处未画出,它们是________、________;
②如果用0.5mol/L的盐酸和氢氧化钠固体进行实验,则实验中所测出的“中和热”将(填“偏大”、“偏小”或“不变”);原因是________.
(3)在分析化学中常用Na2C2O4晶体作为基准物质测定KMnO4溶液的浓度.在H2SO4溶液中,反应如下:
2MnO4-+5C2O42-+16H+![]() 2Mn2++10CO2↑+8H2O
2Mn2++10CO2↑+8H2O
①用托盘天平称取WgNa2C2O4晶体.
②将WgNa2C2O4配成100mL标准溶液,移取20.00mL置于锥形瓶中,则酸性KMnO4溶液应装在________(填“酸式”或“碱式”)滴定管中.
③若滴定管的起始读数和终点读数如图所示,则酸性KMnO4的物质的量浓度为________(填表达式).
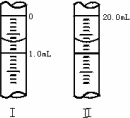
④若滴定完毕立即读数,测定的KMnO4溶液的浓度________(填“偏高”“偏低”或“不变”).
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
(10分)(1)在定量实验中,采用下列操作会导致实验结果偏低的是 (填序号)。
A.中和热测定实验中以环形铁丝搅拌棒代替环形玻璃搅拌棒
B.配制100mL 2 mol/L的NaCl溶液,以胶头滴管加水定容时,液面稍超出容量瓶刻度线,反复摇匀后,凹液面最低点恰好与刻度线相切
C.测定硫酸铜晶体结晶水含量,加热并搅拌时,有少量固体溅出。
D.称取一定质量无水碳酸钠粉末,用稀盐酸滴定(用甲基橙作指示剂),测定盐酸浓度。酸式滴定管用蒸馏水润洗后未用待装液润洗,立即装液、滴定。
(2)下列实验操作或实验所得出的结论一定正确的是 (填序号)
A.配制100mL 1.00mol/L的NaCl溶液时,可用托盘天平准确称取5.85g NaCl
固体
B.某无色溶液中加入盐酸产生无色无味气体且能使澄清石灰水变混浊的气体,则
该溶液中一定含有大量的HCO3-
C.制备Fe(OH)3胶体时,应往沸水中加饱和的FeCl3溶液,并继续加热到溶液呈
红褐色为止
D.除去蛋白质中混有的少量NaCl,加AgNO3溶液后过滤
E.在中学“硫酸铜晶体里的结晶水含量的测定”实验中,至少需要进行四次称量操
作
F.测定中和热实验中,每次实验均应测量三个温度,即盐酸起始温度,NaOH溶液
的起始温度和反应后溶液的最高温度
(3)根据右图描述回答下列问题:
①关闭图A装置中的止水夹a后,从长颈漏斗向试管中注入一定量的水,静置后如图所示。试判断:A装置是否漏气?(填“漏气”、“不漏气”或“不能确定”)
②关闭图B装置中的止水夹a后,开启活塞b,水不断往下滴,直至全部流入烧瓶。试判断:B装置是否漏气?
(填“漏气”、“不漏气”或“不能确定”) ,判断理由是 。
查看答案和解析>>
科目:高中化学 来源:2010—2011学年浙江省杭州学军中学高二下学期期中考试化学试卷 题型:实验题
(18分)Ⅰ测定水中溶解氧的方法是:在水中加入硫酸锰及氢氧化钠和碘化钾溶液,生成氢氧化锰沉淀。氢氧化锰性质极不稳定,迅速与水中溶解氧化合生成锰酸锰:
2MnSO4+4NaOH=2Mn(OH)2↓+2Na2SO4--------------①
2Mn(OH)2+O2=2H2MnO3---------------------------②
H2MnO3十Mn(OH)2=MnMnO3↓+2H2O------③
加入硫酸溶液,使沉淀(MnMnO3)与溶液中所加入的碘化钾发生反应,
2KI+H2SO4=2HI+K2SO4--------------------------- --------④
MnMnO3+2H2SO4+2HI=2MnSO4+I2+3H2O ----—⑤
用已知浓度的Na2S2O3溶液滴定生成的碘,根据消耗的Na2S2O3的体积可以测定水中溶氧量(mg/L)
I2+2Na2S2O3=2NaI+Na2S4O6
测定中,用移液管取50.00 mL水样,迅速加入预先配置好的MnSO4和NaOH混合溶液,再加入KI溶液,立即塞好塞子,震荡使反应完全。打开塞子,迅速加入适量的稀硫酸,期间发生①—⑤反应生成单质碘。用0.10mol/LNa2S2O3溶液滴定生成的碘,消耗了2.68mL Na2S2O3溶液。
已知:H2S2O3 为弱酸
回答下列问题:
(1)盛放Na2S2O3溶液的滴定管种类为
(2)该滴定的指示剂为 ,滴定时,溶液由 色到 色,且半分钟内颜色不再变化即达到滴定终点
(3)下列操作和该滴定有关并会导致测定水中溶氧偏高的是( )
A滴定前滴定管尖嘴无气泡,滴定结束尖嘴有气泡 B锥形瓶用待装液润洗
C滴定管读数开始平视,滴定结束时立即平视读数 D酸式滴定管没有用待装液润洗
(4)水中溶氧量为 mg/L水。
Ⅱ50.00mL0.50mol/L盐酸跟50.0mL0.55mol/L氢氧化钠溶液在下图装置中进行中和反应,通过测定反应前盐酸和氢氧化钠溶液各自的温度和中和过程中混合液的最高温度可计算中和热.试回答下列问题.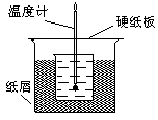
(1)该实验装置设计中缺少的仪器的名称为
(2)若实验测得放出热量为1.43kJ,写出表示中和热的热化学方程式
(3)改用60.0mL0.5mol/L盐酸跟50.0mL0.55mol/L氢氧化钠溶液进行反应,与上述实验相比,所放热量 等,所求中和热数值 等。(填“相等,不相等”)
查看答案和解析>>
科目:高中化学 来源:河北省正定中学2010—2011学年度高三年级第二次月考化学 题型:填空题
(10分)(1)在定量实验中,采用下列操作会导致实验结果偏低的是 (填序号)。
A.中和热测定实验中以环形铁丝搅拌棒代替环形玻璃搅拌棒
B.配制100mL 2 mol/L的NaCl溶液,以胶头滴管加水定容时,液面稍超出容量瓶刻度线,反复摇匀后,凹液面最低点恰好与刻度线相切
mol/L的NaCl溶液,以胶头滴管加水定容时,液面稍超出容量瓶刻度线,反复摇匀后,凹液面最低点恰好与刻度线相切
C.测定硫酸铜晶体结晶水含量,加热并搅拌时,有少量固体溅出。
D.称取一定质量无水碳酸钠粉末,用稀盐酸滴定(用甲基橙作指示剂),测定盐酸浓度。酸式滴定管用蒸馏水润洗后未用待装液润洗,立即装液、滴定。
(2)下列实验操作或实验所得出的结论一定正确的是 (填序号)[来源:学科网ZXXK]
A.配制100mL 1.00mol/L的NaCl 溶液时,可用托盘天平准确称取5.85g NaCl
固体
B.某无色溶液中加入盐酸产生无色无味气体且能使澄清石灰水变混浊的气体,则
该溶液中一定含有大量的HCO3-
C.制备Fe(OH)3胶体时,应往沸水中加饱和的FeCl3溶液,并继续加热到溶液呈
红褐色为止
D.除去蛋白质中混有的少量NaCl,加AgNO3溶液后过滤
E.在中学“硫酸铜晶体里的结晶水含量的测定”实验中,至少需要进行四次称量操
作
F.测定中和热实验中,每次实验均应测量三个温度,即盐酸起始温度,NaOH溶液
的起始温度和反应后溶液的最高温度
(3)根据右图描述回答下列问题:
①关闭图A装置中的止水夹a后,从长颈漏斗向试管中注入一定量的水,静置后如图所示。试判断:A装置是否漏气?(填“漏气”、“不漏气”或“不能确定”)
②关闭图B装置中的止水夹a后,开启活塞b,水不断往下滴,直至全部流入烧瓶。试判断:B装置是否漏气?
(填“漏气”、“不漏气”或“不能确定”) ,判断理由是 。
查看答案和解析>>
科目:高中化学 来源:河北省2011届度高三年级第二次月考化学 题型:填空题
(10分)(1)在定量实验中,采用下列操作会导致实验结果偏低的是 (填序号)。
A.中和热测定实验中以环形铁丝搅拌棒代替环形玻璃搅拌棒
B.配制100mL 2 mol/L的NaCl溶液,以胶头滴管加水定容时,液面稍超出容量瓶刻度线,反复摇匀后,凹液面最低点恰好与刻度线相切
C.测定硫酸铜晶体结晶水含量,加热并搅拌时,有少量固体溅出。
D.称取一定质量无水碳酸钠粉末,用稀盐酸滴定(用甲基橙作指示剂),测定盐酸浓度。酸式滴定管用蒸馏水润洗后未用待装液润洗,立即装液、滴定。
(2)下列实验操作或实验所得出的结论一定正确的是 (填序号)[来源:ZXXK]
A.配制100mL 1.00mol/L的NaCl 溶液时,可用托盘天平准确称取5.85g NaCl
固体
B.某无色溶液中加入盐酸产生无色无味气体且能使澄清石灰水变混浊的气体,则
该溶液中一定含有大量的HCO3-
C.制备Fe(OH)3胶体时,应往沸水中加饱和的FeCl3 溶液,并继续加热到溶液呈
红褐色为止
D.除去蛋白质中混有的少量NaCl,加AgNO3溶液后过滤
E.在中学“硫酸铜晶体里的结晶水含量的测定”实验中,至少需要进行四次称量操
作
F.测定中和热实验中,每次实验均应测量三个温度,即盐酸起始温度,NaOH溶液
的起始温度和反应后溶液的最高温度
(3)根据右图描述回答下列问题:

①关闭图A装置中的止水夹a后,从长颈漏斗向试管中注入一定量的水,静置后如图所示。试判断:A装置是否漏气?(填“漏气”、“不漏气”或“不能确定”)
②关闭图B装置中的止水夹a后,开启活塞b,水不断往下滴,直至全部流入烧瓶。试判断:B装置是否漏气?
(填“漏气”、“不漏气”或“不能确定”) ,判断理由是 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com