
【题目】NH4NO3 溶液受热可发生分解反应:NH4NO3![]() N2↑+HNO3+H2O(未配平)。用 NA 表示阿伏加德罗数的值,下列说法正确的是
N2↑+HNO3+H2O(未配平)。用 NA 表示阿伏加德罗数的值,下列说法正确的是
A.分解时每生成 2.24 L(标准状况)N2,转移电子的数目为 0.6NA
B.2.8 g N2 中含有共用电子对的数目为 0.3NA
C.56 g Fe 与足量稀硝酸反应生成 NO2 分子的数目为 3NA
D.0.1 mol·L-1 NH4NO3 溶液中,NH4+的数目小于 0.1NA
【答案】B
【解析】
A.5NH4NO3![]() 4N2↑+2HNO3+9H2O转移的电子为20个,标准状况下,2.24 LN2为0.1mol,则转移电子为0.1mol×
4N2↑+2HNO3+9H2O转移的电子为20个,标准状况下,2.24 LN2为0.1mol,则转移电子为0.1mol×![]() =0.5mol,故A错误;
=0.5mol,故A错误;
B.2.8 gN2的物质的量为![]() =0.1mol,含有共用电子对的数目为0.1 ×3×NA=0.3 NA,故B正确;
=0.1mol,含有共用电子对的数目为0.1 ×3×NA=0.3 NA,故B正确;
C.5.6 g Fe物质的量为0.1mol,与足量稀硝酸反应生成硝酸铁和NO,转移的电子数为0.3NA,则生成0.1mol NO,不能生成NO2,故C错误;
D.NH4NO3溶液的体积未知,NH4+发生水解,不能计算 0.1 mol/L NH4NO3溶液中的铵根离子数目,故D错误;
故选B。


 53随堂测系列答案
53随堂测系列答案科目:高中化学 来源: 题型:
【题目】已知一个碳原子连两个—OH的结构不稳定,会很快脱去一分子水,其变化如下:
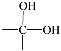 →
→ ![]() + H2O
+ H2O
下图中B和![]() 、
、![]() 等都是A和Cl2发生反应生成的产物,E是一种高分子化合物,透光性能好,常用作一些灯饰外壳。过程中一些小分子都已经略去。
等都是A和Cl2发生反应生成的产物,E是一种高分子化合物,透光性能好,常用作一些灯饰外壳。过程中一些小分子都已经略去。
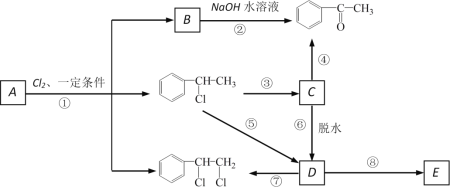
(1)A的化学名称为_____________
(2)第⑦步的化学方程式为___________________________,该反应类型为_____;
(3)E的结构简式为______;
(4)符合下列条件:苯环上有两个取代基且苯环上只有两种不同化学环境的氢的C的同分异构体的结构简式分别是_______________、_____________、________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】把13g Zn放入足量的盐酸中,Zn完全反应。计算:
(1)13g Zn的物质的量___________
(2)参加反应的HCl的物质的量___________
(3)生成H2的体积(标准状况)___________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列选项中离子能大量共存的是( )
(1)与铝粉反应放出H2的无色溶液:NO3-、Al3+、Na+、SO42-
(2)含有大量NO3-的溶液:H+、Fe2+、Cl-、SO42-
(3)中性溶液:Fe3+、Al3+、NO3-、SO42-
(4)使pH试纸显蓝色的溶液:Cu2+、NO3-、Fe3+、SO42-
(5)含有大量Fe3+的溶液:Na+、SCN-、Cl-、I-
(6)常温下![]() =1×10-12的溶液:K+、AlO2-、CO32-、Na+
=1×10-12的溶液:K+、AlO2-、CO32-、Na+
(7)c(H+)=0.1 mol·L-1的溶液:Na+、NH4+、SO42-、S2O32-
A.(3)(6)B.(2)(3)(6)C.(6)D.(2)(6)(7)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D、E五种化合物均含有某种短周期常见元素,它们的转化关系如图所示,其中A的溶液为澄清溶液,C为难溶的白色固体,E易溶于水,取A的溶液灼烧,焰色反应为浅紫色(透过蓝色钴玻璃)。
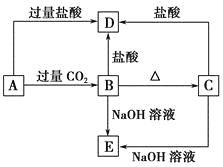
(1)写出化学式:A_______,B_______,C_______,D_______,E_______。
(2)写出下列反应的离子方程式:
A→B:_________________________________________________________;
A→D:__________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】镁一空气电池是一种能被水激活的一次性储备电池,原理如图所示。下列说法错误的是

A. 放电时,外电路电子由镁电极流向多孔碳材料电极
B. 放电时,正极的电极反应式为O2+ 4e—+ 2H2O =4OH
C. 理论上,外电路中流过2 mol电子时,负极质量增加58 g
D. 电池反应产物Mg(OH)2经过灼烧与还原可制成镁锭循环利用
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列事实不能用化学平衡移动原理解释的是
A.收集氯气可以用排饱和食盐水的方法
B.在一定条件下,氢气与碘蒸汽反应达平衡后,加压,混合气体颜色变深
C.可用浓氨水和氢氧化钠固体快速制取氨气
D.合成三氧化硫过程中使用过量的氧气,以提高二氧化硫的转化率
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学课外活动小组拟用铅蓄电池进行电絮凝净水的实验探究,设计的实验装置示意图如下。下列叙述正确的是
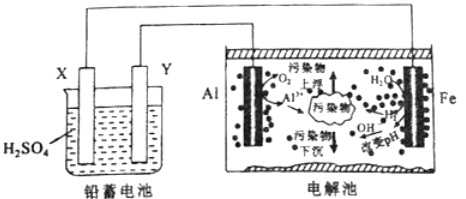
A.Y的电极反应为:Pb-2e-+SO42-=PbSO4
B.电解池内仅发生反应:2Al+6H2O=2Al(OH)3↓+3H2↑
C.若电解池阴极上有0.5mol H2生成,则铅蓄电池中消耗H2SO4为98g
D.用电絮凝法净化过的水,pH显著升高
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】采用如下装置(夹持和加热仪器已略去)电解饱和食盐水,并检验氯气的氧化性,同时用电解产生的H2还原CuO粉末来测定Cu的相对原子质量。

(1)写出电解饱和食盐水的离子方程式_________________________________。
(2)为完成上述实验,正确的连接顺序为A连_______;B连_______ (填写导管口字母)。
(3)若检验氯气的氧化性,则乙装置的a瓶中溶液可以是下列试剂中的___________。
a.酸性高锰酸钾溶液 b.淀粉碘化钾溶液 c.亚硫酸钠溶液 d.氯化亚铁溶液
(4)丙装置的c瓶中盛放的试剂为___________,作用是______________________。
(5)为测定Cu的相对原子质量,设计了如下甲、乙两个实验方案:
精确测量硬质玻璃管的质量为a g,放入CuO后,精确测量硬质玻璃管和CuO的总质量为b g(假设CuO充分反应),实验完毕后:
甲方案:通过精确测量硬质玻璃管和Cu粉的总质量为c g,进而确定Cu的相对原子质量。
乙方案:通过精确测定U型管b反应前后的质量变化,得到生成水的质量d g,进而确定Cu的相对原子质量。
①请你分析并回答:___________方案所测结果更准确。若按合理方案测定的数据计算,Cu的相对原子质量为________________。
②不合理的方案会造成测定结果___________(填“偏低、偏高或无影响”)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com