
常温下,0.1mol·L﹣1一元酸HA与等浓度KOH溶液等体积混合后,所得溶液中部分微粒组分及浓度如图所示,下列说法正确的是
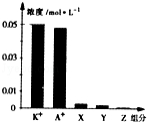
A.该混合溶液pH=7.0
B.原HA溶液中:c(HA)>c(H+)>c(A﹣)
C.图中X表示HA,Y表示OH﹣,Z表示H+
D.混合溶液中:c(X)+x(A﹣)=c(K+)
科目:高中化学 来源:2016-2017学年宁夏高二上月考二化学卷(解析版) 题型:推断题
A、B、C、D、E五种有机物,它们的分子分别由—CH3、—OH、—COOH、—CHO、—C6H5( 代表苯基)中的两种组成,这些化合物的性质如下所述:
①A能够发生银镜反应,且相对分子质量为44;
②B溶液加入氯化铁溶液中,溶液显紫色;
③C和E在有浓硫酸存在并加热的条件下,能发生酯化反应,C和E的相对分子质量之比为8:15;
④B和E都能跟氢氧化钠溶液反应,而A、C、D则不能;
⑤D属于烃类,且D能使酸性高锰酸钾溶液 褪色,还能发生硝化反应。
褪色,还能发生硝化反应。
由此可知,A、B、C、D、E的结构简式是
 A____________;B____________;C____________;D____________;E____________。
A____________;B____________;C____________;D____________;E____________。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年湖北省高一12月月考化学试卷(解析版) 题型:实验题
一种新型高效净水剂PAFC(聚合氯化铁铝[AlFe(OH)nC16-n]m),广泛用于日常生活用水和工业污水的处理。某化工厂欲以工业生产废料(金属铁、铝及其氧化物)为原料制取PAFC,设计生产流程如下:
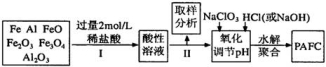
请回答下列问题:
(1)用l0 mol/L的浓盐酸配制2mol/L的稀盐酸,所用玻璃仪器除量筒和玻璃棒外,还有 。
A.容量瓶 B.烧杯 C.烧瓶 D.胶头滴管
(2)下列关于PAFC的说法中正确的有( )
A.PAFC是一种无机高分子化合物
B.PAFC中Fe显+2价
C.PAFC溶于水电离出OH—,是碱
D.PAFC在强酸性和强碱性溶液中均不能稳定存 在
在
(3)步骤Ⅱ中取样分析的目的是( )
A.测定溶液中Fe2+与Fe3+的含量比
B.测定原料是否完全溶解
C.测定溶液中Fe2+的含量,以确定加入NaClO3的量
D.测定溶液中Al3+的含量
(4)写出向溶液中加入NaClO3时,发生反应的离子方程式为______________________。
(5)该化工厂的化验室为测定产品PAFC中A1和Fe的含量,进行下列试剂的选择和基本操作:测定时所需的试剂有_______________。
A.NH3·H2O B.NaOH C.CO2 D .NaClO3
.NaClO3
(6)在测定过程中的操作顺序是: 过滤、___________、灼烧、_________、称量。(写操作名称)。
(7)测定时,直接称量的是____________和_____________的质量(填化学式)。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年湖北省高一12月月考化学试卷(解析版) 题型:选择题
下列各物质,能由单质间发生化合反应得到,但不能由单质与酸发生置换反应得到的是
A.MgCl2 B.FeCl2 C.AlCl3 D.CuCl2
查看答案和解析>>
科目:高中化学 来源:2016-2017学年湖北省高二12月月考化学试卷(解析版) 题型:填空题
工业废水中常含有一定量的Cr2O72﹣和CrO42﹣,它们会对人类及生态系统产生很大的伤害,必须进行处理。该法的工艺流程为CrO42﹣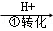 Cr2O72﹣
Cr2O72﹣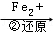 Cr3+
Cr3+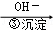 Cr(OH)3↓ 其中第①步存在平衡:2CrO42﹣(黄色)+2H+
Cr(OH)3↓ 其中第①步存在平衡:2CrO42﹣(黄色)+2H+ Cr2O72﹣(橙色)+H2O
Cr2O72﹣(橙色)+H2O
(1)若平衡体系的pH=2,则溶液显 色。
(2)能说明第①步反应达平衡状态的是 。(选填编号)
a.Cr2O72﹣和CrO42﹣的浓度相同 b.v正(Cr2O72﹣)=2v逆(CrO42﹣)
c.溶液的颜色不变 d.溶液的pH值不变
(3)写出第②步中Cr2O72﹣转变为Cr3+的离子方程式: .
(4)向Cr2(SO4)3溶液中,滴加NaOH,当pH=4.6时,开始出现Cr(OH)3沉淀,随着pH的升高,沉淀增多,但当pH≥13时,沉淀消失,出现亮绿色的[Cr(OH)4]﹣离子.其平衡关系如下:H++[Cr(OH)4]﹣(亮绿色) Cr(OH)3(s,灰绿色)+H2O
Cr(OH)3(s,灰绿色)+H2O  Cr3+(紫色)+H2O +3OH﹣.现向0.05mol·L﹣1的Cr2(SO4)3溶液50mL中,加入等体积0.6mol·L﹣1的NaOH溶液,充分反应后,溶液中可观察到的现象为 。
Cr3+(紫色)+H2O +3OH﹣.现向0.05mol·L﹣1的Cr2(SO4)3溶液50mL中,加入等体积0.6mol·L﹣1的NaOH溶液,充分反应后,溶液中可观察到的现象为 。
(5)在Na[Cr(OH)4]和Na2Cr2O7混合后的溶液中加入H2SO4酸化,铬元素以 形式存在(填写离子符号)。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年湖北省高二12月月考化学试卷(解析版) 题型:选择题
常温下,浓度均为0.1mol/L的三种溶液:①CH3COOH溶液②NaOH溶液③CH3COONa溶液,下列说法中不正确的是(忽略混合前后溶液体积变化)
A.溶液的pH值:②>③>①
B.水电离出的c(OH﹣):③>①>②
C.①和②等体积混合后的溶液:c(CH3COOH)+c(CH3COO﹣)=0.1mol/L
D.②和③等体积混合后的溶液:c(Na+)+c(H+)=c(OH﹣)+c(CH3COO﹣)
查看答案和解析>>
科目:高中化学 来源:2016-2017学年湖北省高二12月月考化学试卷(解析版) 题型:选择题
在醋酸溶液中,CH3COOH电离达到平衡的标志是
A.溶液显电中性 B.溶液中检测不出CH3COOH分子存在
C.氢离子浓度恒定不变 D.c(H+)=c(CH3COO-)
查看答案和解析>>
科目:高中化学 来源:2016-2017学年湖北省高一上期中化学试卷(解析版) 题型:选择题
取100 mL 1.0mol·L-1和200 mL 2.0 mol·L-1的盐酸混合后,全部注入500 mL的容量瓶中,加水稀释至刻度线,该混合溶液中H+的物质的量浓度是( )
A.0.5 mol·L-1 B.1.0 mol·L-1 C.1.5. mol·L-1 D.2.0 mol·L-1
查看答案和解析>>
科目:高中化学 来源:2016-2017学年天津市高二12月月考化学卷(解析版) 题型:选择题
A、B、C、D四种物质皆易溶于水,且在水溶液(稀)中存在如下化学平衡,加入水稀释后,平衡向正反应方向移动的是
A.A+B C+D B.A
C+D B.A C+D
C+D
C.A+B C+H2O D.A+2B+H2O
C+H2O D.A+2B+H2O C
C
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com