
【题目】在密闭容器中进行下列反应:M(g)+N(g)==R(g)+2L。此反应符合下列图象,R%为R在平衡混合物中的体积分数,该反应是

A. 正反应为吸热反应 L是气体
B. 正反应为放热反应 L是气体
C. 正反应为吸热反应 L是固体
D. 正反应为放热反应 L是固体或液体
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】A、B、C、D、E是元素周期表中原子序数依次增大的前四周期元素。A与B同周期,且A元素原子核外s能级有1个未成对电子;B元素的原子核外p电子比s电子少1;C元素的原子序数比B元素多1;D元素的原子价电子有6个未成对电子,它的一种化合物常用于检验酒驾;E元素的原子价电子有4个未成对电子。请回答下列问题:
(1)第一电离能介于A和B之间的同周期元素有___________(填元素符号)。
(2)B元素的最高价氧化物的水化物在水溶液中能完全电离,电离所得阴离子的空间构型为______。写出2种与该阴离子互为等电子体的微粒的化学式:_____。画出基态D原子的价电子排布图:_____。
(3)C元素对应的简单氢化物的沸点明显高于同族其他元素对应的简单氢化物,其原因是___________。
(4)元素D可以形成的配合物如图所示。
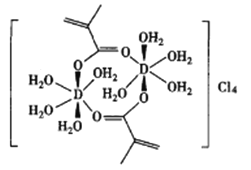
①该配合物中碳原子的杂化类型为___________。
②该配合物中所含化学键的类型不包括___________(填字母)。
a.极性共价键 b.非极性共价键 c.配位键 d.离子键 e.金属键 f.σ键 g.π键
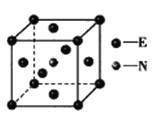
(5)元素E的单质和氮气在640℃可发生置换反应产物之一的晶胞结构如图所示,该反应的化学方程式为___。若该晶体的密度是ρg·cm-3,则两个最近的E原子间的距离为___________cm。(用NA表示阿伏加德罗常数的值)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】海水是一个巨大的化学资源库,下列有关海水综合利用的说法正确的是( )
A. 海水中含有钾元素,只需经过物理变化能得到钾单质
B. 海水蒸发制海盐的过程中只发生了化学变化
C. 从海水中可以得到NaCl,电解熔融NaCl可制备Na
D. 利用潮汐发电是将化学能转化为电能
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】只给出下列甲和乙中对应的物理量,不能求出物质的量的是( )
A.甲:物质中的粒子数;乙:阿伏加德罗常数
B.甲:标准状况下的气体摩尔体积;乙:标准状况下的气体的体积
C.甲:固体的体积;乙:固体的密度
D.甲:溶液中溶质的物质的量浓度;乙:溶液体积
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对于反应:4CO(g)+2NO2(g)=4CO2(g)+N2(g)△H=-1200KJ/mol,温度不同(T2>T1)其他条件相同时,下列图像正确的是

A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据下列实验操作和现象所得到的结论不正确的是
选项 | 实验操作和现象 | 实验结论 |
A | 向苯酚浊液中加入Na2CO3溶液,溶液变澄清 | 酸性:苯酚>HCO |
B | 用pH计测定等浓度的Na2CO3和NaClO溶液的pH | 后者pH比前者的大 |
C | 钠与乙醇反应平缓;钠与水反应剧烈 | 羟基中氢的活性:C2H5OH<H2O |
D | 在2 mL 0.01 mol·L-1的Na2S溶液中先滴入几滴0.01 mol·L-1 ZnSO4溶液有白色沉淀生成,再滴入0.01 mol·L-1 CuSO4溶液,又出现黑色沉淀 | Ksp(CuS)<Ksp(ZnS) |
A. AB. BC. CD. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用微生物可将废水中苯酚的化学能直接转化为电能,装置如图所示。电池工作时,下列说法正确的是

A. a极为正极,发生氧化反应
B. b极的电极反应式为:2NO3-+12H++10e-===N2↑+6H2O
C. 中间室的Cl-向右室移动
D. 左室消耗苯酚 (C6H5OH) 9.4 g时,用电器流过2.4 mol电子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有下列十种物质:①O2 ②铝 ③Na2O ④CO2 ⑤H2SO4 ⑥Ba(OH)2 ⑦红褐色的氢氧化铁液体 ⑧氨水 ⑨盐酸 ⑩CaCO3
(1)按物质的树状分类法填写表格的空白处:
_________ | 氧化物 | _________ | _________ | 电解质 | |
属于该类的物质 | ② | _________ | ⑧ ⑨ | ⑦ | _________ |
(2)写出实验室制备①的化学方程式:____________________。
(3)上述十种物质中,有两种物质之间可发生H++OH-=H2O,该离子反应对应的化学方程式为_________________。
(4)写出制备⑦的化学方程式:__________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】锌是一种常用金属,冶炼方法有火法和湿法。回答下列问题:
I.镓(Ga)是火法冶炼锌过程中的副产品,镓与铝同主族且相邻,化学性质与铝相似。
(1)Ga在元素周期表中的位置为___________。
(2)下列有关镓和镓的化合物的说法正确的是___________(填字母)。
A一定条件下,Ga可溶于盐酸和氢氧化钠溶液
B常温下,Ga可与水剧烈反应放出氢气
C.Ga2O3可由Ga(OH)3受热分解得到
D一定条件下,Ga2O3可与NaOH反应生成盐
Ⅱ工业上利用锌熔砂(主要含ZnO、ZnFe2O4,还含有少量 CaO, FeO、CuO、NiO等氧化物)湿法制取金属锌的流程如图所示:
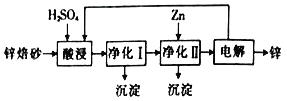
已知:Fe的活泼性强于Ni。
(3) ZnFe2O4可以写成ZnO·Fe2O3,写出ZnFe2O4与H2SO4反应的化学方程式:___________。
(4)净化Ⅰ工操作分为两步:第一步是将溶液中少量的Fe2+氧化;第二步是控制溶液pH,仅使Fe3+转化为Fe(OH)3沉淀,净化I生成的沉淀中还含有溶液中的悬浮杂质,溶液中的悬浮杂质被共同沉淀的原因是______________________。
(5)净化Ⅱ中加入Zn的目的是______________________。
Ⅲ.(6)某化学课外小组拟用废旧电池锌皮(含杂质铁),结合如图所示信息,从提供的试剂中选取适当试剂,制取纯净的ZnSO4·7H2O。
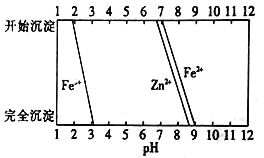
实验步骤如下:
①将锌片完全溶于稍过量的3mol·L-1的稀硫酸,加入___________(填字母,下同);
A.30%H2O2 B新制氯水 C.FeCl3溶液 D.KSCN溶液
②加入___________;
A纯锌粉 B纯碳酸钙粉末 C.纯ZnO粉末 D.3mol·L-1的稀硫酸
③加热到60℃左右并不断搅拌;
④趁热过滤得ZnSO4溶液,再蒸发浓缩、冷却结晶,过滤、洗涤、干燥。
其中步骤③加热的主要目的是_________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com