
【题目】“低碳经济”备受关注,二氧化碳的回收利用是环保和能源领域研究的热点课题。
(1)已知:①CO(g)+H2O(g)![]() H2(g)+CO2(g)△H=-41kJ·mol-1
H2(g)+CO2(g)△H=-41kJ·mol-1
②CH4(g)![]() C(s)+2H2(g)△H=+73kJ·mol-1
C(s)+2H2(g)△H=+73kJ·mol-1
③2CO(g)![]() C(s)+CO2(g)△H=-171kJ·mol-1
C(s)+CO2(g)△H=-171kJ·mol-1
写出CO2与H2反应生成CH4和水蒸气的热化学方程式:_________________________。
(2)CO2与H2在催化剂作用下可以合成二甲醚,反应原理如下:2CO2(g)+6H2(g)![]() CH3OCH3(g)+3H2O(g) △H。某温度下,向体积为2L的密闭容器中充入CO2与H2,发生上述反应。测得平衡混合物中CH3OCH3(g)的体积分数[φ(CH3OCH3) 与起始投料比Z[Z=
CH3OCH3(g)+3H2O(g) △H。某温度下,向体积为2L的密闭容器中充入CO2与H2,发生上述反应。测得平衡混合物中CH3OCH3(g)的体积分数[φ(CH3OCH3) 与起始投料比Z[Z=![]() ]的关系如图1所示;CO2的平衡转化率(a)与温度(T)、压强(p)的关系如图2所示。
]的关系如图1所示;CO2的平衡转化率(a)与温度(T)、压强(p)的关系如图2所示。

①当Z=3时,CO2的平衡转化率a=__________%。
②当Z=4时,反应达到平衡状态后,CH3OCH3的体积分数可能是图1中的_________点(填"D"、"E"或“F")。
③由图2可知该反应的△H_______0(选填“>”、“<“或“=”,下同),压强p1、p2、p3由大到小的顺序为__________。
④若要进一步提高H2的平衡转化率,除了可以适当改变反应温度和压强外,还可以采取的措施
有________________(任写一种)。
(3)我国科研人员研制出的可充电"Na-CO2"电池,以钠箔和多壁碳纳米管(MWCNT)为电极材料,总反应为4Na+3CO2![]() 2Na2CO3+C。放电时该电池“吸入”CO2,其工作原理如图3所示。
2Na2CO3+C。放电时该电池“吸入”CO2,其工作原理如图3所示。

①放电时,正极的电极反应式为____________________。
②若生成的Na2CO3和C全部沉积在正极表面,当正极增加的质量为28g时,转移电子的物质的量为__________。
③可选用高氯酸钠-四甘醇甲醚作电解液的理由是________________________。
【答案】 CO2(g)+4H2(g)![]() CH4(g)+2H2O(g) △H=-162 kJ·mol-1 75 F < p1>p2>p3 将二甲醚从体系中分离或增大n(CO2)∶n(H2) 3CO2+4Na++4e-=2Na2CO3+C 0.5mol 导电性好、与金属钠不反应、难挥发等(答案合理即给分)
CH4(g)+2H2O(g) △H=-162 kJ·mol-1 75 F < p1>p2>p3 将二甲醚从体系中分离或增大n(CO2)∶n(H2) 3CO2+4Na++4e-=2Na2CO3+C 0.5mol 导电性好、与金属钠不反应、难挥发等(答案合理即给分)
【解析】(1)已知:①CO(g)+H2O(g)![]() H2(g)+CO2(g)△H=-41kJ·mol-1
H2(g)+CO2(g)△H=-41kJ·mol-1
②CH4(g)![]() C(s)+2H2(g)△H=+73kJ·mol-1
C(s)+2H2(g)△H=+73kJ·mol-1
③2CO(g)![]() C(s)+CO2(g)△H=-171kJ·mol-1
C(s)+CO2(g)△H=-171kJ·mol-1
根据盖斯定律可知③-①×2-②即得到CO2与H2反应生成CH4和水蒸气的热化学方程式为CO2(g)+4H2(g)![]() CH4(g)+2H2O(g)△H=-162kJ·mol-1。
CH4(g)+2H2O(g)△H=-162kJ·mol-1。
(2)①当Z=3时CH3OCH3(g)的体积分数为15%,根据方程式可知
2CO2(g)+6H2(g)![]() CH3OCH3(g)+3H2O(g)
CH3OCH3(g)+3H2O(g)
起始量(mol) 2 6 0 0
转化量(mol) 2x 6x x 3x
平衡量(mol) 2-2x 6-6x x 3x
则![]() ,解得x=0.75,所以CO2的平衡转化率a=75%。
,解得x=0.75,所以CO2的平衡转化率a=75%。
②反应物按照化学计量数比进行反应时二甲醚的体积分数最高,则当Z=4时,反应达到平衡状态后CH3OCH3的体积分数可能是图1中的F点。③由图2可知压强相同时升高温度转化率降低,所以正反应是放热反应,则该反应的△H<0;正反应体积减小,温度不变时增大压强转化率增大,则压强p1、p2、p3由大到小的顺序为p1>p2>p3。④正反应是体积减小的放热反应。则要进一步提高H2的平衡转化率,除了可以适当改变反应温度和压强外,还可以采取的措施有将二甲醚从体系中分离或增大n(CO2)∶n(H2)。
(3)①放电时,正极发生得到电子的还原反应,则根据总反应式可知电极反应式为3CO2+4Na++4e-=2Na2CO3+C;②根据反应式可知每转移4mol电子,正极质量增加2×106g+12g=224g,所以当正极增加的质量为28g时,转移电子的物质的量为![]() 。③根据题干信息以及金属钠的化学性质可知可选用高氯酸钠-四甘醇甲醚作电解液的理由是导电性好、与金属钠不反应、难挥发等。
。③根据题干信息以及金属钠的化学性质可知可选用高氯酸钠-四甘醇甲醚作电解液的理由是导电性好、与金属钠不反应、难挥发等。


科目:高中化学 来源: 题型:
【题目】固定容积为2L的密闭容器中发生反应xA(g)+yB(g)![]() zC(g),图I表示t℃时容器中各物质的量随时间的变化关系,图II表示平衡常数K随温度变化的关系。结合图像判断,下列结论正确的是
zC(g),图I表示t℃时容器中各物质的量随时间的变化关系,图II表示平衡常数K随温度变化的关系。结合图像判断,下列结论正确的是
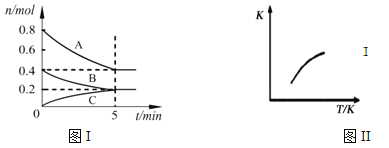
A. 该反应可表示为:2A(g)+B(g)![]() C(g)ΔH﹤0
C(g)ΔH﹤0
B. t℃时该反应的平衡常数K=6.25
C. 当容器中气体密度不再变化时,该反应达到平衡状态
D. t℃,在第6 min时再向体系中充入0.4 mol C,再次达到平衡时C的体积分数大于0.25
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度和有催化剂条件下,恒容密闭容器中发生反应N2+3H2 2NH3,下列说法正确的是( )
t/min | 0 | 5 | 10 | 15 | 20 |
c(NH3)/(mol·L-1) | 0 | 1.00 | 1.60 | 1.80 | 1.80 |
A. 0~10min内,v(NH3)=0.16mol·L-1·min-1 B. 0~10min内,v(N2)=0.18mol·L-1·min-1
C. 0~10min内,v(N2)=0.16mol·L-1·min-1 D. 15~20min内,反应v(N2)正= v(N2)逆=0
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2015年中国药学家屠呦呦获得诺贝尔医学奖,以表彰她在青蒿素研究方面做出的突出贡献。提取青蒿素通常可以用乙醚浸取,这与下列哪种方法的原理相同
A.蒸馏法B.过滤法C.结晶法D.萃取法
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】科学家利用太阳能分解水生成的氢气在催化剂作用下与二氧化碳反应生成甲醇,并开发出直接以甲醇为燃料的燃料电池。已知H2(g)、CO(g)和CH3OH(l)的燃烧热△H分别为—285.8kJ·mol-1、—283.0kJ·mol-1和—726.5kJ·mol-1。请回答下列问题:
(1)用太阳能分解10mol水消耗的能量是_____________;
(2)甲醇不完全燃烧生成一氧化碳和液态水的热化学方程式为_______________________________________________________;
(3)在容积为2L的密闭容器中,由CO2和H2合成甲醇,在其他条件不变的情况下,考查温度对反应的影响,实验结果如下图所示(注:T1、T2均大于300℃);
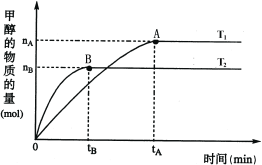
下列说法正确的是________(填序号)
a.温度为T1时,从反应开始到平衡,生成甲醇的平均速率为:v(CH3OH)=![]() mol·L-1·min-1
mol·L-1·min-1
b.T1> T2
c.该反应为放热反应
d.处于A点的反应体系从T1变到T2,达到平衡时![]() 增大
增大
(4)在T1温度时,将1molCO2和3molH2充入一密闭恒容器中,充分反应达到平衡后,若CO2转化率为α, 则容器内的压强与起始压强之比为_______________________;
(5)在直接以甲醇为燃料的电池中,电解质溶液为碱性,负极的反应式为________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验中,所使用的装置(夹持装置略)、试剂和操作方法有错误的是
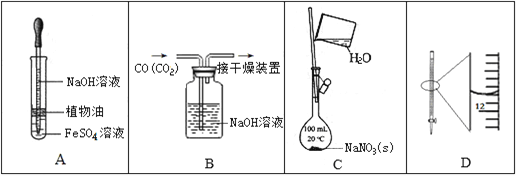
A. 观察Fe(OH)2的生成
B. 除去CO中的CO2
C. 配制一定物质的量浓度的NaNO3溶液
D. 25 mL滴定管读数为11.80 mL
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列指定反应的离子方程式不正确的是
A. 钠与水反应:2Na+2H2O![]() 2Na++2OH–+H2↑
2Na++2OH–+H2↑
B. 向碳酸氢铵溶液中加入足量石灰水: Ca2++HCO3+OH–![]() CaCO3↓+H2O
CaCO3↓+H2O
C. 向氢氧化钡溶液中加入稀硫酸: Ba2++2OH +2H++SO42![]() BaSO4↓+2H2O
BaSO4↓+2H2O
D. 泡沫灭火器反应原理:3HCO3+Al3+![]() 3CO2↑+Al(OH)3↓
3CO2↑+Al(OH)3↓
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃、101kPa时,有以下能量转化图,下列说法不正确的是( )
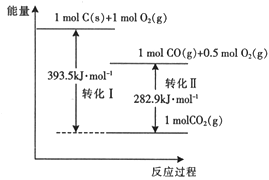
A. 转化Ⅱ的热化学方程式2CO(g)+O2(g)=2CO2(g) △H=-282.9 kJ·mol-1
B. 相同条件下,1mol C(s )和0.5 mol O2(g)总能量高于1mol CO(g)的能量
C. 由C→CO 的热化学方程式2C(s)+O2(g)=2CO(g) △H=-221.2 kJ·mol-1
D. CO2(g)分解为C(s)和O2(g)是吸热反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com