
��8�֣� CH3OH��g��+H2O��g��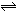 CO2��g��+3H2��g�����÷�Ӧ������ӦΪ���ȷ�Ӧ���������ĿҪ��ش��������⣺
CO2��g��+3H2��g�����÷�Ӧ������ӦΪ���ȷ�Ӧ���������ĿҪ��ش��������⣺
��1���������������������½����¶ȣ����淴Ӧ���� �� �������С�����䡱����ͬ�����������������������¼�ѹ��������Ӧ���� ����
��2��һ�������£������Ϊ2L���ܱ������г���1molCH3OH(g)��3molH2O(g)��20s��û�������ѹǿ�Ƿ�Ӧǰ��1.2�������ü״���ʾ�÷�Ӧ������Ϊ ��
��3���жϸÿ��淴Ӧ�ﵽƽ��״̬�������ǣ�����ţ� ��
�� A �� v����CH3OH��=v��(CO2) B �����������ܶȲ���
C�� ��������ƽ����Է����������� D ��CH3OH��H2O��CO2��H2��Ũ�ȶ����ٷ����仯

| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| ���¶���ͬ��3���ܱ������У�����ͬ��ʽͶ�뷴Ӧ����ֺ��¡���ѹ����÷�Ӧ�ﵽƽ��ʱ���й�������� ����֪CO��g��+2H2��g��  CH3OH��g����H=-90.7kJ/mol�� CH3OH��g����H=-90.7kJ/mol��
|
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
 úֱ��ȼ�յ����������ʽϵͣ�Ϊ����������ʣ���ҵ�Ͻ�ú������ת���CO��H2�����ٺϳ��Ҵ��������ѵȶ�����Դ��
úֱ��ȼ�յ����������ʽϵͣ�Ϊ����������ʣ���ҵ�Ͻ�ú������ת���CO��H2�����ٺϳ��Ҵ��������ѵȶ�����Դ��| ���� | H2 | CO | CO2 | ��CH3��2O | CH3OH | H2O |
| ������� | 0.54 | 0.045 | 0.18 | 0.18 | 0.015 | 0.03 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
 ��CO2ת���ɼ״�ȼ���Ǽ��ţ�������һ�ֿ�ѧ��������ԭ��
��CO2ת���ɼ״�ȼ���Ǽ��ţ�������һ�ֿ�ѧ��������ԭ��| һ������ |
| A������x��ʾ����CH3OHŨ�ȱ仯������Y��ʾCO2Ũ�ȱ仯 |
| B���ӷ�Ӧ��ʼ��ƽ�⣬�����ķ�Ӧ����v��H2��=0.225mol/��L?min�� |
| C��ƽ��ʱH2��ת����Ϊ75% |
| D���÷�Ӧ��ƽ�ⳣ��K=3 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
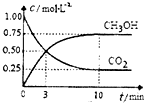 ��֪��CO2��g��+3H2��g��?CH3OH��g��+H2O��g����H=-49��OkJ?mol-1 һ�������£������Ϊ11���ܱ������г���lmolCO2��3mol H2�����CO2��CH3OH��g����Ũ����ʱ��仯������ͼ��ʾ��������������ȷ���ǣ�������
��֪��CO2��g��+3H2��g��?CH3OH��g��+H2O��g����H=-49��OkJ?mol-1 һ�������£������Ϊ11���ܱ������г���lmolCO2��3mol H2�����CO2��CH3OH��g����Ũ����ʱ��仯������ͼ��ʾ��������������ȷ���ǣ�������| A�������¶�ƽ�ⳣ��K���� | B����Ӧ�ﵽƽ��״̬ʱ��CO2��ƽ��ת����Ϊ75% | C��3minʱ����CO2��Ũ�ȱ�ʾ������Ӧ���ʵ�����CH3OH��Ũ�ȱ�ʾ���淴Ӧ���� | D���ӷ�Ӧ��ʼ��ƽ�⣬H2��ƽ����Ӧ����v ��H2��=0.075mol?L-1?min-1 |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com