
����Ŀ����Ҫ������������⡣
��1��Ϊ�����ú�������ʣ�����������Ϊ��ȼ�����壬��Ҫ��Ӧ��̼��ˮ������Ӧ����ˮú�������л�ԭ����___��
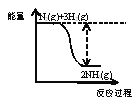
��2�����Ƕ�ֲ����������ȱ�ٵ�Ԫ�أ��ϳɰ��ķ�Ӧ����������ʳ�����Ӧ���£�N2��g����3H2��g��![]() 2NH3��g����
2NH3��g����
�ٺϳɰ��ķ�Ӧ�е������仯��ͼ��ʾ���÷�Ӧ��_____________��Ӧ������ȡ����ȡ�������ԭ���Ƿ�Ӧ�ﻯѧ���������յ�������_____________������ڡ���С�ڡ��������ﻯѧ���γɷų�����������
����һ�������£���һ������N2��H2�Ļ���������ij�ܱ������У�һ��ʱ�������������˵���÷�Ӧ�ﵽƽ��״̬����_____________������ţ���
a��������N2��H2��NH3���� b��N2��H2��NH3�����ʵ���֮��Ϊ1:3:2
c�������е�ѹǿ����ʱ��仯 d��N2��NH3Ũ�����
��3����ҵ���õ�ⱥ��ʳ��ˮ�ķ�����ȡ�������ռ���������仯ѧ��Ӧ����ʽΪ_________��
��4�����и���Ӧ�У�������ͼ��ʾ�����仯����_____________������ţ���

a��H2��Cl2�ķ�Ӧ b��Al������ķ�Ӧ c��Na��H2O�ķ�Ӧ d��Ba��OH��2��8H2O��NH4C1�ķ�Ӧ
��5����ˮ��Դǰ��������
���о�һ�ֺ�ˮ�����ķ���______________��
�ڲ��ÿ����������Ӻ�ˮ����ȡ��Ĺ����У����ռ�SO2����������Ӧ�����������Դﵽ������Ŀ�ģ��÷�Ӧ�����ӷ���ʽΪ________________________________��
���𰸡�C ���� С�� c 2NaCl + 2H2O ![]() 2NaOH + H2�� + C12�� d �����������������ӽ���������һ�ּ��ɣ� Br2��SO2��2H2O��4H����2Br����SO42��
2NaOH + H2�� + C12�� d �����������������ӽ���������һ�ּ��ɣ� Br2��SO2��2H2O��4H����2Br����SO42��
��������
(1)C��ˮ��Ӧ����CO����������ϻ��ϼ۵ı仯�������
(2)����ͼ��֪����Ӧ�������������������������������ѻ�ѧ���������������ɻ�ѧ���ͷ���������ƽ��ʱ���淴Ӧ������ȣ����ƽ�����������жϣ�
(3)��ⱥ��ʳ��ˮ��Ӧ�����������ռ���������ݴ���д��Ӧ�ķ���ʽ��
(4)��ͼ��֪���÷�Ӧ����������е����������ڷ�Ӧ����е����������������ȷ�Ӧ���ݴ��жϣ�
(5)�ٸ���Ŀǰ������ˮ�ij��������ش𣻢������������ռ�SO2��������ת���������ᣬͬʱ�������ᣬ�ݴ���д���ӷ���ʽ��
(1)C��ˮ��Ӧ����CO����������ӦΪC(s)+H2O(g)![]() CO (g)+H2(g)��ˮ��HԪ�صĻ��ϼ۽��ͣ�CԪ�ػ��ϼ����ߣ���������ΪH2O����ԭ����C���ʴ�Ϊ��C��
CO (g)+H2(g)��ˮ��HԪ�صĻ��ϼ۽��ͣ�CԪ�ػ��ϼ����ߣ���������ΪH2O����ԭ����C���ʴ�Ϊ��C��
(2)����ͼ��֪����Ӧ������������������������������÷�ӦΪ���ȷ�Ӧ�����ѻ�ѧ���������������ɻ�ѧ���ͷ���������H=���ѻ�ѧ����������-���ɻ�ѧ���ͷ�������0����֪���ѻ�ѧ����������С�����ɻ�ѧ���ͷ��������ʴ�Ϊ�����ȣ�С�ڣ�
��a����ӦΪ���淴Ӧ��������N2��H2��NH3���治���ж��Ƿ�Ϊƽ��״̬����a����b��N2��H2��NH3�����ʵ���֮��Ϊ1��3��2�����ʵ���ȡ������ʼ���ʵ�����ת���ʣ������ж��Ƿ�Ϊƽ��״̬����b����c���÷�ӦΪ��Ӧǰ���������ʵ������ȵķ�Ӧ���������е�ѹǿ����ʱ��仯��˵����Ӧ�ﵽƽ��״̬����c��ȷ��d��N2��NH3��Ũ��ȡ������ʼŨ����ת���ʣ�N2��NH3Ũ����Ȳ����ж��Ƿ�Ϊƽ��״̬����d���ʴ�Ϊ��c��
(3)��ⱥ��ʳ��ˮ������ȡ�������ռ����������Ӧ�Ļ�ѧ����ʽΪ2NaCl+2H2O![]() 2NaOH+H2��+Cl2�����ʴ�Ϊ��2NaCl+2H2O
2NaOH+H2��+Cl2�����ʴ�Ϊ��2NaCl+2H2O![]() 2NaOH+H2��+Cl2����
2NaOH+H2��+Cl2����
(4)a��H2��Cl2�ķ�Ӧ�����ڷ��ȷ�Ӧ����Ӧ����е�������������������е�����������a����b��Al������ķ�Ӧ�����ڷ��ȷ�Ӧ����Ӧ����е�������������������е�����������b����c��Na��H2O�ķ�Ӧ�����ڷ��ȷ�Ӧ����Ӧ����е�������������������е�����������c����d��Ba(OH)28H2O��NH4Cl�ķ�Ӧ���������ȷ�Ӧ����Ӧ����е�������������������е�����������d��ȷ����ѡd��
(5)�ٵ�����ˮ�ķ����У������ᾧ�������ӽ���Ĥ���������������༶�������ȣ��ʴ�Ϊ�������ᾧ�������ӽ���Ĥ���������������༶��������(��ѡһ��)��
�ڲ��ÿ����������Ӻ�ˮ����ȡ��Ĺ����У����ռ�SO2����������Ӧ�����������Դﵽ������Ŀ�ģ������������ռ�SO2��������ת���������ᣬͬʱ�������ᣬ��Ӧ�����ӷ���ʽΪBr2+SO2+2H2O=4H++SO42-+2Br-���ʴ�Ϊ��Br2+SO2+2H2O=4H++SO42-+2Br-��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������ߵ������£����������ɳ�����3O2![]() 2O3��һ�������¸÷�Ӧ�ﵽƽ��״̬�ı�־��(����)
2O3��һ�������¸÷�Ӧ�ﵽƽ��״̬�ı�־��(����)
A. ��λʱ��������2 mol O3��ͬʱ����3 mol O2
B. O2����������0.3 mol��L��1��s��1��O3����������0.2 mol��L��1��s��1
C. �����ڣ�2������O3��O2Ũ�����
D. �����ܶȲ��ٸı�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij�ֹ��صĹ���ԭ��Ϊ��AgCl(s)+Cu+(aq)![]() Ag(s)+Cu2+(aq)+Cl��(aq)��ͼΪ�ù��ط���װ�õ������[CO(NH2)2]�ļ�����Һ�����װ��ʾ��ͼ������������ȷ����
Ag(s)+Cu2+(aq)+Cl��(aq)��ͼΪ�ù��ط���װ�õ������[CO(NH2)2]�ļ�����Һ�����װ��ʾ��ͼ������������ȷ����

A. ���ع���ʱ��Ag��Ϊ����������������������Ӧ
B. ����װ����Һ��K+����A��
C. �����й���ʱ��Pt�缫�����ķ�ӦΪ��2Cl����2e��=Cl2��
D. ����װ�ù���ʱ��A���ĵ缫��ӦʽΪ��CO(NH2)2+8OH����6e���TCO32��+N2��+6H2O
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����һ���ݻ�Ϊ2 L���ܱ������У�����0.8 mol��A2�����0.6 mol B2���壬һ�������·������·�Ӧ��A2(g)��B2(g)![]() 2AB(g)����H<0����Ӧ�и����ʵ�Ũ����ʱ��ı仯�����ͼ��ʾ������˵������ȷ����
2AB(g)����H<0����Ӧ�и����ʵ�Ũ����ʱ��ı仯�����ͼ��ʾ������˵������ȷ����

A. ͼ��a���ֵΪ0.15 B. �÷�Ӧ��ƽ�ⳣ��K��0.03
C. �¶����ߣ�ƽ�ⳣ��Kֵ��С D. ƽ��ʱA2��ת����Ϊ62.5%
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��NA���������ӵ�������ֵ�������ж���ȷ����
A. 1LpH=13��Ba(OH)2��Һ�к�OH������ĿΪ0.2NA
B. 46gCH3CH2OH��C��H����ĿΪ6NA
C. 4.6gNa�뺬0.1 mol CH3COOH��ϡ������ȫ��Ӧ��ת�Ƶĵ�����Ϊ0.1NA
D. 2.24LCH4��0.5 molCl2��ַ�Ӧ���û��������ԭ����ΪNA
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���±���Ԫ�����ڱ���һ���֣���Ա��еĢ�~����Ԫ�أ���д���пհ�
��A | ��A | ��A | ��A | ��A | ��A | ��A | 0 | |
2 | �� | �� | �� | |||||
3 | �� | �� | �� | �� | �� | |||
4 | �� | �� |
(��Ԫ�ط��Ż�ѧʽ�ش���������)
(1)����ЩԪ���У���ѧ��������õ���_______����ԭ�ӽṹʾ��ͼ��_________��
(2)�õ���ʽ��ʾԪ�آ������ɵĻ�������γɹ��̣�________���û���������_______(��������������������)�����
(3)�����³�Һ̬�ķǽ���������_______��
(4)�������γ��������������Ԫ����_________����Ԫ�صĵ�����������������ˮ���ﷴӦ�Ļ�ѧ����ʽ��___________��
(5)�١��ޡ�������Ԫ�ص�����������Ӧ��ˮ�����У���������ǿ��˳������Ϊ_________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ʵ����Ҫ�ռ�һƿSO2���壬����ȷ���ռ������ǣ� ��
A.��ˮ������B.�����ſ�����
C.�����ſ�����D.�ű���ʳ��ˮ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����������Ʊ�����ˮ������������������������ˮ��Һ��Ϊ����������������������������ƹ�����̿��Ϊԭ���Ʊ���Na2SO4+2C![]() Na2S+2CO2��
Na2S+2CO2��

��1�����ƹ����ڱ���ʱ��ע��________��ԭ����________��
��2��ʵ��������ͼװ����Na2SO4��̿��Ϊԭ���Ʊ�Na2S����������������β���������������£�
����������˳��Ϊ________(������������Сд��ĸ��ʾ)��
�ڼ��װ�������ԣ���________��
�ܼ��ȣ�����ʵ�顣
��3���� a mol Na2SO4��2 a mol C�����������ַ�Ӧ��ʵ�ʵõ�Na2SС��amol����ʵ��Ľ�������________��
ijͬѧ��������ԭ�Ƕȷ�����������п��ܺ�������Na2SO3�������ʵ��֤����²��Ƿ����(��ѡ����Լ��У���̪��Һ�����ᡢϡ���ᡢ����ˮ) ________��
��4����ʵ��ⶨ����������̿����һ�������·�Ӧ�������ɵ����ʵ����������κ������Ϊ1�U3��CO2��CO�������塣��Ӧ����ʽΪ________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���о���ѧ��Ӧ�Ŀ������Ⱦ���ʮ����Ҫ�����塣�ش��������⣺
��1����Ӧ2SO2(g) + O2(g)![]() 2SO3(g)���Ʊ��������Ҫ��Ӧ���÷�ӦΪ���ȷ�Ӧ�������¶ȣ��淴Ӧ������_________��ʹ�ô���V2O5������Ӧ������__________ ����������ӡ��������䡱��С������
2SO3(g)���Ʊ��������Ҫ��Ӧ���÷�ӦΪ���ȷ�Ӧ�������¶ȣ��淴Ӧ������_________��ʹ�ô���V2O5������Ӧ������__________ ����������ӡ��������䡱��С������
��2�������£�ʵ������100 mL 6.0 mol��L��1���������п�۷�Ӧ��ȡ������
��Ϊ���ͷ�Ӧ���е����ʣ��ֲ�Ӱ��������������������Ӧ���м���____������� ����
A��CH3COONa���� B��KNO3����
C��K2SO4��Һ D��KHSO4��Һ
������Һ�еμ���������ͭ��Һ����Ӧ���ʼӿ죬ԭ����___________________��
��3��һ���¶��£�������̶����ܱ������У���ɫ����N����ɫ����M�����ʵ�����ʱ��仯������ͼ��ʾ����Ӧ��ƽ���ʱ����____________���÷�Ӧ�Ļ�ѧ����ʽ�ɱ�ʾΪ______________________________��
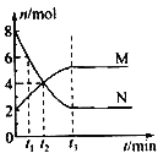
����˵�����ܹ��ж��÷�Ӧ����ƽ��״̬����______________���� ��ţ�
A��������ѹǿ���ٱ仯 B���������ɫ���ٱ仯
C��ÿ��Ӧ2 mol��N����1 mol��M D��������ܶȲ��ٷ����仯
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com