
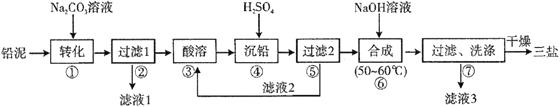
【题目】三盐基硫酸铅(3PbO·PbSO4·H2O,相对分子质量为990)简称“三盐”,白色或微黄色粉末,热稳定性能优良,主要用作聚氯乙烯的热稳定剂。“三盐”是由可溶性铅盐中加入硫酸生成硫酸铅,再加氢氧化钠而制得。以100.0吨铅泥(主要成分为PbO、Pb及PbSO4等)为原料制备三盐的工艺流程如下图所示。
已知:Ksp(PbSO4)=1.82×10-8,Ksp(PbCO3)=1.46×10-13;(2)铅与冷盐酸、冷硫酸几乎不起作用。请回答下列问题:
(1)写出步骤①“转化”的化学方程式_________________________,该反应能发生的原因是__________________________。
(2)步骤②“过滤1”后所得滤渣的主要成分为__________________________。
(3)步骤③“酸溶”,最适合选用的酸为_________________,为提高酸溶速率,可采取的措施是___________________(任意写出一条)。
(4)若步骤④“沉铅”后的滤液中c(Pb2+)=1.82×10-5mol·L-1,则此时c(SO42-)=_________ mol·L-1。
(5)从原子利用率的角度分析该流程的优点为_____________________。
(6)步骤⑥“合成”三盐的化学方程式为____________________________。若得到纯净干燥的三盐49.5t,假设铅泥中的铅元素有80%转化为三盐,则铅泥中铅元素的质量分数为_____%(结果保留一位小数)
【答案】 PbSO4+Na2CO3=PbCO3+Na2SO4 Ksp(PbSO4) > Ksp(PbCO3),容易实现沉淀的转化 Pb PbO PbCO3 HNO3 适当升温(适当增加硝酸浓度、减小滤渣颗粒大小等合理答案均可) 1×10-3 滤液2(HNO3溶液)可以循环利用 4PbSO4+6NaOH![]() 3PbO·PbSO4·H2O+3Na2SO4+2H2O 51.8
3PbO·PbSO4·H2O+3Na2SO4+2H2O 51.8
【解析】(1)步骤①向铅泥中加Na2CO3溶液,由表可以知道PbCO3的溶解度小于PbSO4的溶解度,所以步骤①“转化”的化学方程式:PbSO4+Na2CO3=PbCO3+Na2SO4;该反应能发生的原因是Ksp(PbSO4) > Ksp(PbCO3),容易实现沉淀的转化;正确答案:PbSO4+Na2CO3=PbCO3+Na2SO4;Ksp(PbSO4)> Ksp(PbCO3),容易实现沉淀的转化。
(2)铅泥(主要成分为PbO、Pb及PbSO4等),加入碳酸钠溶液后,由于PbO、Pb与碳酸钠不反应,反应又生成了PbCO3,所以步骤②“过滤1”后所得滤渣的主要成分为Pb、PbO、PbCO3;正确答案:Pb、PbO、PbCO3。
(3)根据题给信息可知:铅与冷盐酸、冷硫酸几乎不起作用,所以步骤③“酸溶”,最适合选用的酸为硝酸;为提高酸溶速率,可采取的措施是适当升温或适当增加硝酸浓度或减小滤渣颗粒大小等;正确答案:HNO3 ;适当升温(适当增加硝酸浓度、减小滤渣颗粒大小等合理答案均可)。
(4)根据Ksp(PbSO4)=1.82×10-8,c(SO42-)×c(Pb2+)=1.82×10-8,c(Pb2+)=1.82×10-5mol·L-1,所以c(SO42-)=1×10-3 mol·L-1;正确答案:1×10-3。
(5)Pb、PbO和PbCO3在硝酸的作用下转化成Pb(NO3)2, Pb(NO3)2中加稀H2SO4转化成PbSO4和硝酸,HNO3可循环利用;正确答案:滤液2(HNO3溶液)可以循环利用。
(6)硫酸铅与强碱溶液加热反应生成3PbO·PbSO4·H2O,化学方程式为4PbSO4+6NaOH![]() 3PbO·PbSO4·H2O+3Na2SO4+2H2O ; 若得到纯净干燥的三盐
3PbO·PbSO4·H2O+3Na2SO4+2H2O ; 若得到纯净干燥的三盐![]() ,则其中铅元素的质量为:
,则其中铅元素的质量为:![]() ,设铅泥中铅元素的质量分数为w,则
,设铅泥中铅元素的质量分数为w,则![]() 铅泥中铅元素为
铅泥中铅元素为![]() ,铅泥中的铅元素有
,铅泥中的铅元素有![]() 转化为三盐,有
转化为三盐,有![]() ,计算得出,w=0.518=51.8%;正确答案:51.8。
,计算得出,w=0.518=51.8%;正确答案:51.8。


科目:高中化学 来源: 题型:
【题目】下列变化过程中,需要加入还原剂才能实现的是( )
A.MnO2→MnO4-B.AlO2-→Al(OH)3
C.AsO33-→AsO43-D.MnO2→MnCl2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某校化学研究性学习小组欲设计实验验证Fe、Cu的金属活动性,他们提出
了以下两种方案。请你帮助他们完成有关实验项目:
方案Ⅰ:有人提出将大小相等的铁片和铜片,分别同时放入稀硫酸(或稀盐酸)中,观察产生气泡的快慢,据此确定它们的活动性。该原理的离子方程式为_______________________________________
方案Ⅱ:有人利用Fe、Cu作电极设计成原电池,以确定它们的活动性。试在下面的方框内画出原电池装置图,标出原电池的电极材料和电解质溶液,并写出电极反应式。
正极反应式:_______________________。
负极反应式:_______________________。
方案Ⅲ:结合你所学的知识,帮助他们再设计一个验证Fe、Cu活动性的简单实验方案(与方案Ⅰ、Ⅱ不能雷同):______________________,用离子方程式表示其反应原理:________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】I.由A、B、C、D四种金属按下表中装置进行实验。
装置 |
|
|
|
现象 | 二价金属A不断溶解 | C的质量增加 | A上有气体产生 |
根据实验现象回答下列问题:
(1)装置甲中负极的电极反应式是______________________________________。
(2)装置乙中正极的电极反应式是________________________________________。
(3)四种金属活泼性由强到弱的顺序是______________________。
II.分别按图所示甲、乙装置进行实验,图中两个烧杯中的溶液为相同浓度的稀硫酸,甲中A为电流表。

(1)下列叙述正确的是________。
A.两烧杯中铜片表面均无气泡产生 B.甲中铜片作正极,乙中铜片作负极
C.两烧杯中溶液中的H+浓度均减小 D.产生气泡的速率甲中的比乙中的慢
(2)甲装置中,某同学发现不仅铜片上有气泡产生,锌片上也产生了气体,原因可能是________________________________________________________________________。
(3)甲装置中,若把稀硫酸换成CuSO4溶液,试写出铜电极的电极反应________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在关于下图所示的原电池中,正确的是
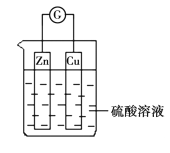
A. Zn被还原
B. 锌片上的电子经导线流向铜片
C. 该原电池运行一段时间后铜片的质量将增加
D. 该原电池将电能转变为化学能
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】党的十九大报告中提出加快生态文明体制改革,建设美丽中国,坚持人与自然和谐共生。下列有关观念或做法不宜提倡的是
A. 青山绿水就是金山银山 B. 创建环境友好型社会人人有责
C. 大力开发森林资源,发展乡村旅游 D. 积极做好治沙工作,做到人进沙退
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机化合物甲有镇咳、镇静的功效,其合成路线如下:

已知: (R、R'、R"代表烃基或氢)
(R、R'、R"代表烃基或氢)
(1)有机物甲的分子式为___________,有机物A中含有的官能团的名称为_________________。
(2)有机物B的名称是____________,由B→D 所需的反应试剂和反应条件为_______________。
(3)在上述①~⑤反应中,属于取代反应的有____________(填序号)。
(4)写出E→F的化学方程式____________________________。
(5)写出同时满足下列条件的甲的同分异构体的结构简式________。
(Ⅰ)属于芳香族化合物 (Ⅱ)核磁共振氢谱上只有2组峰
(6)根据题给信息,写出以CH4为原料制备CH3CHO的合成路线(其他试剂任选)___________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铁、铜的单质及它们的化合物与我们的生产、生活紧密相关。
(1)Cu处于周期表中______区,其最高能层的符号为______,基态铜原子的价电子排布式为________。
(2)向硫酸铜溶液中逐滴滴加氨水,首先形成蓝色沉淀,继续滴加氨水。沉淀溶解,得到深蓝色透明溶液,向深蓝色溶液中加入乙醇,析出深蓝色晶体。
①写出沉淀溶解,得到深蓝色透明溶液的离子方程式:________。
②为什么加入乙醇,能够析出深蓝色晶体?________________
③为什么NH3常在配合物中作配体,而NH4+却不能作配体?_______。
(3)Fe3+可以与SCN-、CN-、H2NCONH2(尿素)等多种配体形成很多的配合物。
①请写出一种与SCN-互为等电子体的分子:________。
②CN-的电子式为________。
③H2NCONH2(尿素)中N、C原子的杂化方式分别为_______、_______,组成尿素的4种元素的第一电离能由大到小的顺序为__________。
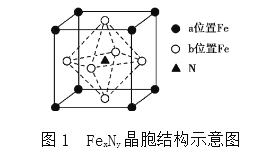
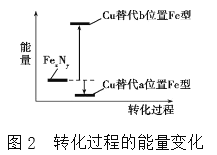
(4)某FeN,的晶胞如图1所示,Cu可以完全替代该晶体中a位置Fe或者b位置Fe,形成Cu替代型产物Fe(x-n)CunNy。FexNy转化为两种Cu替代型产物的能量变化如图2所示,其中更稳定的Cu替代型产物的化学式为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上常用浓氨水检查氯气管道是否泄漏,发生反应为:8NH3 +3C12=N2+6NH4C1, 该反应属于
A. 置换反应 B. 分解反应 C. 化合反应 D. 复分解反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com