
【题目】有机化合物甲有镇咳、镇静的功效,其合成路线如下:

已知: (R、R'、R"代表烃基或氢)
(R、R'、R"代表烃基或氢)
(1)有机物甲的分子式为___________,有机物A中含有的官能团的名称为_________________。
(2)有机物B的名称是____________,由B→D 所需的反应试剂和反应条件为_______________。
(3)在上述①~⑤反应中,属于取代反应的有____________(填序号)。
(4)写出E→F的化学方程式____________________________。
(5)写出同时满足下列条件的甲的同分异构体的结构简式________。
(Ⅰ)属于芳香族化合物 (Ⅱ)核磁共振氢谱上只有2组峰
(6)根据题给信息,写出以CH4为原料制备CH3CHO的合成路线(其他试剂任选)___________________________________________________。
【答案】 C10H14 溴原子 环戊醇 Cu/Ag,加热 ①② 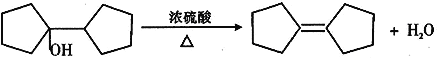
【解析】(1)根据有机物甲得结构简式可知,分子式为C10H14;有机物A是由环戊烷与溴发生取代反应生成的溴代烃,因此有机物A中含有的官能团为溴原子;正确答案:C10H14;溴原子。
(2)有机物A为一溴环戊烷,在氢氧化钾溶液加热的情况下发生取代反应生成醇,有机物B为环戊醇;醇发生催化氧化,所需的反应试剂为氧气,反应条件为Cu/Ag,加热;正确答案:环戊醇;氧气;Cu/Ag,加热。
(3)根据流程及反应条件下可知:反应①、②为取代反应;反应③、⑤为消去反应,反应④为加成反应;在上述①~⑤反应中,属于取代反应的有①②;正确答案:①②。
(4)根据题给信息可知:有机物![]() 与有机物
与有机物![]() 发生反应生成有机物
发生反应生成有机物![]() ,该有机物在浓硫酸作用下发生消去反应,化学方程式为
,该有机物在浓硫酸作用下发生消去反应,化学方程式为 ;正确答案:
;正确答案: 。
。
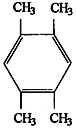
(5)有机物甲的分子式为C10H14,同根异构体满足的条件为(Ⅰ)属于芳香族化合物,含有苯环,(Ⅱ)核磁共振氢谱上只有2组峰,是一个高度对称的结构,具体结构为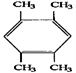 ;正确答案:
;正确答案: 。
。
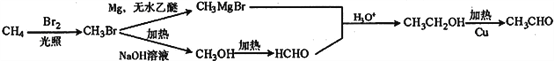
(6)根据题给信息可知:卤代烃在镁、无水乙醚的作用下,生成![]() ,甲烷最终氧化为甲醛,甲醛与
,甲烷最终氧化为甲醛,甲醛与![]() 在一定条件下生成乙醇,最终氧化为乙醛;合成流程如下:
在一定条件下生成乙醇,最终氧化为乙醛;合成流程如下: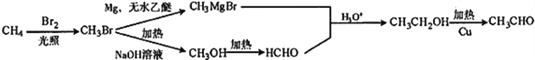 ;正确答案:
;正确答案: 。
。


 科学实验活动册系列答案
科学实验活动册系列答案科目:高中化学 来源: 题型:
【题目】工业酸性废水中的Cr2O72-可转化为Cr3+除去,实验室用电解法模拟该过程,结果如下表所示(实验开始时溶液体积为50mL,Cr2O72-的起始浓度、电压、电解时间均相同)。下列说法中,不正确的是
实验 | ① | ② | ③ |
电解条件 | 阴、阳极均为石墨 | 阴、阳极均为石墨, 滴加1mL浓硫酸 | 阴极为石墨,阳极为铁,滴加1mL浓硫酸 |
Cr2O72-的去除率/% | 0.922 | 12.7 | 57.3 |
A. 对比实验①②可知,降低pH可以提高Cr2O72-的去除率
B. 实验②中,Cr2O72-在阴极放电的电极反应式是Cr2O72-+6e-+14H+═2Cr3++7H2O
C. 实验③中,Cr2O72-去除率提高的原因是Cr2O72-+6 Fe2++14H+═2Cr3++6Fe3++7H2O
D. 实验③中,理论上电路中每通过6mol电子,则有1molCr2O72-被还原
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲元素的原子序数是19,乙元素原子核外有两个电子层,最外电子层上有6个电子;丙是元素周期表第ⅠA族中金属性最弱的碱金属元素。由此推断:
(1)甲元素在周期表中位于第_______周期;乙元素在周期表中位于第______族;丙元素的名称为________。
(2)甲的单质与水反应的离子方程式为____________________________,乙单质与丙单质反应的化学方程式为____________________________________,甲的单质与水反应的生成物的电子式为:_______________,___________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】三盐基硫酸铅(3PbO·PbSO4·H2O,相对分子质量为990)简称“三盐”,白色或微黄色粉末,热稳定性能优良,主要用作聚氯乙烯的热稳定剂。“三盐”是由可溶性铅盐中加入硫酸生成硫酸铅,再加氢氧化钠而制得。以100.0吨铅泥(主要成分为PbO、Pb及PbSO4等)为原料制备三盐的工艺流程如下图所示。
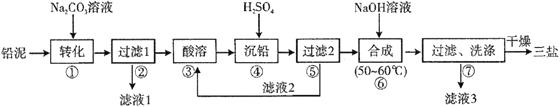
已知:Ksp(PbSO4)=1.82×10-8,Ksp(PbCO3)=1.46×10-13;(2)铅与冷盐酸、冷硫酸几乎不起作用。请回答下列问题:
(1)写出步骤①“转化”的化学方程式_________________________,该反应能发生的原因是__________________________。
(2)步骤②“过滤1”后所得滤渣的主要成分为__________________________。
(3)步骤③“酸溶”,最适合选用的酸为_________________,为提高酸溶速率,可采取的措施是___________________(任意写出一条)。
(4)若步骤④“沉铅”后的滤液中c(Pb2+)=1.82×10-5mol·L-1,则此时c(SO42-)=_________ mol·L-1。
(5)从原子利用率的角度分析该流程的优点为_____________________。
(6)步骤⑥“合成”三盐的化学方程式为____________________________。若得到纯净干燥的三盐49.5t,假设铅泥中的铅元素有80%转化为三盐,则铅泥中铅元素的质量分数为_____%(结果保留一位小数)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一种钌(Ru)基配合物光敏染料敏化太阳能电池的工作原理及电池中发生的主要反应如图所示。下列说法错误的是
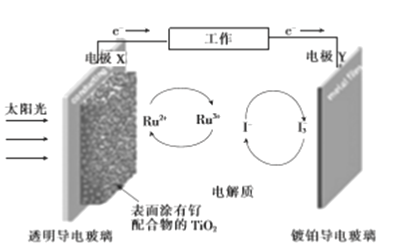
A. 电池工作时,光能转变为电能,X为电池的负极
B. 镀铂导电玻璃上发生氧化反应生成I-
C. 电解质溶液中发生反应:2Ru3++3I-![]() 2Ru2++I3-
2Ru2++I3-
D. 电池工作时,电解质溶液中I-和I3-的浓度基本不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用二氧化锰和足量的浓盐酸反应中制备氯气,如果有34.8 g二氧化锰被还原,那么被氧化的HC1的物质的量是多少?得到的氯气的物质的量是多少?
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学课外兴趣小组为探究NO气体易被空气氧化,并观察NO气体的实际颜色,同时为了防止气体扩散污染空气,对实验室制取NO气体的装置改装如下:
打开止水夹Ⅰ,Ⅱ,从漏斗处加入稀硝酸,直至液面浸没铜丝并与试管A胶塞处相平齐时,关闭止水夹Ⅰ,Ⅱ,用酒精灯微热试管A.
(1)加入稀硝酸与试管A胶塞处相平齐的目的是 .
(2)当用酒精灯微热试管A时,A中反应加快,请写出反应方程式 .
(3)当进入B试管的液体没及铜丝后,再微热B试管,此时B试管中能观察到的现象是 .
(4)为了防止气体污染空气,C烧杯中应装入溶液.
A.NaOH 溶液
B.CuSO4溶液
C.NaCl溶液
D.AgNO3溶液、
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com