
【题目】颠茄酸酯(J)是一种用于胃肠道平滑肌痉挛及溃疡病的辅助治疗药物,其合成路线如下:

回答下列问题:
(1)烃B中含氢的质量分数为7.69%,其相对分子质量小于118,且反应1为加成反应,则B的分子式为___________,X的化学名称为____________。
(2)C→D的反应类型为_____________。
(3)D的结构简式为___________________,G的结构简式为_______________________。
(4)反应3的化学方程式为__________________________________________。
(5)J的核磁共振氢谱有__________个峰。
(6)化合物I有多种同分异构体,同时满足下列条件的结构有_________种。
①能发生水解反应和银镜反应
②能与FeCl3溶液发生显色反应
③苯环上有四个取代基,且苯环上一卤代物只有一种
【答案】 C8H8 乙炔 水解(或取代)反应 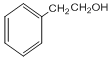
![]()
 +H2O 6 6
+H2O 6 6
【解析】本题考查有机物的推断和合成,从官能团的性质入手,(1)B为烃,仅含碳氢两种元素,碳的质量分数为(1-7.69%)=92.31%,因此有C和H原子个数比为92.31%/12:7.69%/1=8:8,因为A是苯环,因此B中碳原子数至少为6,且B的相对分子质量小于118,同时根据C的分子式,因此B的分子式为C8H8,因为反应1是加成反应,因此X的分子式为C2H2,即为乙炔;(2)对比C和D的分子式,D比C多了一个-OH,少了一个-Br,因此C→D发生水解反应或取代反应;(3)因为D能被氧气氧化,且E能与新制氢氧化铜悬浊液发生反应,说明D中-OH所连的碳原子上有2个氢原子,即-CH2OH,B的结构简式为:![]() ,B生成C发生加成反应,-Br加成到氢原子多的不饱和碳原子上,即C的结构简式为:
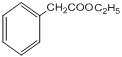
,B生成C发生加成反应,-Br加成到氢原子多的不饱和碳原子上,即C的结构简式为:![]() ,C生成D发生水解反应,即D的结构简式为:
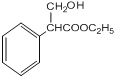
,C生成D发生水解反应,即D的结构简式为: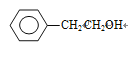 ,F和乙醇发生酯化反应生成G,即G的结构简式为:
,F和乙醇发生酯化反应生成G,即G的结构简式为: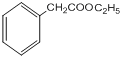 ;(4)H生成I发生加成反应或还原反应,醛基转化成醇羟基,因此I的结构简式为:
;(4)H生成I发生加成反应或还原反应,醛基转化成醇羟基,因此I的结构简式为: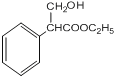 ,反应3发生消去反应,即反应方程式为
,反应3发生消去反应,即反应方程式为
![]()
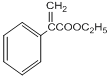 +H2O;(5)J中有6种不同的氢原子,因此核磁共振氢谱有6种不同的峰;(6)①发生水解和银镜反应,说明含有醛基或甲酸某酯,根据分子式,只能是甲酸某酯,②能与FeCl3发生显色反应,说明含有酚羟基,③有四个取代基,且苯环上只有一种卤代物,说明只有一种氢原子,因此符合条件的同分异构体是:
+H2O;(5)J中有6种不同的氢原子,因此核磁共振氢谱有6种不同的峰;(6)①发生水解和银镜反应,说明含有醛基或甲酸某酯,根据分子式,只能是甲酸某酯,②能与FeCl3发生显色反应,说明含有酚羟基,③有四个取代基,且苯环上只有一种卤代物,说明只有一种氢原子,因此符合条件的同分异构体是: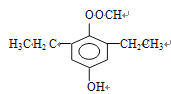 、
、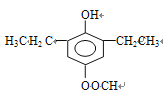 、
、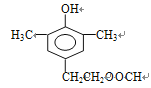 、
、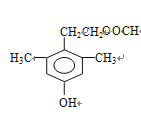 、
、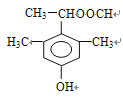 、
、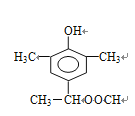 。
。


 寒假乐园北京教育出版社系列答案
寒假乐园北京教育出版社系列答案科目:高中化学 来源: 题型:
【题目】在一密闭容器中进行反应:2SO2(g)+O2(g) ![]() 2SO3(g)。已知反应过程中某一时刻SO2、O2、SO3的浓度分别为0.2 mol·L-1、0.1 mol·L-1、0.2 mol·L-1。当反应达到平衡时,可能存在的数据是( )
2SO3(g)。已知反应过程中某一时刻SO2、O2、SO3的浓度分别为0.2 mol·L-1、0.1 mol·L-1、0.2 mol·L-1。当反应达到平衡时,可能存在的数据是( )
A. SO2为0.4 mol·L-1,O2为0.2 mol·L-1 B. SO2为0.2 mol·L-1
C. SO2、SO3分别为0.15 mol·L-1 、 0.3 mol·L-1 D. SO3为0.4 mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知X是一种具有果香味的合成香料,下图为合成X的某种流程:

提示:①![]() 不能最终被氧化为-COOH;
不能最终被氧化为-COOH;
②D的产量可以用来衡量一个国家的石油化工水平。
请根据以上信息,回答下列问题:
(1)D与C分子中官能团的名称分别是____________,E的结构简式是____________。
(2)D→E的化学反应类型为____________反应。
(3)上述A、B、C、D、E、X六种物质中,互为同系物的是____________。
(4)反应C+E→X的化学方程式为___________________________________________。
(5)反应B→C的化学方程式为_______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】天津港“8.12”爆炸事故中,因爆炸冲击导致氰化钠泄漏,可以通过喷洒双氧水或硫代硫酸钠溶液来处理,以减轻环境污染。
资料:氰化钠化学式NaCN(C元素+2价,N元素-3价),白色结晶颗粒,剧毒,易溶于水,水溶液呈碱性,易水解生成氰化氢。
(1) NaCN水溶液呈碱性,其原因是 (用离子方程式解释)。
(2) NaCN用双氧水处理后,产生一种酸式盐和一种能使湿润红色石蕊试纸变蓝的气体,写出该反应的化学方程式 。
某化学兴趣小组实验室制备硫代硫酸钠(Na2S2O3),并检测用硫代硫酸钠溶液处理后的氰化钠废水能否达标排放。
【实验一】实验室通过下图装置制备Na2S2O3。

(3)a装置中盛Na2SO3固体的仪器名称是 ;b装置的作用是 。
(4)c装置中的产物有Na2S2O3和CO2等,d装置中的溶质有NaOH、Na2CO3,还可能有 。
(5)实验结束后,在e处最好连接盛 (选填“NaOH溶液”、“水”、“CCl4”中任一种)的注射器,再关闭K2打开K1,防止拆除装置时污染空气。
【实验二】测定用硫代硫酸钠溶液处理后的废水中氰化钠的含量。
已知:
① 废水中氰化钠的最高排放标准为0.50 mg/L。
② Ag++2CN- =" [" Ag (CN)2]-, Ag++I- = AgI↓,AgI呈黄色,且CN-优先与Ag+反应。
实验如下:
取25.00 mL处理后的氰化钠废水于锥形瓶中,并滴加几滴KI溶液作指示剂,用1.000 ×10-4mol/L的标准AgNO3溶液滴定,消耗AgNO3溶液的体积为2.50 mL。
(6) 滴定终点的判断方法是 。
(7) 处理后的废水中氰化钠的含量为 mg/L。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用如图所示装置进行下列实验,能得出相应实验结论的是

选项 | ① | ② | ③ | 实验结论 |
A | 浓氨水 | NaOH | 酚酞试液 | 碱性:NaOH>NH3·H2O |
B | 浓硫酸 | 蔗糖 | 品红溶液 | 浓硫酸具有脱水性、氧化性 |
C | 稀盐酸 | Na2SO3 | Ba(NO3)2溶液 | SO2与可溶性钡盐反应均可生成白色沉淀 |
D | 浓硝酸 | Na2CO3 | Na2SiO3溶液 | 酸性:硝酸>碳酸>硅酸 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在标准状况下,将224 L氯化氢气体溶于635 mL的水(密度为1.00 g/cm3)中,所得盐酸的密度为1.18 g/cm3。求:
(1)该盐酸的溶质质量分数是多少?
(2)取这种盐酸10.0 mL,稀释到1.00 L,所得的稀盐酸的物质的量浓度多少?
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表列出了前20号元素中的某些元素性质的有关数据

下列有关叙述正确的是
A. 以上10种元素的原子中,失去核外第一个电子所需能量最少的是⑧
B. 由⑤、⑥、⑦三种元素中的某两种元素形成的化合物中,每个原子都满足最外层为8电子稳定结构的物质可能是PCl5和CCl4
C. 某元素R的原子半径为1.02×10-10 m,该元素在周期表中位于第三周期第ⅤA族
D. 若物质Na2R3是一种含有非极性共价键的离子化合物,则其化合物的电子式![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】日常生活中的手电筒干电池通常是锌锰电池,其构造示意图如右。据图回答:

(1)作正极的是__________。
(2)负极的电极反应是_____________________________
(3)许多国家对废电池进行回收,其主要原因是_______________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com