
【题目】天津港“8.12”爆炸事故中,因爆炸冲击导致氰化钠泄漏,可以通过喷洒双氧水或硫代硫酸钠溶液来处理,以减轻环境污染。
资料:氰化钠化学式NaCN(C元素+2价,N元素-3价),白色结晶颗粒,剧毒,易溶于水,水溶液呈碱性,易水解生成氰化氢。
(1) NaCN水溶液呈碱性,其原因是 (用离子方程式解释)。
(2) NaCN用双氧水处理后,产生一种酸式盐和一种能使湿润红色石蕊试纸变蓝的气体,写出该反应的化学方程式 。
某化学兴趣小组实验室制备硫代硫酸钠(Na2S2O3),并检测用硫代硫酸钠溶液处理后的氰化钠废水能否达标排放。
【实验一】实验室通过下图装置制备Na2S2O3。

(3)a装置中盛Na2SO3固体的仪器名称是 ;b装置的作用是 。
(4)c装置中的产物有Na2S2O3和CO2等,d装置中的溶质有NaOH、Na2CO3,还可能有 。
(5)实验结束后,在e处最好连接盛 (选填“NaOH溶液”、“水”、“CCl4”中任一种)的注射器,再关闭K2打开K1,防止拆除装置时污染空气。
【实验二】测定用硫代硫酸钠溶液处理后的废水中氰化钠的含量。
已知:
① 废水中氰化钠的最高排放标准为0.50 mg/L。
② Ag++2CN- =" [" Ag (CN)2]-, Ag++I- = AgI↓,AgI呈黄色,且CN-优先与Ag+反应。
实验如下:
取25.00 mL处理后的氰化钠废水于锥形瓶中,并滴加几滴KI溶液作指示剂,用1.000 ×10-4mol/L的标准AgNO3溶液滴定,消耗AgNO3溶液的体积为2.50 mL。
(6) 滴定终点的判断方法是 。
(7) 处理后的废水中氰化钠的含量为 mg/L。
【答案】(1)CN-+H2OHCN+OH-(2)NaCN+H2O2+H2O=NaHCO3+NH3↑
(3)圆底烧瓶;安全瓶,防止倒吸(4)Na2SO3(5)NaOH溶液
(6)滴入最后一滴硝酸银溶液,出现淡黄色沉淀(7)0.98
【解析】试题分析:(1)NaCN为强碱弱酸盐,水解呈碱性,反应的离子方程式为:CN-+H2OHCN+OH-;(2)常温下,氰化钠能与过氧化氢溶液反应,生成能使湿润的红色石蕊试纸变蓝色的气体,该气体为氨气,生成的酸式盐为碳酸氢钠,反应方程式为:NaCN+H2O2+H2O=NaHCO3+NH3↑;(3)由仪器结构特征,可知盛装Na2SO3固体的仪器为圆底烧瓶;b装置为安全瓶,防止倒吸;(4)d装置吸收二氧化硫,d中溶质有NaOH、Na2CO3,碱过量,还有亚硫酸钠生成;(5)验结束后,装置b中还有残留的二氧化硫,为防止污染空气,应用氢氧化钠溶液吸收;(6)Ag+与CN-反应生成[Ag(CN)2]-,当CN-反应结束时,滴入最后一滴硝酸银溶液,Ag+与I-生成AgI黄色沉淀,说明反应到达滴定终点;(7)消耗AgNO3的物质的量为2.5×10-3L×0.0001mol/L=2.50×10-7mol,根据方程式Ag++2CN-=[Ag(CN)2]-,处理的废水中氰化钠的质量为2.50×10-7mol×2×49g/mol=2.45×10-5g,废水中氰化钠的含量为![]() =0.98mg/L。
=0.98mg/L。


科目:高中化学 来源: 题型:
【题目】下列涉及有机物性质或应用的说法正确的是( )
A. 利用可降解的“玉米塑料”替代一次性饭盒,可减少“白色污染”
B. 乙烯、聚氯乙烯都能使溴水褪色
C. 保鲜膜、一次性食品袋的主要成分是聚氯乙烯
D. 人造纤维、合成纤维和光导纤维都是有机高分子化合物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】可以证明乙酸是弱酸的事实是( )
A. 乙酸和水能任意比例混溶
B. 1molL﹣1的醋酸水溶液能使紫色石蕊试液变红色
C. 醋酸能与碳酸钠溶液反应生成CO2气体
D. 醋酸溶液中存在醋酸分子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在0.4 L由NaCl、MgCl2、CaCl2组成的混合液中,部分离子浓度大小如图所示,回答下列问题。

(1)该混合液中,NaCl的物质的量为______mol,含溶质MgCl2的质量为________g。
(2)该混合液中CaCl2的物质的量为________mol,将该混合液加水稀释至体积为1 L,稀释后溶液中Ca2+的物质的量浓度为________mol·L1。
(3)向该稀释后的溶液中加入足量硝酸酸化的硝酸银溶液,可得到沉淀________mol。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲醇是一种可再生能源,具有开发和应用的广阔前景,工业上一般可采用如下反应来合成甲醇:
CO(g)+2H2(g) ![]() CH3OH(g),现在实验室模拟该反应并进行分析。
CH3OH(g),现在实验室模拟该反应并进行分析。
(1)下列各项中,不能够说明该反应已达到平衡的是__________(填序号)。
a. 恒温、恒容条件下,容器内的压强不发生变化
b. 一定条件下,CH3OH分解的速率和CH3OH生成的速率相等
c. 一定条件下,CO、H2和CH3OH的浓度保持不变
d. 一定条件下,单位时间内消耗2 mol CO,同时生成1 mol CH3OH
(2)如图是该反应在不同温度下CO的转化率随时间变化的曲线。

① 该反应的焓变ΔH____________0(填“>”、“<”或“=”)。
② T1和T2温度下的平衡常数大小关系是K1____________K2(填“>”、“<”或“=”)。
③ 若容器容积不变,下列措施可增加甲醇产率的是______________。
a. 升高温度
b. 将CH3OH(g)从体系中分离
c. 使用合适的催化剂
d. 充入He,使体系总压强增大
(3)2009年10月,中国科学院长春应用化学研究所在甲醇燃料电池技术方面获得新突破,甲醇燃料电池的工作原理如图所示。

①请写出c口通入的物质发生的相应电极反应式_____________________________。
②工作一段时间后,当0.2 mol甲醇完全反应生成CO2 时,有___________NA个电子转移。

(4)以上述电池做电源,用上图所示装置,在实验室中模拟铝制品表面“钝化”处理的过程中,发现Al电极附近逐渐变浑浊并有气泡逸出,原因是(用相关的电极反应式和离子方程式表示):
_________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】颠茄酸酯(J)是一种用于胃肠道平滑肌痉挛及溃疡病的辅助治疗药物,其合成路线如下:

回答下列问题:
(1)烃B中含氢的质量分数为7.69%,其相对分子质量小于118,且反应1为加成反应,则B的分子式为___________,X的化学名称为____________。
(2)C→D的反应类型为_____________。
(3)D的结构简式为___________________,G的结构简式为_______________________。
(4)反应3的化学方程式为__________________________________________。
(5)J的核磁共振氢谱有__________个峰。
(6)化合物I有多种同分异构体,同时满足下列条件的结构有_________种。
①能发生水解反应和银镜反应
②能与FeCl3溶液发生显色反应
③苯环上有四个取代基,且苯环上一卤代物只有一种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(12分) 某实验小组用下图装置进行乙醇催化氧化的实验。Z.X.X.K]
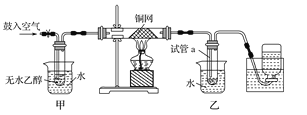
(1)实验过程中铜网出现红色和黑色交替的现象,请写出相应的化学反应方程式 。
在不断鼓入空气的情况下,熄灭酒精灯,反应仍能继续进行,说明该乙醇氧化反应是 反应(放热或吸热)。
(2)甲和乙两个水浴作用不相同。甲的作用是 ;
乙的作用是 。
(3)反应进行一段时间后,干燥试管a中能收集到不同的物质,它们是 ,
集气瓶中收集到的气体的主要成分是 。
(4)若试管a中收集到的液体用紫色石蕊试纸检验,试纸显红色,说明液体中还含有 。要除去该物质,可先在混合液中加入 (填写字母)。然后,再通过 (填实验操作名称)即可除去。
a.氯化钠溶液 b.苯 c.碳酸氢钠溶液 d.四氯化碳
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学与生活息息相关。下列做法正确的是( )
A. 往食品中添加苏丹红
B. 用聚氯乙烯塑料薄膜包装食品
C. 食用含铁丰富的食物可以补充铁
D. 用碳酸钡作医疗上的“钡餐”
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现将AlCl3、MgCl2、MgSO4、Al2(SO4)3四种物质溶于水,形成的混合溶液中c(Al3+)=0.1mol·L-1、c(Mg2+)=0.25mol·L-1、c(Cl-)=0.2mol·L-1,则该溶液中c(SO42-)为
A. 0.15mol·L-1
B. 0.20mol·L-1
C. 0.25mol·L-1
D. 0.30mol·L-1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com