
【题目】甲醇是一种可再生能源,具有开发和应用的广阔前景,工业上一般可采用如下反应来合成甲醇:
CO(g)+2H2(g) ![]() CH3OH(g),现在实验室模拟该反应并进行分析。
CH3OH(g),现在实验室模拟该反应并进行分析。
(1)下列各项中,不能够说明该反应已达到平衡的是__________(填序号)。
a. 恒温、恒容条件下,容器内的压强不发生变化
b. 一定条件下,CH3OH分解的速率和CH3OH生成的速率相等
c. 一定条件下,CO、H2和CH3OH的浓度保持不变
d. 一定条件下,单位时间内消耗2 mol CO,同时生成1 mol CH3OH
(2)如图是该反应在不同温度下CO的转化率随时间变化的曲线。

① 该反应的焓变ΔH____________0(填“>”、“<”或“=”)。
② T1和T2温度下的平衡常数大小关系是K1____________K2(填“>”、“<”或“=”)。
③ 若容器容积不变,下列措施可增加甲醇产率的是______________。
a. 升高温度
b. 将CH3OH(g)从体系中分离
c. 使用合适的催化剂
d. 充入He,使体系总压强增大
(3)2009年10月,中国科学院长春应用化学研究所在甲醇燃料电池技术方面获得新突破,甲醇燃料电池的工作原理如图所示。

①请写出c口通入的物质发生的相应电极反应式_____________________________。
②工作一段时间后,当0.2 mol甲醇完全反应生成CO2 时,有___________NA个电子转移。

(4)以上述电池做电源,用上图所示装置,在实验室中模拟铝制品表面“钝化”处理的过程中,发现Al电极附近逐渐变浑浊并有气泡逸出,原因是(用相关的电极反应式和离子方程式表示):
_________________________________________________。
【答案】 d < > b O2+4e-+4H+=2H2O 1.2 Al-3e-=Al3+。Al3++3HCO3-=Al(OH)3↓+3CO2↑
【解析】(1)a.由方程式可以看出,反应前后气体的物质的量不相等,只有达到平衡状态,容器压强不发生变化,能判断反应达到平衡状态,故a不选;b.一定条件下,CH3OH分解的速率和CH3OH生成的速率相等,即正逆反应速率相等,所以能判断反应达到平衡状态,故b不选;c、一定条件下,CO、H2和CH3OH的浓度保持不变是平衡的标志,故c不选;d、一定条件下,单位时间内消耗2molCO,同时生成1mol CH3OH,只能表明正反应速率,不能表示正逆反应速率相等,故d选;故选d;
(2)①反应CO(g)+2H2(g)CH3OH(g)中,反应向右进行,一氧化碳的转化率增大,温度升高,化学平衡向着吸热方向进行,根据图中的信息可以知道:T2>T1,所以该反应是放热反应,ΔH<0,故答案为:<;
②对于放热反应,温度越高,化学平衡常数越小,T2>T1,反之越大,所以K1>K2,故答案为:>;
③a、若容器容积不变,升高温度,反应CO(g)+2H2(g)CH3OH(g)平衡逆向移动,甲醇产率降低,故a错误;b、将CH3OH(g)从体系中分离,反应CO(g)+2H2(g)CH3OH(g)平衡正向移动,甲醇产率增大,故b正确;c、使用合适的催化剂不会引起化学平衡的移动,甲醇的转化率不变,故c错误;d、若容器容积不变,充入He,使体系总压强增大,单质各组分的浓度不变,化学平衡不移动,甲醇的转化率不变,故d错误;故选b;
(3)①在甲醇燃料电池中,燃料甲醇作负极,氧气作正极,电解质中的阳离子移向正极,所以b口通入的物质为甲醇,c口通入的物质为氧气,该电池正极是氧气发生得电子的还原反应,电极反应式为:O2+4e-+4H+=2H2O;故答案为:O2+4e-+4H+=2H2O;
②当0.2mol甲醇完全反应生成CO2时,根据总反应:2CH3OH+3O2=2CO2+4H2O,消耗氧气0.3mol,转移电子1.2mol;故答案为:1.2;
(4)Al电极为阳极,铝放电,电极反应式为Al-3e-=Al3+,生成的铝离子与溶液中的碳酸氢根离子发生双水解反应放出二氧化碳,反应的离子方程式为Al3++3HCO3-=Al(OH)3↓+3CO2↑,故答案为:Al-3e-=Al3+;Al3++3HCO3-=Al(OH)3↓+3CO2↑。


 世纪百通主体课堂小学课时同步达标系列答案
世纪百通主体课堂小学课时同步达标系列答案 世纪百通优练测系列答案
世纪百通优练测系列答案 百分学生作业本题练王系列答案
百分学生作业本题练王系列答案科目:高中化学 来源: 题型:
【题目】2SO2+O22SO3△H<0是工业上接触法制硫酸的重要反应.下列关于该反应的说法不正确的是( )
A. 增加O2的浓度提高SO2的转化率
B. 降低温度能加快反应的速率
C. 利用该反应放出的热量对SO2、O2预热
D. 即使增大压强也不能使SO2全部转化为SO3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室欲用NaOH固体配制1.0 mol·L1的NaOH溶液240 mL:
(1)配制溶液时,一般可以分为以下几个步骤:
①称量 ②计算 ③溶解 ④倒转摇匀 ⑤转移 ⑥洗涤 ⑦定容 ⑧冷却
其正确的操作顺序为________________。本实验必须用到的仪器有天平、药匙、玻璃棒、烧杯、胶头滴管、还有________。
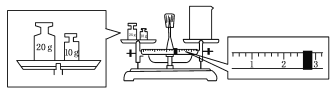
(2)某同学欲称量一定量的NaOH固体,他先用托盘天平称量烧杯的质量,天平平衡后的状态如图。烧杯的实际质量为____________ g,要完成本实验该同学应称出____________ g NaOH。
(3)使用容量瓶前必须进行的一步操作是________。
(4)在配制过程中,其他操作都是正确的,下列操作会引起浓度偏高的是________。
①没有洗涤烧杯和玻璃棒
②转移溶液时不慎有少量洒到容量瓶外面
③容量瓶不干燥,含有少量蒸馏水
④定容时俯视刻度线
⑤未冷却到室温就将溶液转移到容量瓶并定容
⑥定容后塞上瓶塞反复摇匀,静置后,液面低于刻度线,再加水至刻度线
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将纯锌片和纯铜片按图示方式插入同浓度的稀硫酸中一段时间,以下叙述正确的是

A. 两烧杯中铜片表面均无气泡产生
B. 甲中铜片是正极,乙中铜片是负极
C. 两烧杯中溶液的pH均增大
D. 生成氢气的速率甲比乙慢
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】天津港“8.12”爆炸事故中,因爆炸冲击导致氰化钠泄漏,可以通过喷洒双氧水或硫代硫酸钠溶液来处理,以减轻环境污染。
资料:氰化钠化学式NaCN(C元素+2价,N元素-3价),白色结晶颗粒,剧毒,易溶于水,水溶液呈碱性,易水解生成氰化氢。
(1) NaCN水溶液呈碱性,其原因是 (用离子方程式解释)。
(2) NaCN用双氧水处理后,产生一种酸式盐和一种能使湿润红色石蕊试纸变蓝的气体,写出该反应的化学方程式 。
某化学兴趣小组实验室制备硫代硫酸钠(Na2S2O3),并检测用硫代硫酸钠溶液处理后的氰化钠废水能否达标排放。
【实验一】实验室通过下图装置制备Na2S2O3。

(3)a装置中盛Na2SO3固体的仪器名称是 ;b装置的作用是 。
(4)c装置中的产物有Na2S2O3和CO2等,d装置中的溶质有NaOH、Na2CO3,还可能有 。
(5)实验结束后,在e处最好连接盛 (选填“NaOH溶液”、“水”、“CCl4”中任一种)的注射器,再关闭K2打开K1,防止拆除装置时污染空气。
【实验二】测定用硫代硫酸钠溶液处理后的废水中氰化钠的含量。
已知:
① 废水中氰化钠的最高排放标准为0.50 mg/L。
② Ag++2CN- =" [" Ag (CN)2]-, Ag++I- = AgI↓,AgI呈黄色,且CN-优先与Ag+反应。
实验如下:
取25.00 mL处理后的氰化钠废水于锥形瓶中,并滴加几滴KI溶液作指示剂,用1.000 ×10-4mol/L的标准AgNO3溶液滴定,消耗AgNO3溶液的体积为2.50 mL。
(6) 滴定终点的判断方法是 。
(7) 处理后的废水中氰化钠的含量为 mg/L。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某一反应物的物质的量是2.0mol,经过4min后,它的物质的量变成了1.68mol,则在这4min内它的反应速率是( )
A. 无法确定 B. 0.08 molL﹣1min﹣1
C. 0.32 molL﹣1min﹣1 D. 0.06 molL﹣1min﹣1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于胶体的说法正确的是
A. 直径介于1~100纳米之间的微粒称为胶体
B. 当光束通过胶体时,看到的“光柱”是由于光被胶体粒子散射而形成的
C. 胶体的分散质不能透过滤纸的孔隙
D. 溶液是电中性的,胶体是带电的
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫单质及其化合物在化工生产、污水处理等领域应用广泛。
(1)煤制得的化工原料气中含有羰基硫(O=C=S),该物质可转化为H2S,主要反应如下:
ⅰ.水解反应:COS(g)+H2O(g)![]() H2S(g)+CO2(g) △H1
H2S(g)+CO2(g) △H1
ⅱ.氢解反应:COS(g)+H2(g)![]() H2S(g)+CO(g) △H2
H2S(g)+CO(g) △H2
已知反应中相关的化学键键能数据如下表:
化学键 | H-H | C=O(COS) | C=S | H-S |
|
E/kJ·mol-1 | 436 | 745 | 580 | 339 | 1076 |
①恒温恒压下,密闭容器中发生反应i。下列事实能说明反应i达到平衡状态的是_______。 (填标号)
a.容器的体积不再改变
b.化学平衡常数不再改变
c.混合气体的密度不再改变
d.形成1molH—O键,同时形成1molH—S键
②一定条件下,密闭容器中发生反应i,其中COS(g)的平衡转化率(![]() )与温度(T)的关系如图所示。则A、B、C三点对应的状态中,v(COS)=v(H2S)的是____________。(填标号)
)与温度(T)的关系如图所示。则A、B、C三点对应的状态中,v(COS)=v(H2S)的是____________。(填标号)

③反应ii的正、逆反应的平衡常数(K)与温度(T)的关系如图所示,其中表示逆反应的平衡常数(K逆)的是__________(填“A”或“B”)。T1℃时,向容积为10 L的恒容密闭容器中充入2 mol COS(g)和1 mol H2(g),发生反应ii,COS的平衡转化率为_____________。
(2)过二硫酸是一种强氧化性酸,其结构式为
①在Ag+催化作用下,S2O82-能与Mn2+在水溶液中发生反应生成SO42-和MnO4-,该反应的离子方程式为_____________________________。
②工业上可用惰性电极电解硫酸和硫酸铵混合溶液的方法制备过二硫酸铵。总反应的离子方程式为________________________________。
(3)NaHS可用于污水处理的沉淀剂。已知:25℃时,反应Hg2+(aq)+HS-(aq) ![]() HgS(s)+H+(aq)的平衡常数K=1.75×1038,H2S的电离平衡常数Ka1=1.0×10-7,Ka2=7.0×10-15。
HgS(s)+H+(aq)的平衡常数K=1.75×1038,H2S的电离平衡常数Ka1=1.0×10-7,Ka2=7.0×10-15。
①NaHS的电子式为____________________。
②Ksp(HgS)=_____________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com