
| A、元素A的氧化物常温下一般均为无色无味气体 |
| B、元素C、D、E的最高价氧化物对应的水化物两两之间能发生反应 |
| C、原子半径:C>D>B |
| D、元素B的气态氢化物的沸点比元素E气态氢化物的沸点高 |


 新思维假期作业暑假吉林大学出版社系列答案
新思维假期作业暑假吉林大学出版社系列答案 蓝天教育暑假优化学习系列答案
蓝天教育暑假优化学习系列答案科目:高中化学 来源: 题型:
| A、Q1>Q2>Q3 |
| B、Q1<Q3<Q2 |
| C、Q1<Q2<Q3 |
| D、Q1>Q3>Q2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、吸热反应一定不能自发进行 |
| B、△H大于零的反应是放热反应 |
| C、已知S(单斜,s)=S(正交,s)△H<0,则单斜硫比正交硫稳定 |
| D、应用盖斯定律,可计算某些难以直接测量的反应的反应热 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、铊是易导电的银白色金属 |
| B、能生成+3价离子 |
| C、氢氧化铊是两性氢氧化物 |
| D、Tl3+的氧化能力比Al3+强 |
查看答案和解析>>
科目:高中化学 来源: 题型:
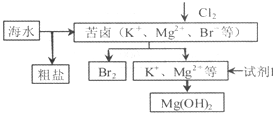 海洋约占地球表面积的71%,对其进行开发利用的部分流程如图所示.下列说法不正确的是( )
海洋约占地球表面积的71%,对其进行开发利用的部分流程如图所示.下列说法不正确的是( )| A、可用BaCl2溶液除去粗盐中的SO42- |
| B、从苦卤中提取Br2的离子方程式为2Br-+Cl2═2C1-十Br2 |
| C、试剂1可以选用Ca(OH)2 |
| D、工业上,电解熔融Mg(OH)2冶炼金属镁 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com