
����Ŀ��ԭ��������С�������е����ֶ�����Ԫ��X��Y��Z��W������X��Z��W����Ԫ�ؿ���ɹ��ۻ�����XH3��H2Z��HW��Y����Ԫ�ؿ��γ����ӻ�����Y2O��Y2O2��
��1��Y2Z�ĵ���ʽ�� ________
��2��ʵ���ҿ�����ͼ��ʾװ���Ʊ����ռ�XH3(ȱ���ռ�װ�ã��г̶ֹ�װ����ȥ)��

��ͼ�з�����Ӧѡ������_____��ƿ�ռ�XH3���A��B������
��ʵ�����Ʒ��д��Թ��е��Լ�һ��ѡ��(��д��ѧʽ)_________________���ձ�����Һ����ɫ��Ϊ��ɫ����ԭ����(�õ��뷽��ʽ��ʾ)��___________________________________
��XH3�ǹ�ҵ�����������������Ҫ����ԭ�ϣ��Ʊ������и����ʷ����Ļ�ѧ��Ӧ����ʽΪ__________________________��
��3������W2��ȼ�տ��������ֲ������һ�ֲ���ף������и�ԭ������㲻ȫ��8���ӽṹ���Ļ�ѧʽ��_________�� XH3��HW���ֻ������ܷ�Ӧ�������ӻ������ң�n mol����n mol����һ�������·�Ӧ������4n mol HW����һ������û������������ܶ�����ͬ״���������ܶȵ�174�����仯ѧʽ��_________��
���𰸡� ![]() A NH4Cl��Ca(OH)2 NH3H2O
A NH4Cl��Ca(OH)2 NH3H2O![]() NH4++OH 4NH3��5O2
NH4++OH 4NH3��5O2 ![]() 4NO��6H2O PCl5 P3N3Cl6
4NO��6H2O PCl5 P3N3Cl6
�����������������ԭ��������С�������е����ֶ�����Ԫ��X��Y��Z��W��Y����Ԫ�ؿ��γ����ӻ�����Y2O��Y2O2����YΪNa������X��Z��W����Ԫ�ؿ���ɹ��ۻ�����XH3��H2Z��HW����XΪN��ZΪS��WΪCl��
��1��Na2S�ĵ���ʽ��![]() ��
��
��2�����ռ�NH3�������ſ���������ͼ�з�����Ӧѡ������A��ƿ�ռ�NH3��
��ʵ�����Ʒ��д��Թ��е��Լ�һ��ѡ��NH4Cl��Ca(OH)2���ձ�����Һ����ɫ��Ϊ��ɫ����ԭ���ǰ�����ˮ��Ӧ���ɵ�һˮ�ϰ����������뷽��ʽΪNH3H2O![]() NH4++OH��
NH4++OH��
��NH3�ǹ�ҵ�����������������Ҫ����ԭ�ϣ��Ʊ��������������ʷ�������������ѧ��Ӧ����ʽΪ4NH3��5O2 ![]() 4NO��6H2O��
4NO��6H2O��
��3������Cl2��ȼ�տ��������ֲ������һ�ֲ���ף������и�ԭ������㲻ȫ��8���ӽṹ�����Ϊ���Ȼ��ף��仯ѧʽ��PCl5�� NH3��HCl���ֻ������ܷ�Ӧ�������ӻ������Ȼ����n mol PCl5��n molNH4Cl��һ�������·�Ӧ������4n mol HCl����һ������û������������ܶ�����ͬ״���������ܶȵ�174������û��������Է�������Ϊ348���������غ㶨�ɿ�֪���仯ѧʽ��P3N3Cl6��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij�¶��£���ӦSO2��g��+ ![]() O2��g��SO3��g����ƽ�ⳣ��K1=50����ͬһ�¶��£���Ӧ2SO3��g��2SO2��g��+O2��g����ƽ�ⳣ��K2��ֵΪ�� ��
O2��g��SO3��g����ƽ�ⳣ��K1=50����ͬһ�¶��£���Ӧ2SO3��g��2SO2��g��+O2��g����ƽ�ⳣ��K2��ֵΪ�� ��
A.2500
B.100
C.4��10��4
D.2��10��2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��SO2��NO2���γ����꣬ijͬѧ������Ϊ�������������ʵ�飺
��ʵ��һ������ֻ����ƿ�ռ��������������������壬Ȼ���䵹����ˮ���У��ֱ���ͨ������O2��Cl2����ͼA��B��C��ʾ��һ��ʱ���A��Bװ�õļ���ƿ�г�����Һ������ƿ��Һ�岻��ɢ����Cװ�õļ���ƿ�л�������ʣ��(�ɿ���Һ�����ɢ) ��
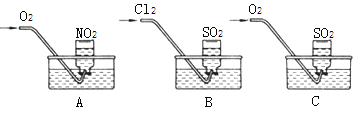
��1��д��װ��A���ܷ�Ӧ�Ļ�ѧ����ʽ________________�������ʵ�������£�����Ħ�����Ϊa L/mol����װ��A�ļ���ƿ��������Һ���ʵ����ʵ���Ũ��Ϊ______��
��2��д��Bװ�õ���Һ��������ƿʱ���йط�Ӧ�����ӷ���ʽ__________________��
��3��ʵ��ǰ��Cװ�õ�ˮ����μӼ�����ɫʯ����Һ��ͨ�������ɹ۲쵽��ʵ����������Һ��ɫ���д����Ӧ���ܻ�ѧ����ʽ___________________________��
��ʵ�����������ͼB��ԭ���������ͼװ�òⶨij���Ṥ���ŷ�β���ж�������ĺ�����ͼ����������������ȷ����ͨ����β���������β��ͨ��һ������ĵ�ˮ����ͨ��ʵ��ⶨSO2�ĺ�������ϴ��ƿD����Һ��ɫ�պ���ʧʱ�������رջ���K��
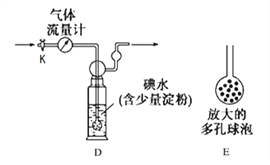
��4��D�е���ĩ������һ���������E����������________���������ʵ���ȷ�ȡ�
��5�����������иպ�ͨ��2Lβ��ʱ��D����Һ��ɫ�պ���ʧ�������رջ���K������D��ǡ�õõ�100mL��Һ��������Һȫ��ת������ƿ�У��������BaCl2��Һ�����ˡ�ϴ�ӡ�����õ�4.66g ��ɫ������ͨ�������֪������β���ж�������ĺ���Ϊ________g/L����ϴ��ƿD����Һ��ɫ��ʧ��û�м�ʱ�رջ���K����õ�SO2����________(�ƫ�ߡ�����ƫ�͡�����Ӱ�족)��
��6������⻯��H2S����ȼ��Ҳ���ܲ�����Ⱦ��SO2���Լ��㣺��״���£�0.35molH2S��11.2LO2�ڵ�ȼ�����³�ַ�Ӧ��������������������Ϊ________g��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��Ϊ�˴Ӻ�����ȡҺ����ȡ�⣬ijͬѧ���������ʵ�鷽����( )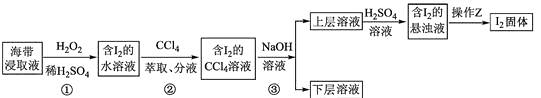
����˵����ȷ����
A.���з�Ӧ�����ӷ���ʽ��2I + H2O2 = I2 + 2OH
B.���з�Һʱ��I2��CCl4��Һ�ӷ�Һ©���Ͽڵ���
C.���еõ����ϲ���Һ�к���I
D.����Z�������Ǽ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����й����Ҵ��������˵���У���ȷ���ǣ� ��
A.�Ҵ���������Ӷ��ܺͽ����Ʒ�Ӧ
B.����������ˮ�����������Ҵ�
C.�Ҵ����������ʹ��ɫʯ����Һ���
D.�Ҵ������ụΪͬ���칹��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ӦN2��g��+3H2��g��2NH3��g�����ܱ������н��У����й��ڸ÷�Ӧ��˵����ȷ���ǣ� ��
A.�����ܼ�����Ӧ����
B.����ѹǿ�ܼӿ췴Ӧ����
C.��Ӧ�ﵽƽ��ʱ��v������Ӧ��=v���淴Ӧ��=0
D.��Ӧ�ﵽƽ��ʱ��N2ת����Ϊ100%
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ��ʾװ���У��ס��ҡ��������ձ����ηֱ�ʢ��100g 5.00%��NaOH��Һ��������CuSO4��Һ��100g 10.00%��K2SO4��Һ���缫��Ϊʯī�缫�� 
��1����ͨ��Դ������һ��ʱ���ñ���K2SO4Ũ��Ϊ10.47%������c�缫�������ӣ��ݴ˻ش����⣺
�ٵ�Դ��N��Ϊ����
�ڵ缫b�Ϸ����ĵ缫��ӦΪ��
����ʽ����缫b�����ɵ������ڱ�״���µ������
�ܵ缫c�������仯��g��
�ݵ��ǰ�����Һ���ᡢ���Դ�С�Ƿ����仯��������ԭ��
����Һ��
����Һ��
����Һ��
��2�������������ͭȫ����������ʱ����ܷ�������У�Ϊʲô�� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��պ��Ũ��ˮ�IJ�������պ��Ũ����IJ������ӽ�ʱ������������ȷ����
A.��������B.��������C.��������ɫ����D.����������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������ܱ������н��еĹ�ҵ�ϳɰ��ķ�Ӧ��N2+3H22NH3 �� ����˵��������� �� ��
A.ʹ�ú��ʵĴ�����������Ӧ����
B.�����¶ȿ�������Ӧ����
C.����ѹǿ��Ӱ�췴Ӧ����
D.����N2Ũ�ȿ�������Ӧ����
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com