
某研究性学习小组用下列装置(铁架台等支撑仪器略)探究氧化铁与乙醇的反应,并检验反应产物。
(1)为快速得到乙醇气体,可采取的方法是 ;
若实验时小试管中的溶液已经开始发生倒吸,你采取的措施是 (填写编号);
a.取下小试管 b.移去酒精灯 c.将导管从乳胶管中取下 d.以上都可以
(2)盛Cu(OH)2悬浊液的试管中出现的现象为 。
(3)如图实验,观察到红色的Fe2O3全部变为黑色固体(M),充分反应后停止加热。为了检验M的组成,进行下列实验。
①M能被磁铁吸引;加入足量稀硫酸,振荡,固体全部溶解,未观察到有气体生成;
② 经检验溶液中有Fe2+和Fe3+,检验该溶液中的Fe2+的方法是 ;
关于M中铁元素价态的判断正确的是 (填写编号)。
a.一定有+3价和+2价铁,无0价铁
b.一定有+3价、+2价和0价铁
c.一定有+3价和0价铁,无+2价铁
d.一定有+3和+2价铁,可能有0价铁
(4)若M的成份可表达为FeXOY,用CO还原法定量测定其化学组成。称取a g M样品进行定量测定,实验装置和步骤如下:
①组装仪器;②点燃酒精灯;③加入试剂; ④打开分液漏斗活塞;⑤检查气密性;⑥停止加热;⑦关闭分液漏斗活塞;⑧……。正确的操作顺序是 (填写编号)
a.①⑤④③②⑥⑦⑧ b.①③⑤④②⑦⑥⑧ c.①⑤③④②⑥⑦⑧ d.①③⑤②④⑥⑦⑧
(5)若实验中每步反应都进行完全,反应后M样品质量减小b g,则FexOy中 = 。
= 。
(1)在烧杯中加入热水(对烧杯加热) c;
(2)试管中出现砖红色沉淀。
(3)在Fe2+和Fe3+溶液中检验Fe2+的方法是:取少量溶液于试管中,加入酸性高锰酸钾溶液,若紫红色褪去,则说明有Fe2+(或向溶液中加入K3[Fe(CN)6],若产生蓝色沉淀,则说明有Fe2+)。d;
(4)c;
(5)
解析试题分析:(1) 快速得到乙醇气体,可采取的方法是在烧杯中加入80℃的热水给烧瓶加热(或烧杯热水并加热),若实验时小试管中的溶液已经开始发生倒吸,应采取的措施是将导管从乳胶管中取下;(2)盛Cu(OH)2悬浊液的试管中出现砖红色沉淀。
(3)在取少量溶液于试管中,加入酸性高锰酸钾溶液,若紫红色褪去,则说明有Fe2+(或向溶液中加入K3[Fe(CN)6],若产生蓝色沉淀,则说明有Fe2+)。M能被磁铁吸引,说明可能是单质Fe或Fe3O4,加入足量稀硫酸,振荡,固体全部溶解,未观察到有气体生成,不可能全部为Fe,证明一定含有Fe3O4,稀硫酸溶解得到Fe2+和Fe3+溶液,若有少量的Fe单质,能与Fe3+反应生成Fe2+,故选d;(5)M样品质量ag与CO减小b g,减小的是O的质量,余下的是Fe的质量,则FexOy中 =
= =
= 。
。
考点:化学实验的设计与评价。


科目:高中化学 来源: 题型:填空题
以下是某课题组设计的合成聚酯类高分子材料的路线: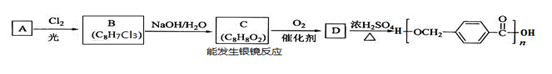
已知:同一碳原子上连两个羟基时结构不稳定,易脱水生成醛或酮
请根据以上信息回答下列问题:
(1)烃A的结构简式为 ,A的化学名称为__________。
(2) 由B生成C的化学方程式为 。
(3) C的同分异构体中,既能与FeCl3溶液发生显色反应,又能发生银镜反应的有机物共有______种,其中在核磁共振氢谱中出现五组峰的有机物的结构简式为___________。
(4) D的结构简式为 ,D的某同分异构体中含有苯环的碳酸二酯在酸性条件下发生水解反应的化学方程式为 。
查看答案和解析>>
科目:高中化学 来源: 题型:问答题
实验室制取乙酸丁酯的实验装置有如右下图所示两种装置供选用。其有关物质的物理性质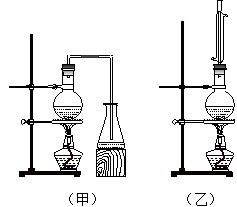
如下表:
| | 乙酸 | 1-丁醇 | 乙酸丁酯 |
| 熔点(℃) | 16.6 | -89.5 | -73.5 |
| 沸点(℃) | 117.9 | 117 | 126.3 |
| 密度(g/cm3) | 1.05 | 0.81 | 0.88 |
| 水溶性 | 互溶 | 可溶(9g/100g水) | 微溶 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
( 11分)乙醇的沸点是78℃,能与水以任意比混溶。乙醚的沸点为34.6℃,难溶于水,在饱和Na2CO3溶液中几乎不溶,乙醚极易燃烧。实验室制醚的反应原理是:
2CH3CH2OH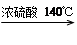 H2O + CH3CH2—O—CH2CH3 (乙醚)
H2O + CH3CH2—O—CH2CH3 (乙醚)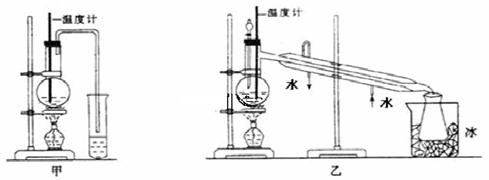
(1)甲图和乙图是两套实验室制乙醚的装置,选装置___(填“甲”或“乙”)最合理,理由是_ 。
(2)反应液中应加入沸石,其作用是____________。
(3)反应中温度计的正确位置是水银球置于________________________。
(4)用上述装置乙制得的乙醚中可能含有大量的杂质,该杂质是__________,除去这种杂质的简易方法是________________________________。
(5)如果温度太高(如170℃),将会发生一个有机副反应,反应方程式为:__________。
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
味精是烹制菜肴时常用的调味品,其主要成分是谷氨酸钠(化学式为C5H8NO4Na)。谷氨酸钠有鲜味,易溶于水。某品牌味精包装上标注:“谷氨酸钠含量≥80%,NaCl含量≤20%”。某学校化学科研小组现对此味精中NaCl的含量进行测定。
查阅资料:资料表明,谷氨酸钠的存在不影响NaCl含量的测定。
设计实验方案:
(1)实验原理:____________________________________________________。
(2)实验试剂:水、试剂X的溶液等。
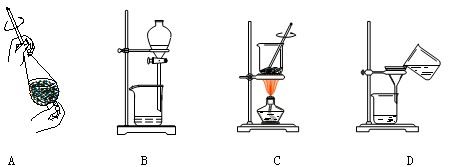
(3)实验过程:(如图所示)
根据上述实验步骤回答下列有关问题:
操作1所需要的玻璃仪器有______________________________________;
用简明扼要的语言描述操作2的过程:_____________________________________________;
通过计算判断该味精中NaCl的质量分数是否符合其包装上标注的标准:
__________________________________________________________________
_________________________________________________________________;
加水溶解所得溶液A为50 mL,则溶液A中NaCl的物质的量浓度是
__________________________________________________________________
________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
为了测定乙醇的结构式是 ,利用乙醇和钠的反应,设计如图装置进行实验,在烧瓶中放入足量的钠,从分液漏斗中缓缓滴入一定量的乙醇,通过测量量筒中水的体积,就可知反应生成的氢气的体积。
,利用乙醇和钠的反应,设计如图装置进行实验,在烧瓶中放入足量的钠,从分液漏斗中缓缓滴入一定量的乙醇,通过测量量筒中水的体积,就可知反应生成的氢气的体积。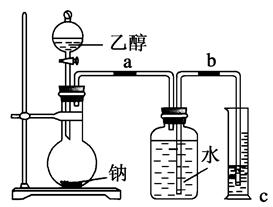
(1)实验前检验该装置的气密性的实验操作是
__________________________________________________。
(2)有人认为装置中有空气,所测的气体体积应扣除装置中空气的体积,才是氢气的体积,你认为________(填“正确”或“不正确”)。
(3)如果实验开始前b导管内未充满水,则实验结果将________(填“偏大”或“偏小”)。
(4)若测得有1.15 g C2H6O参加反应,把量筒c中的水的体积换算成标准状况下H2的体积为280 mL,试结合计算和讨论,判断下面(Ⅰ)和(Ⅱ)两式中,哪个正确________。
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
2008年,三鹿等多家乳制品企业为使蛋白质含量检测合格而加入三聚氰胺,使多名儿童患肾结石,实验室可用下列实验装置测定三聚氰胺的分子式。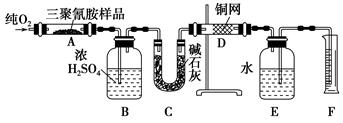
已知三聚氰胺的相对分子质量为126。取1.26 g三聚氰胺样品,放在纯氧中充分燃烧,生成CO2、H2O、N2,实验测得装置B增重0.54 g,C增重1.32g,排入F中水的体积为672 mL(可按标准状况计算)。
(1)E装置的作用是_____________。
(2)需要加热的装置是____________(填字母代号)。
(3)装置D的作用是_________________________________。
(4)F处读数时应该注意:____________、____________。
(5)三聚氰胺的分子式为_________________。
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
在“绿色化学”工艺中,理想的状态是反应物中的原子全部转化为期望的最终产物,即原子的利用率为100%。下列反应类型中能体现“原子经济性”原则的是( )
①置换反应 ②化合反应 ③分解反应 ④取代反应 ⑤加成反应 ⑥加聚反应
| A.①②⑤ | B.②⑤⑥ | C.③④ | D.只有⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列反应不属于取代反应的是 ( )
| A.溴乙烷与氢氧化钠水溶液共热 | B.溴乙烷与氢氧化钠的乙醇溶液共热 |
| C.甲烷与氯气 | D.苯在催化剂作用下能与液溴发生取代反应 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com