
【题目】(1)等温、等压下,等体积的O2和O3所含分子个数比______,质量比为_______。
(2)已知16 g A和20 g B恰好完全反应生成0.04 mol C和31.76 g D,则C的摩尔质量为_____。
(3)在三个密闭容器中分别充入Ne、H2、O2三种气体,当它们的温度和密度都相同时,这三种气体的压强(p)分别用p(Ne)、p(H2)、p(O2)表示,由大到小的顺序是____________。
【答案】1∶1 2∶3 106 g·mol-1 p(H2)>p(Ne)>p(O2)
【解析】
(1)同温同压下,等体积的O2和O3的物质的量相同,根据n=![]() 计算分子数的比,根据n=
计算分子数的比,根据n=![]() 计算质量比;
计算质量比;
(2)根据质量守恒计算C物质的质量,再根据M=![]() 计算C的摩尔质量;
计算C的摩尔质量;
(3)在温度和密度都相同条件下,如体积相同,则质量相同,气体的物质的量越大,压强越大,压强与摩尔质量成反比。
(1)同温同压下,等体积的O2和O3的物质的量相同,设物质的量均为n,根据n=![]() 可知气体的物质的量之比等于二者的分子数之比为1:1;根据n=
可知气体的物质的量之比等于二者的分子数之比为1:1;根据n=![]() 可知二者的质量比为32n:48n=2:3;
可知二者的质量比为32n:48n=2:3;
(2)根据质量守恒定律知,C的质量=(16+20-31.76)g=4.24g,C的摩尔质量M=![]() =
=![]() ;
;
(3)Ne的摩尔质量是20g/mol,氢气的摩尔质量是2g/mol,氧气的摩尔质量是32g/mol,根据![]() 可知密度与摩尔质量成正比;由n=
可知密度与摩尔质量成正比;由n=![]() 可知:气体的物质的量与摩尔质量成反比,气体的物质的量越多,压强就越大。即气体的压强与气体的摩尔质量成反比。气体摩尔质量大小关系:M(O2)>M(Ne)>M(H2),所以其压强大小顺序是P(H2)>P(Ne)>P(O2)。
可知:气体的物质的量与摩尔质量成反比,气体的物质的量越多,压强就越大。即气体的压强与气体的摩尔质量成反比。气体摩尔质量大小关系:M(O2)>M(Ne)>M(H2),所以其压强大小顺序是P(H2)>P(Ne)>P(O2)。


 暑假接力赛新疆青少年出版社系列答案
暑假接力赛新疆青少年出版社系列答案科目:高中化学 来源: 题型:
【题目】下面有关发泡塑料饭盒的叙述,不正确的是
A. 主要材质是高分子材料 B. 价廉、质轻、保温性能好
C. 适用于微波炉加热食品 D. 不适于盛放含油较多的食品
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表是元素周期表的一部分。表中所列的字母分别代表一种化学元素。
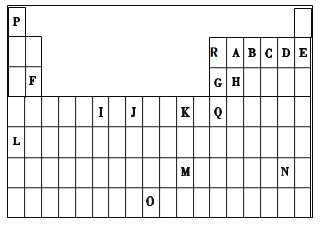
试回答下列问题:
(1)I的最高化合价为__________,J价电子排布图__________。
(2)写出基态时G元素原子中,电子占据的最高能层符号为__________,该能层具有的原子轨道数为____________ 。
(3)第一电离能介于R、B之间的第二周期元素有_____________种。
(4)下列关于元素在元素周期表中的位置以及元素原子的外围电子排布特点的有关叙述不正确的是__________。
a.L位于元素周期表第五周期ⅠA族,属于s区元素
b.O位于元素周期表第七周期Ⅷ族,属于ds区元素
c.M的外围电子排布式为6s1,属于ds区元素
d.H所在族的外围电子排布式为ns2np2,属于p区元素
(5)配合物甲的焰色反应呈紫色,其内界由中心离子J3+与配位体AB-构成,配位数为6,甲的水溶液可用于实验室J2+的定性检验,此方法检验J2+的离子方程式为_____________________。
(6)写出Q元素的简写电子排布式___________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于SO2的说法中,不正确的是
A.SO2能使品红溶液褪色,是因为SO2具有漂白性
B.SO2在空气中极易被氧化为SO3
C.SO2通入Na2SO3或NaHCO3溶液中均能发生反应
D.SO2是形成酸雨的大气污染物之一,主要来自于化石燃料的燃烧和工厂排放的废气
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某有机反应中间体(M)的一种合成路线如图所示。



③标准状况下,气态烃A的密度是H2的14倍
④芳香族化合物H能发生银镜反应
请回答下列问题:
(1)B的名称(系统命名)为_____________ ;H→I的反应类型为___________;
(2)J中官能团的名称为_________,
(3)G→H的化学方程式为____________________________________________;
(4)D+J→M的化学方程式为__________________________________________;
(5)写出符合下列条件的J的所有同分异构体的结构简式________(不考虑立体异构)。
①苯环上连有-NO2 ②核磁共振氢谱有3个峰
符合以上条件的J的所有同分异构体在下列某种表征仪器中显示的信号(或数据)完全相同,该仪器是__________________(填选项字母)。
a.质谱仪 b.红外光谱仪 c.元素分析仪
(6)结合已有知识和相关信息,写出以CH3CHO和E为原料,经三步制备 的合成路线流程图(无机试剂任用)。合成路线流程图示例为:
的合成路线流程图(无机试剂任用)。合成路线流程图示例为: _____________
_____________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有M、N两种溶液,经测定这两种溶液中含有下列12种离子:Al3+、Cl-、Na+、K+、NO3-、OH-、Fe2+、AlO2-、CO32-、NH4+、SO42-、H+。
(1)完成下列表格中实验①的结论和实验②的实验内容以及现象:_____________、_________________

(2)根据(1)中的实验回答:
NO3-存在于________溶液中,理由是___________________________________________;
Cl-存在于________溶液中,理由是__________________________________________。
(3)根据(1)中的实验确定,M溶液中含有的离子为__________________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室制取氨气通常有两种方法:
①用固体氢氧化钙与氯化铵共热;
②在常温下用固体氢氧化钠与浓氨水反应。

(1)上面的制取装置图中,方法①应选用装置__________(填“A”或“B”,下同);方法②应选用装置__________。
(2)加热氯化铵与氢氧化钙混合物制取氨气的反应方程式是________________。
(3)在制取后,如果要干燥氨气,应选用的干燥剂是________________(填字母)。
A.浓硫酸 B.碱石灰 C.五氧化二磷
(4)检验集气瓶中是否收集满氨气的方法是__________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NA为阿伏加德罗常数的数值,下列叙述错误的是( )
A. 18gH2O中含有的质子数为10NA
B. 1.0L1.0mo1·L-1的NaAlO2水溶液中含有的氧原子数为2NA
C. 46gNO2和N2O4混合气体中含有原子总数为3NA
D. 1molNa与足量O2反应,生成Na2O和Na2O2的混合物,钠失去NA个电子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Se、Br两种元素的部分信息如图所示,下列说法正确的是
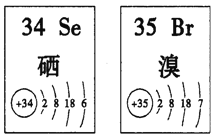
A. 原子半径:Br>Se>P B. 还原性:S2->Se2->Br-
C. SeO2既有氧化性又有还原性 D. 在Se2Br2分子中只含有极性键
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com