
【题目】为保护加酶洗衣粉洗涤效果,应注意
A. 使用沸水先冲泡洗衣粉 B. 用含氯较高的自来水作水源
C. 和其他洗涤剂混合使用 D. 室温时用饮用水先溶解洗衣粉
科目:高中化学 来源: 题型:
【题目】化学概念在逻辑上存在如图关系,对下列概念的说法正确的是( )

A. 化合物与氧化物属于交叉关系
B. 单质与非电解质属于包含关系
C. 溶液与分散系属于并列关系
D. 化合物与电解质属于包含关系
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件下,在体积为V L的密闭容器中发生化学反应CO(g)+2H2(g)![]() CH3OH(g),可判断该可逆反应达到化学平衡状态的标志是
CH3OH(g),可判断该可逆反应达到化学平衡状态的标志是
A. v生成(CH3OH)=v消耗(CO)
B. 混合气体的密度不再改变
C. 混合气体的平均相对分子质量不再改变
D. CO、H2、CH3OH的浓度比为1:2:1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一种可用于生物医学领域的平面五角星形钯(Ⅱ)配位络离子结构如右图,已知钯是原子序数为46的过渡元素。
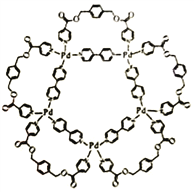
回答下列问题。
(1)钯(Ⅱ)配位络离子中的第二周期元素,其第一电离能从大到小的顺序为_____________(填元素符号)。
(2)钯(Ⅱ)配位络离子中含有的作用力类型为___________ (填序号)。
A.金属键 B.离子键 C.共价键 D.配位键 E.氢键 F.范德华力
(3)钯(Ⅱ)配位络离子中基态钯离子价电子排布式为____________,钯离子的杂化轨道类型_______(填“是”或“不是”)sp3,理由是___________。
(4)钯(Ⅱ)配位络离子中能与氢氧化钠溶液反应的配体,其分子式为__________,每1mol该配体与氢氧化钠反应时断裂的共价键类型及数目为____________。
(5)钯易与亚砜(![]() )生成配合物。当R1和R2都为-CH2C6H5时,三种配合物的结构和键长数据如下:
)生成配合物。当R1和R2都为-CH2C6H5时,三种配合物的结构和键长数据如下:
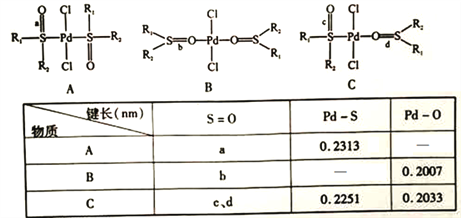
①亚砜的晶体类型为___________________。
②配位键稳定性:Pd-s>Pd-O,其证据为______________ (用上表数据说明)。
③三种配合物中S=O键长不同,其数值最小的是______________(填“a"“b"“c”或“d")
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图中的电化学装置以甲醇(CH3OH)为主要原料合成碳酸二甲酯[(CH3O)2CO],相关说法错误的是
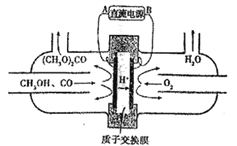
A. B是直流电源的负极
B. 碳酸二甲酯中碳均为+4价
C. 阳极附近溶液pH降低
D. 每当有2molH+通过离子交换膜,消耗氧气的体积在标准状况下为11.2L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】五氯化磷(PCl5)常温下是一种淡黄色固体,在潮湿空气中水解产生两种酸。PCl5在有机合成中被广泛用作氯化剂、催化剂、脱水剂等,高纯度PCl5主要用于医药中间体及锂电池原材料的合成。工业生产PCl5的传统方法是在搅拌式反应釜中注入液体三氯化磷(PCl3),再通入氯气在合适的温度下发生反应:PCl3+Cl2![]() PCl5。某工厂对传统方法进行了改进以生产高纯度PCl5,主要流程如下图所示(循环水的作用是控制温度)。
PCl5。某工厂对传统方法进行了改进以生产高纯度PCl5,主要流程如下图所示(循环水的作用是控制温度)。
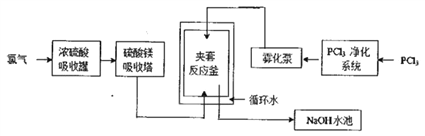
请回答下列相关问题。
(1)工业生产氯气的主要方法的离子方程式是___________,利用该反应所得产品可继续生产_________(任写一种)等化工产品。
(2)浓硫酸吸收罐和硫酸镁吸收塔的作用是______________________,若去掉这两个设备夹套反应釜中发生的主要副反应是______________________________。
(3)夹套反应釜中的原料混合方式与搅拌式反应釜相比主要优点是____________________________。 (4)NaOH水池的作用是_______________________,从降低生产成本的角度考虑NaOH溶液可更换为______。
(5)生产过程中PCl3的加料速率会对生产造成明显的影响,具体情况如下表。根据表中数据判断最佳的加料速率范围是_________________kg·h-1。
PCl3加料速率/kg·h-1 | PCl5状态 | 热交换情况 | 生产500kg产品的周期/h |
40 | 致密、坚硬、造粒困难 | 快、温度可控 | 11.5 |
50 | 致密、坚硬、造粒困难 | 快、温度可控 | 9.2 |
60 | 较松散、造粒容易 | 较快、温度可控 | 7.2 |
70 | 松散、造粒容易 | 较快、温度可控 | 6.5 |
80 | 松散、造粒容易 | 慢、温度升高难以控制 | 5.3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】1894年,Fenton发现采用Fe2+和H2O2混合溶液,能产生具有高反应活性和强氧化性的羟基自由基(-OH),从而氧化降解有机污染物,称为Fenton反应。电Fenton法采用惰性电极电解法,右图为其中一个电极的反应机理,其中含有Fenton反应。下列说法不正确的是( )
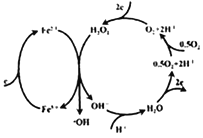
A. 羟基自由基(-OH)的电子式为:![]()
B. 右图所在的惰性电极应与外接电源的负极相连
C. Fenton反应:Fe2++H2O2==Fe3++OH-+-OH
D. 右图所在的惰性电极每消耗22.4LO2(标准状况),理论上在外电电路中转移4mole-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法不正确的是( )
A.氯化钠可用于制备纯碱
B.食品袋中常放有生石灰,能起到抗氧化剂的作用
C.大力发展新能源汽车能减少酸雨危害
D.石油裂化、煤的干馏、玉米制乙醇、蛋白质变性都属于化学变化
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com