
【题目】氢氧燃料电池可以使用在航天飞机上,其反应原理示意图如右图。下列有关氢氧燃料电池的说法不正确的是

A. 该装置将化学能转化为电能
B. 为了增加灯泡亮度,可以将电极碳棒变得粗糙多孔
C. 电子迁移方向:电极a→灯泡→电极b→电解质溶液→电极a
D. 该电池的总反应:2H2+O2=2H2O
科目:高中化学 来源: 题型:
【题目】镁化合物具有广泛用途。请回答有关镁的下列问题:
(1)单质镁在空气中燃烧的主要产物是白色的____,还生成少量的______(填化学式);
(2)CH3MgCl是一种重要的有机合成试剂,其中镁的化合价是___________,该化合物水解的化学方程式为____________;
(3)下图是金属镁和卤素反应的能量变化图(反应物和产物均为298K时的稳定状态)。
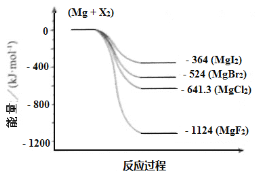
下列选项中正确的是_____________(填序号)。
① MgI2中Mg2+ 与I- 间的作用力小于MgF2中Mg2+ 与F- 间的作用力
② Mg与F2的反应是吸热反应
③ MgBr2与Cl2 反应的△H > 0
④ 化合物的热稳定性顺序为MgI2 < MgBr2 < MgCl2 < MgF2
⑤ MgF2(s) + Br2(l) = MgBr2(s) + F2(g) △H = +600 kJ · mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】环境保护是当今倍受人们关注的社会问题.下列叙述不正确的是( )
A.二氧化硫会形成酸雨
B.氮氧化物会形成光化学烟雾
C.过度使用煤作能源会引起雾霾等环境危害
D.一氧化碳是造成温室效应的主要物质
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用Cl2生产某些含氯有机物时会产生副产物HCl。利用反应A,可实现氯的循环利用。反应A:4HCl+O2![]() 2Cl2+2H2O
2Cl2+2H2O
已知:ⅰ.反应A中,4 mol HCl被氧化,放出115.6 kJ的热量。
ⅱ.
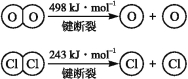
(1)反应A的热化学方程式是 。
(2)断开1 mol H—O键与断开1 mol H—Cl键所需能量相差约为 kJ,H2O中H—O键比HCl中H—Cl键(填“强”或“弱”) 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A. 需要加热才能发生的反应一定是吸热反应
B. 放热反应在常温下一定很容易发生
C. 反应是放热还是吸热,取决于反应物和生成物所具有的总能量的相对大小
D. 在一定条件下,某可逆反应正向是吸热反应,则其逆向必是放热反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学选修5:有机化学基础
有机物H(C25H44O5)是一种新型治疗高血压病的药物,工业上以淀粉、烃A为基本原料合成H的路线如下图所示。

巳知:(i)烃A在质谱图中的最大质荷比为72,B分子中核磁共振氢谱有2个峰且面积比为9:2。
(ii)  。
。
(iii)反应③中发生反应的E、G物质的量之比为4:1。
(1)A的分子式为_____;B的名称是_______;C的结构简式为_______。
(2)反应②的类型是______;F中的官能团名称是_______。
(3)写出反应①的化学方程式:___________。
(4)E有多种同分异构体,其中满足下列条件的同分异构体共有____种,核磁共振氢谱有4个峰的物质结构简式为__________。
①能发生银镜反应 ②能与单质钠发生反应
(5)1,3-丁二烯是一种重要化工原料,以乙醛为基本原料可制得该烃,请写出相应的转化流程图:__________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据下列实验事实:
(1)X+Y2+===X2++Y
(2)Z+2H2O![]() Z(OH)2+H2↑
Z(OH)2+H2↑
(3)Z2+离子的氧化性比X2+弱
(4)由Y、W作电极组成的原电池反应为:Y-2e-===Y2+
由此可知,X、Y、Z、W的还原性由强到弱的顺序是()
A. X>Y>Z>W B. Y>X>W>Z
C. Z>X>Y>W D. Z>Y>X>W
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)已知:在298K、101kPa时,
①C(s,石墨)+O2(g) = CO2(g) △H1 = -400 kJ·mol-1;
②2H2(g)+O2(g) = 2H2O(l) △H2 = -570 kJ·mol-1;
③2C2H2(g)+5O2(g) = 4CO2(g)+ 2H2O(l) △H3 = -2600 kJ·mol-1;
写出298K时由C(s,石墨)和H2(g)生成1 mol C2H2(g)反应的热化学方程式 。以硫酸为电解质溶液,依据反应③设计一个燃料电池,写出其电极反应式 。
(2)工业合成氨的反应原理为 N2(g)+3H2(g)![]() 2NH3(g) ΔH=-92.4 kJ·mol-1某温度下,把10 mol N2与25mol H2置于容积为10 L的密闭容器内,10 min时反应达到平衡状态,测得氮气的平衡转化率为50%,则10 min内该反应的平均速率v(H2)= mol·L-1·min-1,则该温度下该反应的平衡常数K= 。
2NH3(g) ΔH=-92.4 kJ·mol-1某温度下,把10 mol N2与25mol H2置于容积为10 L的密闭容器内,10 min时反应达到平衡状态,测得氮气的平衡转化率为50%,则10 min内该反应的平均速率v(H2)= mol·L-1·min-1,则该温度下该反应的平衡常数K= 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com