
【题目】用Cl2生产某些含氯有机物时会产生副产物HCl。利用反应A,可实现氯的循环利用。反应A:4HCl+O2![]() 2Cl2+2H2O
2Cl2+2H2O
已知:ⅰ.反应A中,4 mol HCl被氧化,放出115.6 kJ的热量。
ⅱ.
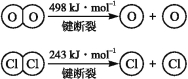
(1)反应A的热化学方程式是 。
(2)断开1 mol H—O键与断开1 mol H—Cl键所需能量相差约为 kJ,H2O中H—O键比HCl中H—Cl键(填“强”或“弱”) 。
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】一定温度下,体积不变的密闭容器中,对可逆反应A(g) + 2B(g)![]() 3C(g) + D(s) 的下列叙述中,能说明反应已达到平衡的是:
3C(g) + D(s) 的下列叙述中,能说明反应已达到平衡的是:
A. 单位时间内消耗a mol A,同时生成3a mol C
B. C的生成速率与C的分解速率相等
C. 混合气体的总物质的量不再变化
D. 容器内的压强不再变化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】电解H2SO4和NaCl的混合溶液,起始一段时间阴极和阳极上分別析出的物质是
A. H2、O2 B. Cu、O2 C. H2、Cl2 D. Cu、Cl2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知25℃时一些难溶物质的溶度积常数如下:
化学式 | Zn(OH)2 | ZnS | AgCl | Ag2S | MgCO3 | Mg(OH)2 |
溶度积 | 5×10-17 | 2.5×10-22 | 1.8×10-10 | 6.3×10-50 | 6.8×10-6 | 1.8×10-11 |
根据上表数据,判断下列化学方程式不正确的是
A. 2AgCl+Na2S═2NaCl+Ag2S
B. MgCO3+H2O![]() Mg(OH)2+CO2↑
Mg(OH)2+CO2↑
C. ZnS+2H2O═Zn(OH)2+H2S↑
D. Mg(HCO3)2+2Ca(OH)2═Mg(OH)2↓+2CaCO3↓+2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述正确的是
A. 含金属元素的离子一定是阳离子
B. 金属阳离子被还原一定得到金属单质
C. 共价化合物中只含共价键
D. 1H、2H、3H互为同素异形体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氢氧燃料电池可以使用在航天飞机上,其反应原理示意图如右图。下列有关氢氧燃料电池的说法不正确的是

A. 该装置将化学能转化为电能
B. 为了增加灯泡亮度,可以将电极碳棒变得粗糙多孔
C. 电子迁移方向:电极a→灯泡→电极b→电解质溶液→电极a
D. 该电池的总反应:2H2+O2=2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以烃A为主要原料,采用以下路线合成药物X、Y和高聚物Z。
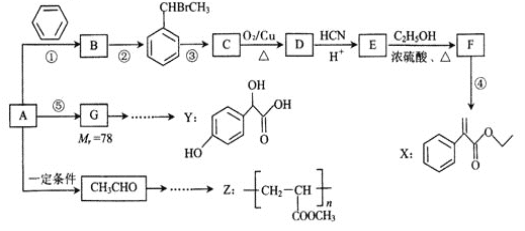
已知:

Ⅱ.反应①、反应②、反应⑤的原子利用率均为100%。
请回答下列问题:
(1)B的名称为______________。
(2)X中的含氧官能团名称为____,反应③的条件为_______,反应③的反应类型是_________。
(3)关于药物Y 的说法正确的是_________________。
的说法正确的是_________________。
A.药物Y的分子式为C8H804,遇氯化铁溶液可以发生显色反应
B.1mol药物Y与H2、浓溴水中的Br2反应,最多消耗分别为4 mol和2 mol
C.1mol药物Y与足量的钠反应可以生成33.6 L氢气
D.药物Y中⑥、⑦、⑧三处- OH的电离程度由大到小的顺序是⑧>⑥>⑦
(4)写出反应E-F的化学方程式_____________________________________。
(5)写出符合下列条件的E的所有同分异构体的结构简式________________________。
①属于酚类化合物,且是苯的对位二元取代物;②能发生银镜反应和水解反应。
(6)设计一条以CH3CHO为起始原料合成Z的线路(无机试剂及溶剂任选) ___________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】同温同压下,下列各组热化学方程式中,△H1<△H2是
A.C(s)+![]() O2(g)=CO(g);△H1 C(s)+O2(g)=CO2(g);△H2
O2(g)=CO(g);△H1 C(s)+O2(g)=CO2(g);△H2
B.![]() H2(g)+
H2(g)+![]() Cl2(g)=HCl(g);△H1 H2(g)+Cl2(g)=2HCl(g);△H2
Cl2(g)=HCl(g);△H1 H2(g)+Cl2(g)=2HCl(g);△H2
C.S(g)+O2(g)=SO2(g);△H1 S(s)+O2(g)=SO2(g); △H2
D.2H2(g)+O2(g)=2H2O(g);△H1 2H2(g)+O2(g)=2H2O(l);△H2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com