
【题目】下列各分子中,化学键类型有差异的是
A. H2O、CO2 B. MgF2、H2O2
C. NaOH、Ba(OH)2 D. NaCl、KCl
 学业测评一课一测系列答案
学业测评一课一测系列答案科目:高中化学 来源: 题型:
【题目】已知:Na2S2O3+H2SO4===Na2SO4+SO2↑+S↓+H2O,下列各组实验中,反应速率最快的是
组号 | 反应 | Na2S2O3 | H2SO4 | H2O | ||
体积/ mL | 浓度/ mol·L-1 | 体积/ mL | 浓度/ mol·L-1 | 体积/ mL | ||
A | 10 | 5 | 0.2 | 5 | 0.1 | 10 |
B | 10 | 5 | 0.1 | 5 | 0.1 | 10 |
C | 30 | 5 | 0.1 | 5 | 0.1 | 10 |
D | 30 | 5 | 0.2 | 5 | 0.2 | 10 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某研究性学习小组的同学通过查阅资料得到如下信息:草酸晶体(H2C2O4·2H2O)无色,熔点为101℃,受热脱水、升华,易溶于水,170℃以上分解可得到CO、CO2、H2O,H2C2O4难溶于水。他们欲利用如下装置验证上述产物(加热仪器、夹持仪器省略)。
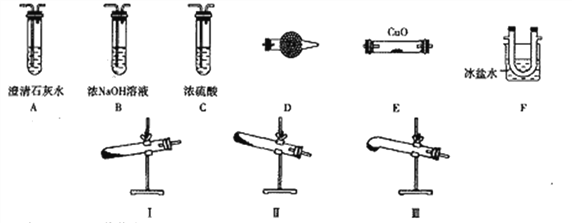
(1)加热草酸晶体使其分解的装置是________(从I、II、III中选取),验证其分解产物的装置依次是______→A→尾气处理装置(用装置字母作答,装置可重复使用)。
(2)D中试剂是_________,证明有CO生成的现象是_______。
(3)实验中有两处需要加热,加热的顺序是_________,写出一种处理尾气的方法:_____________。
(4)若上述实验均产生了预期的现象,写出草酸分解的化学方程式:_________________。
(5)设计一种方案证明草酸是弱酸_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据下图所示回答有关问题:

(1)甲池为_________(选填“原电池”或“电解池”),
(2)乙池中Zn棒上发生反应的电极反应式为:____________________.
(3)石墨A上收集到1.12L气体(标况下),则反应过程中转移的电子数为__________.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用Cl2生产某些含氯有机物时会产生副产物HCl。利用反应A,可实现氯的循环利用。反应A:4HCl+O2![]() 2Cl2+2H2O
2Cl2+2H2O
已知:ⅰ.反应A中,4 mol HCl被氧化,放出115.6 kJ的热量。
ⅱ.
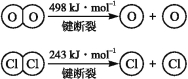
(1)反应A的热化学方程式是 。
(2)断开1 mol H—O键与断开1 mol H—Cl键所需能量相差约为 kJ,H2O中H—O键比HCl中H—Cl键(填“强”或“弱”) 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Q、R、T、M、W五种短周期元素在周期表中的相对位置如图所示,其中M的原子序数是R的原子序数的2倍。下列说法正确的是( )
![]()
A. MW6中各原子核外均满足8电子稳定结构
B. Q、W的单核离子的核外电子数相等
C. 五种元素均能形成氢化物
D. W的氢化物水溶液酸性最强,说明W的非金属性在五种元素中最强
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学选修5:有机化学基础
有机物H(C25H44O5)是一种新型治疗高血压病的药物,工业上以淀粉、烃A为基本原料合成H的路线如下图所示。

巳知:(i)烃A在质谱图中的最大质荷比为72,B分子中核磁共振氢谱有2个峰且面积比为9:2。
(ii)  。
。
(iii)反应③中发生反应的E、G物质的量之比为4:1。
(1)A的分子式为_____;B的名称是_______;C的结构简式为_______。
(2)反应②的类型是______;F中的官能团名称是_______。
(3)写出反应①的化学方程式:___________。
(4)E有多种同分异构体,其中满足下列条件的同分异构体共有____种,核磁共振氢谱有4个峰的物质结构简式为__________。
①能发生银镜反应 ②能与单质钠发生反应
(5)1,3-丁二烯是一种重要化工原料,以乙醛为基本原料可制得该烃,请写出相应的转化流程图:__________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】二氧化碳的回收利用是环保领域研究的热点课题。
(1)在太阳能的作用下,以CO2为原料制取炭黑的流程如图1所示,其总反应的化学方程式为_________。

(2)CO2经过催化氢化合成低碳烯烃.其合成乙烯的反应为2CO2(g)+6H2(g)![]() CH2=CH2(g)+4H2O(g)△H,几种物质的能量(在标准状况下,规定单质的能量为0,测得其他物质在生成时所放出或吸收的热量)如下表所示:
CH2=CH2(g)+4H2O(g)△H,几种物质的能量(在标准状况下,规定单质的能量为0,测得其他物质在生成时所放出或吸收的热量)如下表所示:
物质 | H2(g) | CO2(g) | CH2=CH2(g) | H2O(g) |
能量/kJmol-1 | 0 | -394 | 52 | -242 |
则△H=_________。
(3)在2L恒容密闭容器中充入2molCO2和nmolH2,在一定条件下发生(2)中的反应,CO2的转化率与温度、投料比[X= ![]() ]的关系如图2所示。
]的关系如图2所示。
①X1_________X2(填“>”、“<”或“=”,下同),平衡常数KA_________KB.
②若B点的投料比为3,且从反应开始到B点需要10min,则v(H2)=_________。
(4)以稀硫酸为电解质溶液,利用太阳能将CO2转化为低碳烯烃,工作原理图如图3。
①b电极的名称是_________;
②产生丙烯的电极反应式为_______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】 恒温恒压下,在容积可变的器皿中,反应2NO2 (g)![]() N2O4 (g)达到平衡后,再向容器内通入一定量NO2,又达到平衡时,N2O4的体积分数
N2O4 (g)达到平衡后,再向容器内通入一定量NO2,又达到平衡时,N2O4的体积分数
A.减小 B.增大 C.不变 D.无法判断
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com