
����Ŀ��������̼�Ļ��������ǻ��������о����ȵ���⡣
��1����̫���ܵ������£���CO2Ϊԭ����ȡ̿�ڵ�������ͼ1��ʾ�����ܷ�Ӧ�Ļ�ѧ����ʽΪ_________��

��2��CO2�������⻯�ϳɵ�̼ϩ������ϳ���ϩ�ķ�ӦΪ2CO2��g��+6H2��g��![]() CH2=CH2��g��+4H2O��g����H���������ʵ��������ڱ�״���£��涨���ʵ�����Ϊ0�������������������ʱ���ų������յ����������±���ʾ��
CH2=CH2��g��+4H2O��g����H���������ʵ��������ڱ�״���£��涨���ʵ�����Ϊ0�������������������ʱ���ų������յ����������±���ʾ��
���� | H2��g�� | CO2��g�� | CH2=CH2��g�� | H2O��g�� |
����/kJmol-1 | 0 | -394 | 52 | -242 |
���H=_________��
��3����2L�����ܱ������г���2molCO2��nmolH2����һ�������·�����2���еķ�Ӧ��CO2��ת�������¶ȡ�Ͷ�ϱ�[X= ![]() ]�Ĺ�ϵ��ͼ2��ʾ��
]�Ĺ�ϵ��ͼ2��ʾ��
��X1_________X2�����������������=������ͬ����ƽ�ⳣ��KA_________KB��
����B���Ͷ�ϱ�Ϊ3���Ҵӷ�Ӧ��ʼ��B����Ҫ10min����v��H2��=_________��
��4����ϡ����Ϊ�������Һ������̫���ܽ�CO2ת��Ϊ��̼ϩ��������ԭ��ͼ��ͼ3��
��b�缫��������_________��
�ڲ�����ϩ�ĵ缫��ӦʽΪ_______________��
���𰸡� ![]()
![]()
![]()
![]()
![]()
![]()
![]()
����������1����700K�����£�CO2��FeO������Ӧ����C��Fe3O4������1��Fe3O4�ֽ�����FeO��O2������������Ӧ������FeO�����������ݷ�Ӧ��������P��Ӧ������д����ʽΪCO2![]() C+O2���ʴ�Ϊ��CO2
C+O2���ʴ�Ϊ��CO2![]() C+O2��
C+O2��
��2���ʱ������������������ȥ��Ӧ������������÷�Ӧ���ʱ�=[52+��-242����4-��-392����2-0]kJ/mol=-128kJ/mol���ʴ�Ϊ��-128kJ/mol��
��3������ͬ�����£�Ͷ�ϱ�[X=![]() ]Խ������̼��ת����Խ����ͼ֪����ͬ�¶���X1��ת���ʴ���X2������X1��X2���÷�Ӧ������Ӧ�Ƿ��ȷ�Ӧ���¶�Խ����ƽ�ⳣ��ԽС���¶�A��B������ƽ�ⳣ��A��B���ʴ�Ϊ����������
]Խ������̼��ת����Խ����ͼ֪����ͬ�¶���X1��ת���ʴ���X2������X1��X2���÷�Ӧ������Ӧ�Ƿ��ȷ�Ӧ���¶�Խ����ƽ�ⳣ��ԽС���¶�A��B������ƽ�ⳣ��A��B���ʴ�Ϊ����������
����B���Ͷ�ϱ�Ϊ3���Ҵӷ�Ӧ��ʼ��B����Ҫ10min��n��CO2��=2mol����n��H2��=10mol��B�������̼��ת����Ϊ75%����μӷ�Ӧ��n��CO2��=2mol��75%=1.5mol�����ݶ�����̼������֮��Ĺ�ϵʽ֪���μӷ�Ӧ��n��H2��=3n��CO2��=4.5mol����v��H2��=![]() =
=![]() =0.225mol/��L��min�����ʴ�Ϊ��0.225mol/��L��min����
=0.225mol/��L��min�����ʴ�Ϊ��0.225mol/��L��min����
��4��������ͼ֪�����������ĵ缫�������������������ĵ�Դ�缫Ϊ����������bΪ�������ʴ�Ϊ��������
�������϶�����̼�õ��Ӻ������ӷ�Ӧ���ɱ�ϩ��ˮ���缫��ӦʽΪ3CO2+18H++18e-��CH3CH=CH2+6H2O���ʴ�Ϊ��3CO2+18H++18e-��CH3CH=CH2+6H2O��


 һ����ʦ�����Ծ�ϵ�д�
һ����ʦ�����Ծ�ϵ�д� �����Ծ���Ԫ���Ծ�ϵ�д�
�����Ծ���Ԫ���Ծ�ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��A��B��C��D����ԭ��������������ķֱ�λ��������ͬ�����ڵ�����Ԫ�أ�m��n��p�ֱ���Ԫ��A��B��C���ĵ��ʣ� x��y��z����A��B��C��ɵĶ�Ԫ���������y��z��������y�������������ϣ�����֮��������ת����ϵ��D�ĵ��ʿ�����ˮ�����û���Ӧ������˵����ȷ����
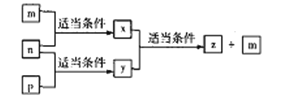
A. D�ĵ������ȼ��ʱ����y������
B. Ԫ�صķǽ�����:C>A>B>D
C. B��C��D��A�γɵļ�������۵�:C>D>B
D. ԭ�Ӱ뾶:D>B>C>A
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����и������У���ѧ�������в������
A. H2O��CO2 B. MgF2��H2O2
C. NaOH��Ba(OH)2 D. NaCl��KCl
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪���������η���![]() �����ͷ���
�����ͷ���![]() ��Ӧ�������������η���
��Ӧ�������������η���![]() ��ֱ���ͷ���
��ֱ���ͷ���![]() �����
�����![]() �����е�Ԫ�ص�ԭ��������С��10�����
�����е�Ԫ�ص�ԭ��������С��10�����![]() ���ӵ�Ԫ��Ϊ�������ڵ�Ԫ�ء�����ͼ���������ж�����ȷ���ǣ� ��
���ӵ�Ԫ��Ϊ�������ڵ�Ԫ�ء�����ͼ���������ж�����ȷ���ǣ� ��

A. ���³�ѹ�£� ![]() ��һ��Һ̬�л��� B.
��һ��Һ̬�л��� B. ![]() ��һ�ֺ��зǼ��Լ��ķ���
��һ�ֺ��зǼ��Լ��ķ���
C. �����![]() ��Ư����ɫ���� D. ������Ӧ��������ȡ����Ӧ
��Ư����ɫ���� D. ������Ӧ��������ȡ����Ӧ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������AΪ��Ҫԭ�ϣ���������·�ߺϳ�ҩ��X��Y�߾���Z��
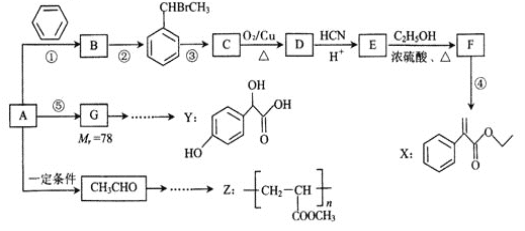
��֪��

������Ӧ������Ӧ������Ӧ����ԭ�������ʾ�Ϊ100%��
��ش��������⣺
(1)B������Ϊ______________��
(2)X�еĺ�������������Ϊ____����Ӧ��������Ϊ_______����Ӧ���ķ�Ӧ������_________��
(3)����ҩ��Y ��˵����ȷ����_________________��
��˵����ȷ����_________________��
A��ҩ��Y�ķ���ʽΪC8H804�����Ȼ�����Һ���Է�����ɫ��Ӧ
B��1molҩ��Y��H2��Ũ��ˮ�е�Br2��Ӧ��������ķֱ�Ϊ4 mol��2 mol
C��1molҩ��Y���������Ʒ�Ӧ��������33.6 L����
D��ҩ��Y����������������- OH�ĵ���̶��ɴ�С��˳������>��>��
(4)д����ӦE-F�Ļ�ѧ����ʽ_____________________________________��
(5)д����������������E������ͬ���칹��Ľṹ��ʽ________________________��
�����ڷ��������DZ��Ķ�λ��Ԫȡ������ܷ���������Ӧ��ˮ�ⷴӦ��
(6)���һ����CH3CHOΪ��ʼԭ�Ϻϳ�Z����·�����Լ����ܼ���ѡ�� ___________________
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������������ȷ����
A. ͬ��ͬѹ�£���ͬ��������ʣ������ʵ���һ�����
B. �����ʵ����ļ����һ����̼�����ķ�����ǰ�ߴ��ں���
C. 1Lһ����̼����һ����1L����������С
D. ��ͬ�����µ�һ����̼�͵����������������ȣ�������Ҳ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ֶ���������Ԫ��W��X��Y��Z��ԭ��������������W��X�ļ����Ӿ�����ͬ���Ӳ�ṹ��X��ԭ�Ӱ뾶�Ƕ���������Ԫ��ԭ�������ģ�W��Yͬ�壬Z��X�γɵ����ӻ������ˮ��Һ�����ԡ�����˵����ȷ���ǣ� ��
A. �����Ӱ뾶��W<X<Z B. W��X�γɵĻ���������ˮ����Һ�ʼ���
C. ��̬�⻯������ȶ��ԣ�W<Y D. ����������ˮ��������ԣ�Y>Z
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij������ˮ�к�����̬�ȣ�ͨ������ʵ��ⶨ��Ũ��
��ȡˮ��20.0mL����ƿ������10��0 mLKI��Һ(����)������ָʾ��2-3�Ρ�
��ȡһ�ζ�������������ˮ������ˮϴ����Ȼ��ע��0��01 mol��L��1��Na2S2O3��Һ������Һ�棬���¶�����
������ƿ���ڵζ����½��еζ��������ķ�ӦΪ��I2+2Na2S2O3 =2NaI+Na2S4O6��
�Իش��������⣺
��1�������������ָʾ����______________��
(2) ������Ӧʹ��____________ʽ�ζ��ܡ�
��3���������ζ��յ������_______________________________��
��4������ȥNa2S2O3��Һ20��00mL�����ˮ��C12�����ʵ���Ũ��Ϊ______________ ��
��5����ָ��ʵ���е�һ�����Դ���_______________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ȼ�ϵ���Ƿ�����ɫ��ѧ��������ͷ���װ�á���ͼΪ�õ�صĹ���ԭ��ʾ��ͼ���õ�صĵ缫�����һ��ϸС�IJ��ۣ��������������ǿ�������ȶ�����ش�
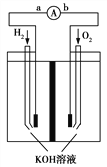
��1������ȼ�ϵ�طŵ�ʱ����ת����ʽ��Ҫ��________��
�ڵ����е�����������Ϊ________(��a.b��ʾ)��
��2��������ӦʽΪ__________________��
��3���缫����Ʋ��۵�ԭ��Ϊ__________________��
��4���õ�ع���ʱ��H2��O2�������ⲿ��������ؿ����������ṩ���ܡ���ˣ�������ȫ�����ǹؼ�����֮һ���������һ����Ҫ�Ĵ�����ϣ�����ͷ���ԭ�����£�
��.Li��H2![]() 2LiH ��.LiH��H2O===LiOH��H2��
2LiH ��.LiH��H2O===LiOH��H2��
�ٷ�Ӧ���еĻ�ԭ����________����Ӧ���е���������____________��
��֪LiH������ܶ�Ϊ0.82 g/cm3���������224 L(��״��)H2�����ɵ�LiH����뱻���յ�H2�����Ϊ________��
�۽��ɢ����ɵ�LiH��H2O���÷ų���H2�������ȼ�ϣ�������ת����Ϊ80%��������ͨ�����ӵ����ʵ���Ϊ________mol��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com