
 状元坊全程突破导练测系列答案
状元坊全程突破导练测系列答案 直通贵州名校周测月考直通名校系列答案
直通贵州名校周测月考直通名校系列答案科目:高中化学 来源:不详 题型:单选题
| A.8,3 | B.5,8 | C.3,8 | D.8,5 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题

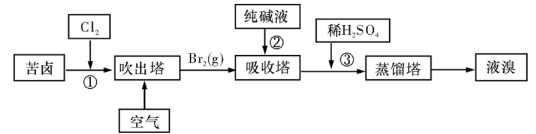
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.从海带中提取碘单质的过程涉及氧化还原反应 |
| B.往淡水中加入NaCl等配成的人造海水,可用于海产品的长途运输 |
| C.赤潮主要是由工农业生产和生活废水引起沿海水域的富营养化而造成的 |
| D.海洋经济专属区的资源开发可获得Fe、Co、K、Au、Mg、B等金属 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
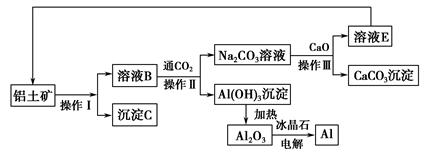
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.海水中含有钾元素,只需经过物理变化就可以得到钾单质 |
| B.海水蒸发制海盐的过程中只发生了化学变化 |
| C.从海水中可以得到NaCl,电解熔融NaCl可制备Cl2 |
| D.利用潮汐发电是将化学能转化为电能 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
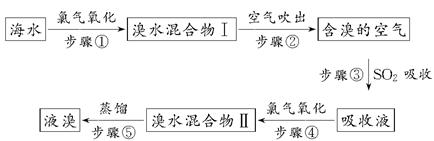
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
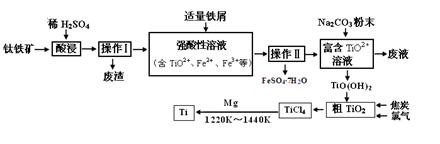

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com