
| A.海水中含有钾元素,只需经过物理变化就可以得到钾单质 |
| B.海水蒸发制海盐的过程中只发生了化学变化 |
| C.从海水中可以得到NaCl,电解熔融NaCl可制备Cl2 |
| D.利用潮汐发电是将化学能转化为电能 |
 导学全程练创优训练系列答案
导学全程练创优训练系列答案科目:高中化学 来源:不详 题型:填空题
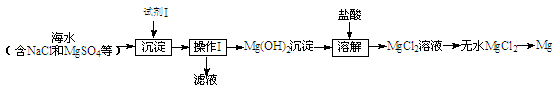
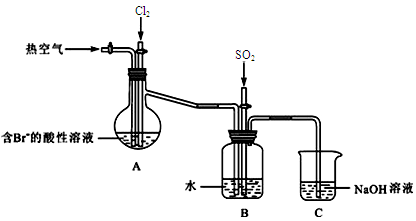
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.制钛:用金属钠置换出氯化钛(TiCl4)溶液中的钛 |
| B.炼铁:用焦炭和空气反应产生的一氧化碳在高温下还原铁矿石中的铁 |
| C.制钠:用海水作原料制得精盐,再电解纯净氯化钠溶液得到金属钠 |
| D.炼铜:用黄铜矿经电解精炼得到纯度为99.9%的铜 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
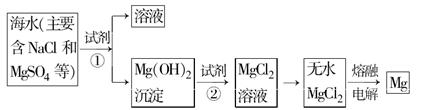
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
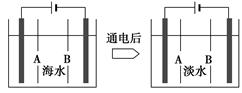
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.浓硫酸遇明火爆炸 |
| B.浓硫酸遇水发热爆炸 |
| C.铁与水(常温下)反应产生的氧化物爆炸 |
| D.稀释后的硫酸与铁反应产生的氢气在空气中遇明火而爆炸 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.蒸馏法是海水淡化的方法之一 |
| B.淡水的密度小于海水的密度 |
| C.融化的雪水中矿物质含量比深井水中的少 |
| D.0 ℃以上,温度越高,水的密度越小 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题

 2I-+S4O62-)
2I-+S4O62-)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com