
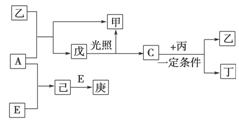
在有机化工生产中,下图是合成某种聚酯纤维H的流程图.

已知:A、D为烃,质谱图表明G的相对分子质量为166,其中含碳57.8%,含氢3.6%,其余为氧;G能与NaHCO3溶液反应且含有苯环;核磁共振氢谱表明E、G分子中均有两种类型的氢原子,且E分子中两种类型的氢原子的个数比为1∶1.
已知乙二酸和乙二醇能发生如下反应:

(1)①、③ 的反应类型依次为 、 ;
(2)B的名称为: ;
E的结构简式为: ;
(3)写出下列化学方程式:
②
⑥
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
某兴趣小组进行“活泼金属与酸反应”的实验,
将5.4g的铝片投入500 mL 0.5 mol·L-1的硫酸溶液中,下
图为反应产生氢气速率与反应时间的关系图。
(1)关于图像的描述不正确的是 (填序号,下同)。
 ① a → b段产生H2加快可能是表面的氧化膜逐渐溶解,
① a → b段产生H2加快可能是表面的氧化膜逐渐溶解,
加快了反应速率
② b → c段产生H2较快可能是该反应放热,导致温度升高,加快了反应
③ c以后,产生H2速率逐渐下降可能是铝片趋于消耗完全
(2)其他条件不变,现换用500 mL 1 mol·L-1盐酸,产生氢气速率普遍较使用500 mL
0.5 mol·L-1硫酸的快,可能的原因是________。
①盐酸中c(H+)的浓度更大 ②Cl-有催化作用
③SO42-有催化作用 ④SO42-有阻化作用(使反应变慢)
⑤Al3+有催化作用
(3)要加快铝与硫酸溶液制H2的反应速率,小组成员提出一系列方案,比如:
①加入某种催化剂 ②加入蒸馏水
③将铝片换成铝粉 ④增加硫酸的浓度至18 mol/L
⑤ ⑥ 。
以上方案不合理的有 ;请你再补充两种合理方案,填入空白⑤⑥处。
查看答案和解析>>
科目:高中化学 来源: 题型:
已知某反应aA(g)+ bB(g) 2C(g)的各物质浓度数据如下:
2C(g)的各物质浓度数据如下:
| A | B | C | |
| 起始浓度(mol/L) | 3.0 | 1.0 | 0 |
| 2s末浓度(mol/L) | 1.8 | 0.6 | 0.8 |
据此可推算出上述方程式中各物质的化学计量数之比是( )
A. 9:3:4 B. 3:1:2
C. 2:1:3 D. 3:2:1
查看答案和解析>>
科目:高中化学 来源: 题型:
以下物质:(1) 甲烷;(2) 苯;(3) 聚乙烯;(4) 聚乙炔;(5) 2-丁炔;(6) 环己烷;(7) 邻二甲苯;(8) 苯乙烯.既能使KMnO4酸性溶液褪色,又能使溴水因发生化学反应而褪色的是( )
A.(3)(4)(5)(8) B.(4)(5)(7)(8)
C.(4)(5)(8) D.(3)(4)(5)(7)(8)
查看答案和解析>>
科目:高中化学 来源: 题型:
已知空气-锌电池的电极反应:
锌片:Zn-2OH--2e- = ZnO + H2O,石墨:1/2 O2+H2O +2e- = 2OH-
据次推断锌片是
A、负极,被氧化 B、负极,被还原 C、正极,被氧化 D、正极,被还原
查看答案和解析>>
科目:高中化学 来源: 题型:
下列实验能获得成功的是
A.乙烯通入Br2的CCl4溶液中制备CH2Br—CH2Br
B.苯和浓溴水用铁作催化剂制溴苯
C.CH4与Cl2在光照条件下制备纯净的CH3Cl
D.氯乙烷与NaOH溶液共热,在水解后的溶液中直接加入AgNO3溶液检验Cl-
查看答案和解析>>
科目:高中化学 来源: 题型:
A、B、C、D、E为五种元素的单质,其余为化合物。其中只有E为金属元素,五种元素的原子序数按B、D、C、A、E顺序依次增大,D、C元素在周期表中位置相邻,在一定条件下,B可以分别和A、C、D化合生成甲、乙、丙化合物,C和D化合可得丁。已知乙、丙每个分子中均含有10个电子,相互转化关系如图所示:
请回答下列问题:
(1)下面是周期表的一部分,请按A、C、E用元素符号填在相应的位置上。

(2)写出工业上制取A反应的离子方程式:___________________________。
(3)戊的分子式为________。B与D形成的原子个数比为2∶1的化合物中,D原子最外层为8电子结构,请写出该化合物的电子式:________________。
(4)A与丙常温下发生反应生成甲与单质D,该反应的化学方程式为_______________________________。
(5)8 g E在A中燃烧放出热量Q kJ,写出该反应的热化学方程式:________________________________(热量是常温下测定的)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com