
【题目】硫代硫酸钠(Na2S2O3)又名大苏打、海波,可用于照相业作定影剂,也可用于纸浆漂白作脱氯剂等。实验室常以硫化钠(Na2S)为原料制取Na2S2O3。
实验项目I:工业级硫化钠的纯化。
本实验对Na2S的纯度要求较高,利用图1所示的装置将工业级的Na2S提纯。
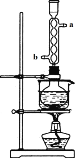
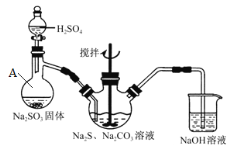
图1 图2
已知:Na2S常温下微溶于酒精,加热时溶解度迅速增大,杂质不溶于酒精。
提纯步骤依次为:
① 将已称量好的工业Na2S放入圆底烧瓶中,并加入一定质量的酒精和少量水;
② 按图1所示连接仪器,水浴加热;
冷凝管的作用是 。
向冷凝管中通入冷却水的方向是从 口进水(填“a”或“b”)。
③ 待烧瓶中固体不再减少时,停止加热,将烧瓶取下,趁热过滤,除去不溶物;
④ 将滤液转移至烧杯中,冷却结晶,过滤;
⑤ 将所得固体用少量 (填试剂名称)洗涤,干燥后得到Na2S·9H2O晶体。
实验项目II:硫代硫酸钠的制备。
制备步骤依次为:
① 称取一定质量的硫化钠晶体和碳酸钠固体,溶于水,转移至三颈瓶中;
② 按图2所示连接仪器,并在各仪器中加入相应的试剂,打开分液漏斗的活塞,使反应生成的气体较均匀地通入三颈瓶中,并用电磁搅拌器不断搅拌;
仪器A的名称为 。
写出三颈瓶中发生的反应的化学方程式: 。
③ 随着气体的通入,逐渐有浅黄色的硫析出,继续通入气体至溶液pH接近7,停止通入气体,取下三颈烧瓶,过滤;
实验过程中若未及时停止通入气体可能产生的后果为 。
④ 将滤液置于蒸发皿中加热,待 时,停止加热,冷却,过滤,即得Na2S2O3·5H2O晶体。
【答案】
②冷凝回流 b
⑤乙醇
②蒸馏烧瓶 Na2CO3+2Na2S+4SO2=3Na2S2O3+CO2
③Na2S2O3在酸性环境中不稳定,产率降低
④少量晶体析出时
【解析】
试题分析:② 根据装置图可知冷凝管的作用是冷凝回流,为充分冷却,冷凝水应低进高出,从冷凝管的b进水;⑤硫化钠常温下微溶于酒精,所以用乙醇洗涤,防止硫化钠损失;②根据图示仪器A的名称为蒸馏烧瓶;写出三颈瓶中Na2CO3、2Na2S、4SO2发生反应生成Na2S2O3,化学方程式为Na2CO3+2Na2S+4SO2=3Na2S2O3+CO2;③Na2S2O3在酸性环境中不稳定,实验过程中若未及时停止通入气体可能产生的后果为产率降低;④ 将滤液置于蒸发皿中加热,待少量晶体析出时时,停止加热,冷却,过滤,即得Na2S2O3·5H2O晶体。


 星级口算天天练系列答案
星级口算天天练系列答案 芒果教辅达标测试卷系列答案
芒果教辅达标测试卷系列答案科目:高中化学 来源: 题型:
【题目】
(1)用已称量的5.85gNaCl固体配制100mL 1.00mol/LNaCl溶液,所需的仪器为_______________.
(2)在9.5g某二价金属的氯化物中含有0.2molCl-,此氯化物的摩尔质量为___________,该金属元素的相对原子质量为___________。
(3)在氯化物ACl3中,A元素与氯元素的质量比为1∶3.94,则A的相对原子质量为___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向 0.1 mol/L 醋酸溶液中加水稀释,下列变化叙述错误的是( )
A. 溶液的 pH 逐渐增大 B. 溶液中的 c(OH-)逐渐减小
C. 醋酸的电离程度逐渐增大 D. 溶液的导电能力逐渐减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表是25℃时某些盐的浓度积常数和弱酸的电离平衡常数,下列说法正确的是( )
化学式 | AgCl | Ag2CrO4 | CH3COOH | HClO | H2CO3 |
Ksp或Ka | Ksp=1.8×10-10 | Ksp=2.0×10-12 | Ka=1.8×10-5 | Ka=3.0×10-8 | Ka1=4.1×10-7 Ka2=5.6×10-11 |
A.相同浓度CH3COONa和NaClO的混合液中,各离子浓度的大小关系是
c(Na+)>c(ClO-)>c(CH3COO-)>c(OH-)>c(H+)
B.碳酸钠溶液中滴加少量氯水的离子方程式H2O+2CO32-+Cl2=2HCO3-+Cl-+ClO-
C.向0.1mol/LCH3COOH溶液中滴加NaOH溶液至c(CH3COOH):c(CH3COO-)=9:5,此时溶液pH=5
D.向浓度均为1×10-3mol/L的KCl和K2CrO4混合液中滴加1×10-3mol/L的AgNO3溶液,CrO42-先形成沉淀
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知常温时Ksp(AgCl)=1.8×10-10,Ksp(AgI)=1.0×10-16,Ksp(Ag2CrO4)=1.1×10-12。下列说法中正确的是( )
A.由于Ksp(AgCl)>Ksp(AgI),所以AgI可以转化为AgCl
B.向Ag2CrO4溶液中加入固体K2CrO4,溶解平衡逆向移动,所以Ag2CrO4的Ksp减小
C.由于Ksp(Ag2CrO4)<Ksp(AgCl),所以沉淀AgCl容易转化为沉淀Ag2CrO4
D.常温下,AgCl饱和溶液中加入NaI,若要使溶液中开始转化为AgI,则NaI的浓度必不低于0.75×10-11 mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于石灰石和熟石灰用途的说法中,错误的是
A. 燃煤时加入石灰石,可减少硫氧化物的排放
B. 氯水中加入适量石灰石,可增强氯水的漂白性
C. 酸性土壤中加入适量的熟石灰,可以中和其酸性
D. 盐碱地(含较多NaCl、Na2CO3)中施用熟石灰,可降低土壤的碱性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某反应CH3OH(l)+NH3(g) = CH3NH2(g)+H2O(g)在高温度时才能自发进行,则该反应过程的△H、△S判断正确的是( )
A. △H>0 、△S<0 B. △H<0 、△S>0
C. △H<0 、△S<0 D. △H>0 、△S>0
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述正确的是
A.将30 mL 0.5 mol/L NaOH溶液加水稀释到500 mL,所得溶液的NaOH的浓度为0.3 mol/L
B.配制250 mL 1.0 mol/L H2SO4溶液,需要18 mol/L的浓H2SO4的体积约为13.9 mL
C.0.270 kg质量分数为10%的CuCl2溶液中Cl-的物质的量为0.2 mol
D.80 g NaOH溶于1 L水中所得的溶液的物质的量浓度为2 mol/L
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com