
| A. | 在同一条件下不同物质有不同的熵值,其体系的混乱程度越大,熵值越大 | |
| B. | 焓变是一个反应能否自发进行相关的因素,多数放热反应能自发进行 | |
| C. | 一个反应能否自发进行,与焓变和熵变的共同影响有关 | |
| D. | 自发进行的反应一定能迅速进行 |
分析 反应自发进行的判断依据为:△G=△H-T•△S,当反应自发进行时,△G<O,反应能否自发进行与焓变与熵变都有关系,以此解答该题.
解答 解:A.△S与物质的混乱度有关,体系的混乱程度越大,熵值越大,故A正确;
B.多数放热反应在一定温度下,△G<O,反应能自发进行,故B正确;
C.反应自发进行的判断依据为:△G=△H-T•△S,当反应自发进行时,△G<O,反应能否自发进行与焓变与熵变都有关系,故C正确;
D.△G<0反应自发进行,能自发进行,但反应速率不一定大,如金属的腐蚀等,故D错误;
故选D.
点评 本题考查化学反应进行方向的判断,为高频考点,侧重考查学生的分析能力,明确反应自发进行判断依据是解题关键,题目难度不大.


 探究与巩固河南科学技术出版社系列答案
探究与巩固河南科学技术出版社系列答案科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 阿伏加德罗常数个硫酸分子里含有4molO | |
| B. | CH4的摩尔质量为16g | |
| C. | lmolFe的质量为56g/mol | |
| D. | lmolNH3为18g |
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
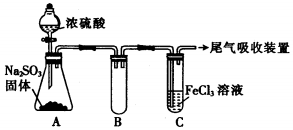
| 实验步骤(简述操作过程) | 预期现象和结论 |
| ① ② ③ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 原子半径:丁>丙>乙>甲 | |
| B. | 乙元素在周期表中的位置为第三周期第Ⅳ族 | |
| C. | 1molA与足量B完全反应共转移1mol电子 | |
| D. | 1.0mol•L-1E溶液中阴离子总的物质的量小于0.1mol |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 赤铁矿主要成分是 Fe2O3,Fe2O3是红棕色的,常用作红色油漆和涂料 | |
| B. | Fe3O4是黑色晶体,其中$\frac{1}{3}$的铁显+2 价,$\frac{2}{3}$的铁显+3 价 | |
| C. | FeO、Fe2O3 都不溶于水,但都能和盐酸反应生成相应的盐 | |
| D. | FeO 不稳定,在空气中加热迅速被氧化成 Fe2O3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 过量的铝与冷的浓硝酸 | B. | 过量的二氧化锰与浓盐酸 | ||
| C. | 过量的铜与浓硫酸 | D. | 过量的锌与18 mol/L硫酸 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com