
| A������Fe2O3��Ͷ���� |
| B������������������䣬����H2�������� |
| C������N2������������ѹǿ���� |
| D������N2����������������� |
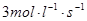 (3) 50% (4)33.3% (5)4:3
(3) 50% (4)33.3% (5)4:3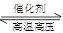 2NH3
2NH3


| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
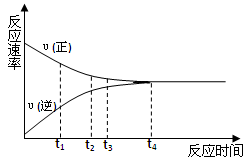
| A��t1ʱ�̣���(��)< ��(��) | B��t2ʱ�̣���(��)> ��(��) |
| C��t3ʱ�̣���(��)= ��(��) | D��t4ʱ�̣���(��)= ��(��) |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
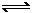 ?N2O4����Ӧ�в������������±���ʾ��
?N2O4����Ӧ�в������������±���ʾ��| ��Ӧʱ��/min | 0 | 10 | 20 | 30 | 40 | 50 |
| ������Է������� | 46 | 57 | 64 | 69 | 69 | 69 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
 C(g)��2D(g)����H<0����һ�������´ﵽƽ�⣬������ȷ����(����)
C(g)��2D(g)����H<0����һ�������´ﵽƽ�⣬������ȷ����(����)| A���٢� | B���� | C���� | D���ܢ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
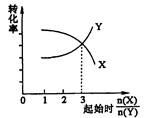
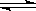 3Z B 3X��2Y
3Z B 3X��2Y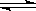 2Z
2Z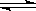 Z D 3X��Y
Z D 3X��Y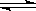 Z
Z�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ�������
 2SO3(g)����ʱ������SO3��Ũ��Ϊ0.9mol/L��O2�����ʵ���Ϊ2.1mol������ SO2��ת���ʣ��� O2����ʼŨ��(mol/L)���� SO2��ƽ����Ӧ����(mol/L�� min)
2SO3(g)����ʱ������SO3��Ũ��Ϊ0.9mol/L��O2�����ʵ���Ϊ2.1mol������ SO2��ת���ʣ��� O2����ʼŨ��(mol/L)���� SO2��ƽ����Ӧ����(mol/L�� min) �鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
 2NO2(g)��ϵ�У�n(NO)��ʱ��ı仯���±���
2NO2(g)��ϵ�У�n(NO)��ʱ��ı仯���±���| ʱ��(s) | 0 | 1 | 2 | 3 | 4 | 5 |
| n(NO)(mol) | 0.020 | 0.010 | 0.008 | 0.007 | 0.007 | 0.007 |
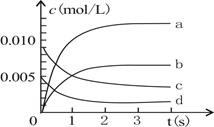
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
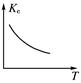
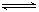 2NO2 ��ƽ
2NO2 ��ƽ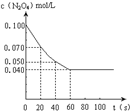
| T/ K | 323 | 373 |
| Kֵ | 0.022 | �� |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com