
下列各组离子在相应的条件下一定能大量共存的是
A.在碱性溶液中:HCO3-、K+、C1-、Na+
B.与铝粉反应放出氢气的无色溶液中:NO3-、K+、Na+、SO42-
C.在c(H+)/c(OH-)==1×1013的溶液中:NH4+、Br-、C1-、K+
D.通有SO2的溶液中: Ca2+、C1-、NO3-、A13+
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源:2015届安徽望江中学同步课时练(人教选修4)1.3化学反应热的计算(解析版) 题型:选择题
已知热化学方程式:SO2(g)+O2(g)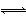 SO3(g) ΔH=-98.32 kJ·mol-1,在容器中充入2 mol SO2和1 mol O2,充分反应,最终放出的热量( )
SO3(g) ΔH=-98.32 kJ·mol-1,在容器中充入2 mol SO2和1 mol O2,充分反应,最终放出的热量( )
A.=196.64 kJB.=98.32 kJ C.<196.64 kJD.>196.64 kJ
查看答案和解析>>
科目:高中化学 来源:2015届四川省高三入学考试化学试卷(解析版) 题型:填空题
工业上利用天然气(主要成分是CH4)与H2O进行高温重整制备合成气(CO+H2),CO和H2在一定条件下能制备甲醛、甲醚等多种有机物。已知CH4、H2和CO的燃烧热(△H)分别为-890.3 kJ·mol-1、-285.8 kJ·mol-1和-283.0 kJ·mol-1;18.0 g水蒸气液化时的能量变化为44.0 kJ。
(1)写出甲烷与水蒸气在高温下反应制合成气的热化学方程式 。
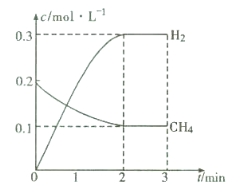
(2)在一定条件下,向体积固定为2 L的密闭容器中充人0.40mol CH4(g)和0.60mol H2O(g),测得CH4(g)和H2(g)的物质的量浓度随时间变化的曲线如图所示。3 min时改变条件,反应进行到4 min时,体系中各物质的物质的量如下表所示:
t/min | n(CH4)/mol | n(H2O)/mol | n(CO)/mol | n(H2)/mo1 |
4 | 0.18 | 0.38 | 0.22 | 0.66 |
则3~4min之间,平衡向 (填“正”或“逆”)反应方向移动,3min时改变的条件是 。
(3)已知温度、压强和碳水比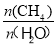 对该反应的影响如图所示。
对该反应的影响如图所示。
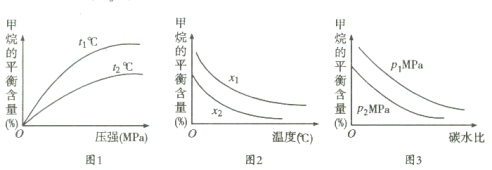
①图1中,两条曲线所示温度的关系:t1 t2(填“>”、“<”或“=”,下同)
②图2中,两条曲线所示碳水比的关系:x1 x2
③图3中,两条曲线所示压强的关系:p1 p2
(4)以天然气(假设杂质不参与反应)为原料的燃料电池示意图如图所示。
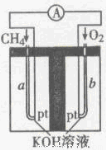
①放电时,正极的电极反应式为
②假设装置中盛装100.0 mL 3.0mol·L-1KOH溶液,放电时参与反应的氧气在标准状况下体积为8 960 mL。放电完毕后,电解质溶液中各离子浓度的大小关系为 。
查看答案和解析>>
科目:高中化学 来源:2015届四川省成都市高新区高三9月月考化学试卷(解析版) 题型:选择题
铁和氧化铁的混合物共a mol,加盐酸后固体全部溶解,共收集到b mol氢气,且向反应后的溶液中加入KSCN溶液不显红色,则原混合物中单质铁的物质的量为
A.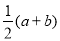 molB.
molB.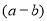 molC.
molC.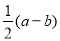 molD.
molD. 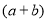 mol
mol
查看答案和解析>>
科目:高中化学 来源:2015届四川省成都市高新区高三9月月考化学试卷(解析版) 题型:选择题
已知25℃时有关物质的电离平衡常数:
弱酸 | CH3COOH | 苯酚 | H2CO3 |
电离平衡常数 | 1.75×l0–5 | 1.1×l0–10 | K1=4.4×l0–7 K2=4.7×l0–11 |
下列叙述错误的是
A.等物质的量浓度的各溶液pH关系为:
pH(C6H5ONa)>pH(Na2CO3)>pH(NaHCO3)>pH(CH3COONa)
B.向苯酚钠溶液中通入少量CO2气体反应为:C6H5O– +H2O + CO2 →C6H5OH +HCO3-
C.等物质的量浓度的苯酚稀溶液与 NaOH稀溶液等体积混合后溶液中:
c(Na+)>c(C6H5O–)>c(OH–)>c(H+)
D.NaHCO3和Na2CO3混合液中,一定有c(Na+)+ c(H+)=c(OH–)+ c(HCO3–) +2c(CO32–)
查看答案和解析>>
科目:高中化学 来源:2015届四川省成都市高新区高三9月月考化学试卷(解析版) 题型:选择题
下列化学用语正确的是
A.乙烯的分子式:CH2===CH2
B.次氯酸分子的结构式:H—O—Cl
C.羟基的电子式:
D.以铁作阳极电解时,阳极的电极反应式:Fe-3e-===Fe3+
查看答案和解析>>
科目:高中化学 来源:2015届四川省成都市2012级临诊考试化学试卷(解析版) 题型:填空题
(12分)某工业废水肿含有一定量的Cr2O72-和CrO42-,现
取样该工业废水,检测其中铬的含量。
步骤I:取25. 00 mL废水,加入适后稀硫酸酸化。
步骤Ⅱ:加入过量的碘化钾溶液,滴人几滴指示剂。
步骤Ⅲ: 用o .1000 mol·L-1Na2S2O3溶液滴定(I2+2Na2 S2O3= 2NaI+Na2S4O6)
达到终点时消耗溶液24. 00 mL。
步骤Ⅳ:将上述反应后的溶液进行如下处理:反应后废液
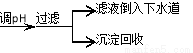
回答下列问题
(1)步骤I加入稀硫酸酸化的目的是 ;
(2)步骤Ⅱ中发生如下反应,请完善并配平离子方程式

该步骤中所加指示剂是 ;
(3)步骤Ⅲ判断滴定达到终点的现象是__ __。
(4)步骤Ⅳ在生产生活中的意义是____ (任答一条);
(5)计算工业废水中铬元素的含量是 mg/L.
查看答案和解析>>
科目:高中化学 来源:2015届四川省成都市2012级临诊考试化学试卷(解析版) 题型:选择题
金属M和N可构成如图所示的装置.下列分析正确的是
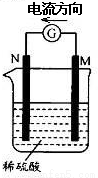
A.金属活泼性N>M
B.M逐渐溶解
C.负极反应为2H++2e- =H2↑
D.SO42-向M极定向移动
查看答案和解析>>
科目:高中化学 来源:2015届内蒙古赤峰市元宝山区高二上学期期末化学试卷(解析版) 题型:选择题
反应A+B→C(△H<0)分两步进行:①A+B→X(△H>0),②X→C(△H<0)。下列示意图中,能正确表示总反应过程中能量变化的是( )
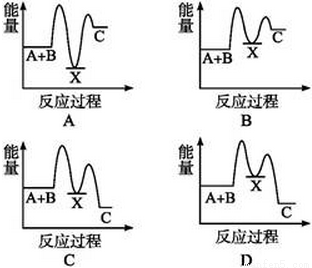
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com