
【题目】(1)检测人的血液中葡萄糖(简称血糖,相对分子质量为180)的含量,参考指标常以两种计量单位表示,即“mmol/L”和“mg/dL”(1L=10dL)。以“mmol/L”表示时,人的血糖正常值为3.61~6.11mmol/L之间。如果以“mg/dL”表示,若某人的血糖检测结果是92mg/dL,他的血糖正常吗_____________(填正常或不正常)
(2)某工厂的工业废水中含有大量的FeSO4、较多的Cu2+和少量的Na+。为了减少污染并变废为宝,工厂计划从该废水中回收硫酸亚铁和金属铜。请根据流程图,在方框和括号内填写物质名称(或主要成分的化学式)或操作方法,完成回收硫酸亚铁和铜的简单实验方案______。

(3)如图,验证牺牲阳极的阴极保护法时,往Fe电极区滴入2滴黄色K3[Fe(CN)6](铁氰化钾)溶液,观察烧杯内溶液颜色有无变化.请回答:

①.电压表指针有何变化_________原因是_______________________
②.请写出Fe2+与[Fe(CN)6]3反应的离子方程式:____________________
(4)K3[Fe(C2O4)3]·3H2O(三草酸合铁酸钾)为亮绿色晶体,可用于晒制蓝图。晒制蓝图时,用K3[Fe(C2O4)3]·3H2O作感光剂,以K3[Fe(CN)6]溶液为显色剂。其光解反应的化学方程式为:2K3[Fe(C2O4)3]![]() 2FeC2O4+3K2C2O4+2CO2↑;显色反应的化学方程式为__________________。
2FeC2O4+3K2C2O4+2CO2↑;显色反应的化学方程式为__________________。
【答案】正常  发生偏转 因为有电流产生 3Fe2++2[Fe(CN)6]3=Fe3[Fe(CN)6]2↓ 3FeC2O4+2K3[Fe(CN)6]
发生偏转 因为有电流产生 3Fe2++2[Fe(CN)6]3=Fe3[Fe(CN)6]2↓ 3FeC2O4+2K3[Fe(CN)6]![]() Fe3[Fe(CN)6]2+3K2C2O4
Fe3[Fe(CN)6]2+3K2C2O4
【解析】
(1)根据物质的量浓度概念以及物质的量和质量之间的关系解答;
(2)依据本题要求,应用如图所示流程图,欲回收硫酸亚铁和铜,结合图中提示分析可得结论;
(3)该装置是原电池,锌易失电子作负极,铁作正极,亚铁离子和铁氰化钾溶液能产生蓝色沉淀,据此解答;
(4)发生显色反应的是Fe2+和K3[Fe(CN)6]反应生成Fe3[Fe(CN)6]2。
(1)1mmol=10-3mol、1g=103mg、1L=10dL,故3.61mmol糖质量为:3.61![]() -3 mol×180mg/mol=649.80mg,用 mg/dL表示血糖浓度为:
-3 mol×180mg/mol=649.80mg,用 mg/dL表示血糖浓度为:![]() =64.98mg/dL;
=64.98mg/dL;
6.11mmol,血糖的质量为:6.11×10-3mol×180mg/mol=1099.80mg,用 mg/dL表示血糖浓度为:![]() = 109.98mg/dL,故血糖正常取值范围是64.98109.98mg/dL,由于此人血糖在这个范围之内,所以正常;
= 109.98mg/dL,故血糖正常取值范围是64.98109.98mg/dL,由于此人血糖在这个范围之内,所以正常;
本题答案为:正常
(2)废水中加入过量的铁粉,过滤,得到固体为铁和铜的混合物,滤液为硫酸亚铁。再往得到的固体混合物中加入稀硫酸,铁溶解,过滤后得到固体铜,此时滤液为硫酸亚铁;对所得滤液硫酸亚铁,进行蒸发结晶操作,得到带7个结晶水的硫酸亚铁晶体;
本题答案为: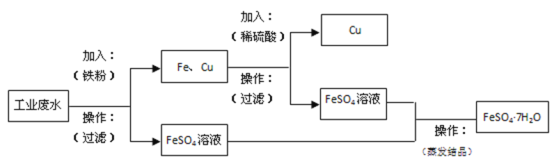
(3)该装置是原电池,锌易失电子作负极,铁作正极,故电压表指针发生偏转,亚铁离子和铁氰化钾溶液能产生蓝色沉淀,离子方程式为:3Fe2++2[Fe(CN)6]3=Fe3[Fe(CN)6]2↓;
本题答案为:发生偏转,因为有电流产生;3Fe2++2[Fe(CN)6]3=Fe3[Fe(CN)6]2↓。
(4)发生显色反应的是Fe2+和K3[Fe(CN)6]反应生成Fe3[Fe(CN)6]2。化学方程式为:3FeC2O4+2K3[Fe(CN)6]![]() Fe3[Fe(CN)6]2+3K2C2O4;
Fe3[Fe(CN)6]2+3K2C2O4;
本题答案为:3FeC2O4+2K3[Fe(CN)6]![]() Fe3[Fe(CN)6]2+3K2C2O4。
Fe3[Fe(CN)6]2+3K2C2O4。


 永乾教育寒假作业快乐假期延边人民出版社系列答案
永乾教育寒假作业快乐假期延边人民出版社系列答案科目:高中化学 来源: 题型:
【题目】X、Y、Z、W四种元素在元素周期表中序数逐渐增大。X为非金属元素,且X、W同主族,Y、Z为同周期的相邻元素。W原子的质子数等于Y、Z原子最外层电子数之和。Y的氢化物分子中有3个共价键。Z原子最外层电子数是次外层电子数的3倍。试推断:
(1)Z的元素原子结构示意图是:___________;
(2)由X、Y、Z所形成的离子化合物是_________,它与W的最高价氧化物对应水化物的溶液加热时反应的离子方程式是___________;
(3)Y的单质的结构式为_______,其中的化学键属于___________键(填“离子”或“共价”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于氢键,下列说法正确的是( )
A. 每一个水分子中含有两个氢键 B. 分子间形成的氢键使物质的熔点和沸点升高
C. 冰、液氨和溴苯中都存在氢键 D. H2O是一种非常稳定的化合物,这是由于存在氢键的缘故
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】完成下列各小题。
Ⅰ.按要求书写:
(1)最简单的炔烃的电子式__________________;
(2)苯甲醛发生银镜反应的离子方程式:__________________________
(3)某芳香烃的相对分子质量为102,若该分子内所有原子均在同一平面内,则其结构简式为_______________;
(4)两个乳酸分子间形成六元环酯的化学方程式:___________________ 。
Ⅱ.按要求书写下列化学方程式:
(1)2一丁炔与足量溴的四氯化碳溶液反应:__________________ ;
(2)甲苯与浓硝酸、浓硫酸混合后在100℃时发生反应:____________ ;
(3)1,2一二溴丙烷与氢氧化钠乙醇溶液共热充分反应:_____________ 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学兴趣小组为探究元素性质的递变规律,设计了如下系列实验。

I.将 NaOH溶液与 NH4Cl 溶液混合生成 NH3·H2O,从而验证 NaOH的碱性大于 NH3·H2O,继而可以验证 Na 的金属性大于 N,你认为此设计是否合理? 并说明理由:_____________________。
II.根据下图所示装置图回答以下问题。
(1)利用如图装置可以验证元素的非金属性的变化规律。图中 A 装置名称是____________,干燥管 D的作用是______________。
(2)实验室中现有药品Na2S、KMnO4、MnO2、浓盐酸,请从中选择合适药品设计实验验证氯的非金属性大于硫,烧瓶中发生反应的离子方程式为_____________________。
(3)若要用此装置证明酸性: HNO3>H2CO3>H2SiO3 进而证明非金属性: N>C>Si,从以下所 给物质中选出甲同学设计的实验所用到物质:
①稀 HNO3溶液 ②稀盐酸 ③碳酸钙 ④Na2SiO3溶液 ⑤SiO2
装置 A、C中所选试剂分别为______________(填序号);能说明酸性 H2CO3>H2SiO3的实验现象是________________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某研究性学习小组为确定某蜡状有机物A的结构和性质,他们拟用传统实验的手段与现代技术相结合的方法进行探究。请你参与探究过程:
Ⅰ.实验式的确定
(1)取样品A进行燃烧法测定。发现燃烧后只生成CO2和H2O,某次燃烧后,经换算得到了0.125 mol CO2和2.7g H2O。据此得出的结论是_______;
(2)另一实验中,取3.4 g蜡状A在3.36 L(标准状况下,下同)氧气中完全燃烧,两者均恰好完全反应,生成2.8 L CO2和液态水。通过计算确定A的实验式;__________
Ⅱ.结构式确定(经测定A的相对分子质量不超过140)
(3)取少量样品熔化,加入钠有氢气放出,说明A分子中含有_______基;
(4)进行核磁共振,发现只有两个特征峰,且面积比为8:4,再做红外光谱,发现与乙醇一样透过率在同一处波数被吸收。图谱如下:

则A的结构简式为_______;
Ⅲ.性质探究
(5)A与浓氢溴酸混合加热发生反应的化学方程式为_______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】“高钙牛奶”、“含氟牙膏”、“铁强化酱油”等商品名称中的“钙”、“氟”、“铁”指 的是( )
A. 单质 B. 氧化物 C. 分子 D. 元素
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图中A~G均为中学化学中常见的物质,它们之间有如下转化关系。其中A是天然气的主要成分,B是一种能使带火星木条复燃的气体,C是一种能使澄清石灰石变浑浊的气体,E是一种淡黄色粉末状固体。(反应过程中某些产物已略去)
请回答问题:

(1)A的电子式为_______________________________。
(2)E的化学式为_______________________________。
(3)写出C转化为F的化学方程式_________________________________________。
(4)写出G溶液中通入过量C的离子方程式_________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com