
| A、NH4Cl |
| B、KCl溶液 |
| C、NaNO3 |
| D、CH3COONa |


 口算题卡北京妇女儿童出版社系列答案
口算题卡北京妇女儿童出版社系列答案科目:高中化学 来源: 题型:
| A、等质量的铝分别投入过量的稀盐酸和NaOH溶液中,反应生成的气体在相同条件下体积相等 |
| B、金属单质与水反应都生成对应的碱和氢气 |
| C、活泼的金属或较活泼的金属都能与酸反应,但不能与碱反应 |
| D、由于钠比较活泼,所以它能从溶液中置换出金属活动顺序表中钠后面的金属 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
A、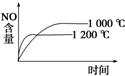 |
B、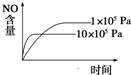 |
C、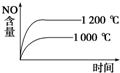 |
D、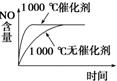 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、NH4NO3 溶于水虽然吸热,但其溶于水是自发过程 |
| B、加热液体(温度高于沸点)会自发转变成气体,可用熵变解释 |
| C、同温同压下,H2(g)+Cl2(g)?2HCl(g)在光照和点燃条件下的△H不同 |
| D、要正确判断化学反应能否自发进行,要综合考虑反应的△H和△S |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、2Fe3++SO2+2H2O═2Fe2++SO42-+4H+ |
| B、H2O2+H2SO4═SO2↑+O2↑+2H2O |
| C、I2+SO2+2H2O═H2SO4+2HI |
| D、2Fe3+2I-═2Fe2++I2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、1mol稀H2SO4与足量NaOH溶液反应 |
| B、稀盐酸与氨水反应生成1 mol H2O |
| C、稀NaOH与95%浓硫酸反应生成1 mol水 |
| D、稀盐酸与稀Ba(OH)2溶液反应生成1 mol水 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、道尔顿提出原子学说 |
| B、汤姆生发现电子,并提出原子结构轨道模型 |
| C、舍勒发现了氯气 |
| D、卢瑟福根据α粒子散射现象,提出了带核的原子结构模型 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com