
科目:高中化学 来源:不详 题型:计算题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题

| A.该试剂的物质的量浓度为9.2 mol·L—1 |
| B.该硫酸50 mL与足量的铜反应可得到标准状况下SO2 10.3 L |
| C.配制200 mL 4.6 mol·L—1的稀硫酸需取该硫酸50 mL |
| D.该硫酸与等体积的水混合所得溶液的质量分数小于49% |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
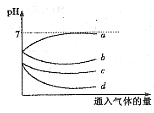
| A.曲线b表示向H2S水溶液中通入O2 |
| B.曲线b表示向SO2水溶液中通入O2 |
| C.曲线c表示向H2S水溶液中通入Cl2 |
| D.曲线d表示向SO2水溶液中通入Cl2 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.氧化剂 | B.还原剂 | C.催化剂 | D.吸附剂 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
| A.沸点高、难挥发 | B.酸性 | C.吸水性 | D.脱水性 E.强氧化性 |
| 用途或现象 | 体现浓硫酸的性质 |
( 1)浓硫酸使胆矾变成白色 1)浓硫酸使胆矾变成白色 | |
| (2)浓硫酸使蔗糖变”黑面包” | |
| (3)浓硫酸与铜片共热 | |
| (4)浓硫酸的木炭共热产生气体 | |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题

 若把①试管中的生成物倒人水中发现溶液变蓝
若把①试管中的生成物倒人水中发现溶液变蓝查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com