
用50mL0.50mol/L盐酸与50mL0.55mol/LNaOH溶液在如图所示的装置中进行中和反应。通过测定反应过程中所放出的热量可计算中和热。回答下列问题:

(1)从实验装置上看,图中尚缺少的一种玻璃仪器是 。
(2)烧杯间填满碎纸条的作用是 。
(3)环形玻璃搅拌棒能否用环形铁质搅拌棒代替 (填“能”或者“否”)其原因是 。
(4)大烧杯上如不盖硬纸板,求得的中和热数值 (填“偏大、偏小、无影响”)。
(5)如果用60mL0.50mol/L盐酸与50mL0.55mol/LNaOH溶液进行反应,与上述实验相比,所放出的热量 (填“相等、不相等”),所求中和热 (填“相等、不相等”),简述理由 。
 能考试期末冲刺卷系列答案
能考试期末冲刺卷系列答案科目:高中化学 来源:2016届山东省齐鲁教科研协作体19所高三上学期第一次联考化学试卷(解析版) 题型:选择题
铝对生物有毒害作用,尤其对人体的毒害更加严重。下列说法不正确的是
A.不吃或少吃使用了含铝食品添加剂的食物
B.不能用铝制器皿长期存放酸性或碱性食品
C.杜绝铝制品在生产生活中的应用
D.铝不属于重金属,它使人体中毒的原理与铅不同
查看答案和解析>>
科目:高中化学 来源:2016届安徽省江南十校新高三摸底联考化学试卷(解析版) 题型:选择题
设NA为阿伏伽德罗常数,下列说法不正确的是
A.含1 mol FeCl3的饱和溶液最多可形成胶体粒子数为NA
B.4.6 g Na与稀盐酸反应,转移电子数一定为0.2NA
C.10.6 g Na2 C03晶体中含CO32一数目为0.1 NA
D.常温下,22 g CO2含碳氧双键数目为NA
查看答案和解析>>
科目:高中化学 来源:2015-2016学年河北省高二上学期第一次月考化学试卷(解析版) 题型:填空题
(20分)按下图所示装置进行实验,并回答下列问题:
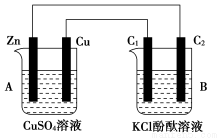
(1)判断装置的名称:A池为 ,B池为 。
(2)锌极为____极,电极反应式为 ;铜极电极反应式为 ;石墨棒C1为____极,电极反应式为 ;石墨棒C2附近的实验现象为___ _____。
(3)当C2极析出224 mL气体(标准状况下)时,锌质量 (填增加或减少),为 g;CuSO4溶液的质量 (填增加或减少),为 g。
查看答案和解析>>
科目:高中化学 来源:2016届天津一中高三零月考化学试卷(解析版) 题型:选择题
X﹑Y﹑Z﹑M是元素周期表中前20号元素,其原子序数依次增大,且X﹑Y﹑Z相邻。X 的核电荷数是Y 的核外电子数的一半,Y与M可形成化合物M2Y。则下列说法正确的是
A.还原性: X的氢化物﹥Y的氢化物﹥Z的氢化物
B.简单离子的半径:M的离子>Z的离子 >Y的离子>X的离子
C.YX2﹑M2Y都含有极性键
D.Z元素的最高价氧化物的水化物的化学式为HZO4
查看答案和解析>>
科目:高中化学 来源:2016届湖南省衡阳市高三上学期第一次月考化学试卷(解析版) 题型:选择题
某同学欲配制符合下列条件的溶液,其中可能实现的是
A.只含0.1 mol Na+、0.2 mol Mg2+、0.1 mol Cl-和0.1 mol NO3-的溶液
B.只含0.1 mol NH4+、0.1 mol Ca2+、0.1 mol CO32-和0.1 mol Cl-的溶液
C.为了通过测定pH的大小,达到比较HCl和CH3COOH酸性强弱的目的,分别配制100 mL 0.1 mol/L的NaCl溶液和CH3COONa溶液
D.仅用1 000 mL的容量瓶、烧杯、玻璃棒、量筒、58.5 g NaCl固体和水配制1 L 1 mol/L的NaCl溶液
查看答案和解析>>
科目:高中化学 来源:2015-2016学年吉林省高一入学摸底化学试卷(解析版) 题型:填空题
W、X、Y和Z都是周期表中前20号元素,已知:
①W的阳离子和Y的阴离子具有相同的核外电子排布,且能形成组成为WY的化合物;
②Y和Z属同族元素,它们能形成两种常见化合物;
③X和Z属同一周期元素,它们能形成两种气态化合物;
④W和X能形成组成为WX2的化合物;
⑤X和Y不在同一周期,它们能形成组成为XY2的化合物。
请回答:
(1)W元素是______;Z元素是________。
(2)化合物WY和WX2的化学式分别是____________和 ____________。
(3)Y和Z形成的两种常见化合物的分子式是________和________。
(4)写出X和Z形成的一种气态化合物跟WZ反应的化学方程式:___________
查看答案和解析>>
科目:高中化学 来源:2016届四川省高三9月月考化学试卷(解析版) 题型:选择题
已知反应10AgF+5Cl2+5H2O═9AgCl+AgClO3+10HF+O2,则有1molO2生成时反应所转移的电子总数为
A.4mol B.9mol C.10mol D.5mol
查看答案和解析>>
科目:高中化学 来源:2015-2016学年辽宁葫芦岛一中高二上期初考试化学试卷 (解析版) 题型:填空题
(15分)下表是元素周期表的一部分,针对a~k十一种元素回答下列问题(请用具体化学式回答,否则不给分):
周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA |
2 | a | c | d | e | f | g | |
3 | b | h | i | j | k |
(1)这些元素中非金属性最强的单质是 ,最高价氧化物对应水化物酸性最强的是 ,最高价氧化物对应水化物碱性最强的是 。
(2)表中k的氢化物的化学式为 ,它的还原性比j的氢化物还原性 (填“强”或“弱”),它水溶液的酸性比j的氢化物水溶液的酸性 (填“强”或“弱”)。
(3)e单质为 ,其结构式为 。
(4)用电子式表示h与k构成化合物的形成过程
(5)写出i的氧化物与强碱溶液反应的离子方程式
(6)H2和e的单质化合的反应是可逆反应,且该反应正方向放热。将等物质的量的H2、e的单质充入一恒容密闭容器中,在适当条件下反应。下列说法正确的是 (填写选项)。
A.升高温度,不论正反应方向还是逆反应方向速率都加快
B.向上述容器中充入适量Ar气可加快反应速率
C.反应过程中,e的单质的体积分数始终为50%
D.反应器内压强不随时间变化而变化,说明反应到达平衡
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com