
| 状态 条件 | 起始时各物质的物质的量(mol) | 平衡时NH3的物质的量(mol) | |||
| 编号 | x(N2) | y(H2) | z(NH3) | ||
| 恒压 | (1) | 1 | 3 | 0 | a |
| (2) | 3 | 0 | |||
| (3) | 0.2 | 0.5a | |||
| x、y、z取值必须满足的一般条件: | |||||
| 恒容 | (4) | 1 | 3 | 0 | b |
| (5) | 0 | 0 | b | ||
| (6) | 2.25 | b | |||
| x、y、z取值必须满足的一般条件(一个只含x、z,另一个只含y、z): | |||||
| a与b的关系是:a | |||||
| 恒压 | (2) | 9 | 3a | ||
| (3) | 0.4 | 1.2 | |||
| y=3x(x≥0);z≥0(x、y、z不同时为0) | |||||
| 恒容 | (5) | 2 | |||
| (6) | 0.75 | 0.5 | |||
| 2x+z=2;2y+3z=6. | |||||
| > | |||||


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
| A、铜作阳极,铁制品作阴极,溶液中含Fe2+ |
| B、铜作阴极,铁制品作阳极,溶液中含Cu2+ |
| C、铜作阴极,铁制品作阳极,溶液中含Fe3+ |
| D、铜作阳极,铁制品作阴极,溶液中含Cu2+ |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| 催化剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、3.36L |
| B、6.72L |
| C、5.60L |
| D、大于5.60L,小于6.72L |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、为了防止铁生锈,在其表面涂一层防锈油漆 |
| B、为防止火灾,在面粉厂、加油站等场所要严禁烟火 |
| C、为加快KClO3的分解速率,加入MnO2 |
| D、为加快H2O2的分解速率,把反应容器放到冷水中冷却 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A | B | C | D | |
| 实验 | 用CCl4提取溴水中的Br2 | 除去乙醇中的苯酚 | 从KI和I2的固体混合物中回收I2 | 配制1000mL0.1000mol?L-1K2Cr2O2溶液 |
| 装置或仪器 |  | 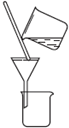 | 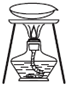 | 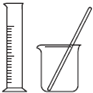 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com