
| A、3.36L |
| B、6.72L |
| C、5.60L |
| D、大于5.60L,小于6.72L |


科目:高中化学 来源: 题型:
| A、①② | B、①②④ |
| C、①②⑤ | D、③④⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:
 电解原理在化学工业中有广泛应用.如图表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连.X、Y都是惰性电极,a是饱和NaCl溶液,实验开始时,同时在两边各滴入几滴酚酞试液,下列选项错误的( )
电解原理在化学工业中有广泛应用.如图表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连.X、Y都是惰性电极,a是饱和NaCl溶液,实验开始时,同时在两边各滴入几滴酚酞试液,下列选项错误的( )| A、Y电极上的电极反应式为2Cl--2e-=Cl2↑.检验该电极反应产物的方法是把湿润的碘化钾淀粉试纸放在Y电极附近,试纸变蓝色 | ||||
B、电解池中X极上的电极反应式为2H2O
| ||||
| C、如要用电解方法精炼粗铜,电解液a换用CuSO4溶液,则X电极的材料是精铜 | ||||
| D、若想用电解实验制得白色纯净的Fe(OH)2沉淀,a仍是饱和NaCl溶液,往U形管添加完饱和NaCl溶液后需加入少量苯,苯的作用是防止生成的Fe(OH)2被空气氧化 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 状态 条件 | 起始时各物质的物质的量(mol) | 平衡时NH3的物质的量(mol) | |||
| 编号 | x(N2) | y(H2) | z(NH3) | ||
| 恒压 | (1) | 1 | 3 | 0 | a |
| (2) | 3 | 0 | |||
| (3) | 0.2 | 0.5a | |||
| x、y、z取值必须满足的一般条件: | |||||
| 恒容 | (4) | 1 | 3 | 0 | b |
| (5) | 0 | 0 | b | ||
| (6) | 2.25 | b | |||
| x、y、z取值必须满足的一般条件(一个只含x、z,另一个只含y、z): | |||||
| a与b的关系是:a | |||||
查看答案和解析>>
科目:高中化学 来源: 题型:
A、Cu
| ||||
B、Cu
| ||||
C、Cu
| ||||
D、Cu
|
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:

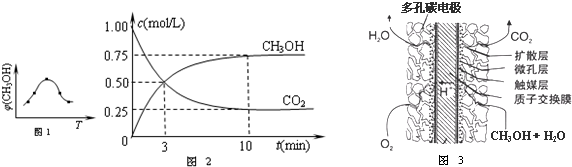
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、AgNO3溶液 |
| B、KMnO4溶液 |
| C、稀氨水 |
| D、NaOH溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:
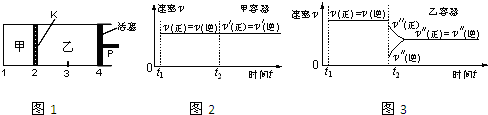
| A、保持温度和活塞位置不变,在甲中再加入1 mol A和2 mol B,达到新的平衡后,甲中C的浓度是乙中C的浓度的2倍 |
| B、保持活塞位置不变,升高温度,达到新的平衡后,甲、乙中B的体积分数均增大 |
| C、保持温度不变,移动活塞P,使乙的容积和甲相等,达到新的平衡后,乙中C的体积分数是甲中C的体积分数的2倍 |
| D、保持温度和乙中的压强不变,t2时分别向甲、乙中加入等质量的氦气后,甲、乙中反应速率变化情况分别如图2和图3所示(t1前的反应速率变化已省略) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com