
用实验确定某酸HA是弱电解质。两同学的方案是:
甲:① 称取一定量的HA的配制0.1mol/L的溶液100mL;②用pH试纸测出该溶液的pH值,即可证明HA是弱电解质。
乙:① 用已知物质的量浓度的HA溶液、盐酸,分别配制pH=1的两种酸溶液各100mL;
② 分别取这两种溶液各10mL,加水稀释为100mL;
③ 各取相同体积的两种稀释液装入两个试管,同时加入纯度相同的锌粒,观察现象,即可证明HA是弱电解质。
(1)在两个方案的第①步中,都用到的定量仪器是 。
(2)甲方案中,说明HA是弱电解质的理由是测得溶液的pH 1(选填“>”、“<”、“=”)。
乙方案中,说明HA是弱电解质的现象是 (填字母序号,多选倒扣分)。
a.装HCl的试管中放出H2的速率快;
b.装HA溶液的试管中入出H2的速率快;
c.两个试管中产生气体速率一样快。
(3)请你再提出一个合理而比较容易进行的方案(药品可任取),作简明扼要表述。
。
(1)100ml容量瓶
(2)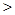 b
b
(3)配制NaA溶液,测其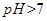 证明HA是弱电解质
证明HA是弱电解质
【解析】
试题分析:(1)在两个方案的第①步中都要配置溶液,需要使用的定量仪器是100ml容量瓶;(2)甲方案中,由于弱电解质只是部分电离,所以当HA是弱电解质时,其pH>1,乙方案中由于pH=1,所以在与纯度相同的锌粒时,由于弱电解质的电离,所以c(H+)较大,所以放出H2的速率快,故选b;(3)HA是弱电解质,其强碱盐的PH大于7,所以可以采用以下方案:配制NaA溶液,测其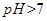 证明HA是弱电解质。
证明HA是弱电解质。
考点:弱电解质、盐类水解
点评:该题考查了弱电解质、盐类水解,是高考考查的重点,但是该题比较容易。


 亮点激活精编提优100分大试卷系列答案
亮点激活精编提优100分大试卷系列答案科目:高中化学 来源: 题型:阅读理解
 甲、乙两位同学设计用实验确定某酸HA是弱电解质,存在电离平衡,且改变条件平衡发生移动.实验方案如下:
甲、乙两位同学设计用实验确定某酸HA是弱电解质,存在电离平衡,且改变条件平衡发生移动.实验方案如下:| 1 | 25 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com