
【题目】从煤和石油中可以提炼出化工原料A和H。已知A是石油裂解气的主要产物之一,其产量是衡量一个国家石油化工发展水平的标志。H是一种比水轻的油状液体,H仅由碳氢两种元素组成,H不能使酸性KMnO4溶液褪色,其碳元素与氢元素的质量比为12:l,H的相对分子质量为78。下列是有机物A~G之间的转化关系:

请回答下列问题:
(1)D中所含官能团的名称是_________________;
(2)写出反应③的化学方程式_______________________________________;
(3)G是一种高分子化合物,可以用来制造农用薄膜材料等,其结构简式__________;
(4)在体育竞技比赛中,当运动员肌肉挫伤或扭伤时,随队医生立即对准其受伤部位喷射物质F(沸点12.27℃)进行应急处理。写出由A制备F的化学方程式:___________;
(5)下列关于B的一种同系物甲醇的说法不正确的是___________(填字母)。
a.甲醇的结构简式为CH3OH,官能团为—OH
b.甲醇完全燃烧后的产物为CO2和H2O
c.B与甲醇都极易溶于水,是因为它们都能与水分子间形成氢键
d.甲醇与钠反应可以产生氢气,所以甲醇显酸性
(6)等质量的A、H完全燃烧时消耗O2的物质的量_______(填“A>H、A<H或A=H”)。
【答案】 羧基 2CH3CH2OH+O2![]() 2CH3CHO+2H2O
2CH3CHO+2H2O ![]() CH2=CH2 + HCl
CH2=CH2 + HCl ![]() CH3CH2Cl d A>H
CH3CH2Cl d A>H
【解析】
从煤和石油中可以提炼出化工原料A和H。已知A是石油裂解气的主要产物之一,其产量是衡量一个国家石油化工发展水平的标志,A是乙烯。乙烯和氯化氢发生加成反应生成F是CH3CH2Cl。乙烯和水发生加成反应生成B是乙醇,乙醇发生催化氧化生成C是乙醛,乙醇被酸性高锰酸钾溶液氧化生成D是乙酸,乙酸和乙醇发生酯化反应生成E是乙酸乙酯。H是一种比水轻的油状液体,H仅由碳氢两种元素组成,H不能使酸性KMnO4溶液褪色,其碳元素与氢元素的质量比为12:l,H的相对分子质量为78,则含有的碳原子个数是![]() ,氢原子个数是
,氢原子个数是![]() ,因此H是苯,据此解答。
,因此H是苯,据此解答。
根据以上分析可知A是CH2=CH2,B是CH3CH2OH,C是CH3CHO,D是CH3COOH,E是CH3COOC2H5,F是CH3CH2Cl。则
(1)D是乙酸,其中所含官能团的名称是羧基;
(2)反应③是乙醇的催化氧化,化学方程式为2CH3CH2OH+O2![]() 2CH3CHO+2H2O;
2CH3CHO+2H2O;
(3)G是一种高分子化合物,可以用来制造农用薄膜材料等,因此G是聚乙烯,其结构简式为![]() ;
;
(4)乙烯和氯化氢发生加成反应生成氯乙烷,反应的化学方程式为CH2=CH2 + HCl ![]() CH3CH2Cl;
CH3CH2Cl;
(5)a.甲醇的结构简式为CH3OH,官能团为-OH,a正确;
b.甲醇完全燃烧后的产物为CO2和H2O,b正确;
c.B与甲醇都极易溶于水,是因为它们都能与水分子间形成氢键,c正确;
d.甲醇含有羟基,与钠反应可以产生氢气,甲醇是非电解质,不显酸性,d错误。
答案选d。
(6)乙烯分子中氢元素含量高于苯中氢元素含量,含氢量越高,消耗的氧气越多,则等质量的A、H完全燃烧时消耗O2的物质的量A>H。


 提分百分百检测卷单元期末测试卷系列答案
提分百分百检测卷单元期末测试卷系列答案科目:高中化学 来源: 题型:
【题目】甲、乙、丙、丁分别为A、B、C、D四种短周期元素的最高价氧化物对应的水化物,已知0.1mol·L-1甲、丙、丁溶液的pH与A、C、D的原子序数关系如图所示(lg2=0.3),且常温下甲、丙、丁均可与乙反应。下列说法正确的是

A. 原子半径:A<B<C<D
B. A、B分别与D形成的化合物均为离子化合物
C. B、C的简单离子都会影响水的电离平衡
D. 乙在浓氨水中能溶解
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】可逆反应:A+3B![]() 2C+2D在4种不同的情况下的反应速率分别为
2C+2D在4种不同的情况下的反应速率分别为
①v(A )=0.15mol/(L·s) ②v(B )=0.6mol/(L·s) ③v(C )=0.4mol/(L·s) ④v(D )=0.45mol/(L·s)
该反应进行速率最快的是
A. .① B. ②和③ C. ④ D. ①和④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列解释事实的方程式正确的是( )
A. 将NO2通入水中,红棕色消失:3NO2+H2O=2HNO3+O2
B. 漂白粉实现漂白性:CO2+2ClO-+H2O=CO32-+2HClO
C. Na与水反应产生气体:Na+H2O=Na++OH-+H2↑
D. 燃煤时加入石灰石可减少SO2的排放:2CaCO3+O2+2SO2![]() 2CaSO4+2CO2
2CaSO4+2CO2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学在实验室利用氢氧化钠、盐酸分离铁粉和铝粉混合物,转化关系如下如所示:下列说法不正确的是( )

A. x为NaOH溶液,y为盐酸
B. a→b发生的反应为:AlO2-+H++H2O=Al(OH)3↓
C. 按照本流程,x和y调换后也能达到实验目的
D. b、c既能与强酸又能与强碱反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法错误的是
A. 氯化铵溶液,加水稀释时,c(NH4+)/c(Cl-)的值一定减小
B. 0.1 mol·L-1的盐酸和0.1 mol·L-1的弱酸HA溶液分别加水稀释10倍:pH(HA) > pH(盐酸)
C. 已知25℃时,HA的Ka=6.25×10—5,当pH为5.0时,HA溶液中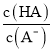 = 0.16
= 0.16
D. 某二元酸的酸式盐NaHA溶液中必然存在:c(H+)+c(A2—)=c(OH—)+c(H2A)
【答案】D
【解析】A、加水稀释时,促进铵根离子水解,所以铵根离子浓度减小的程度大,c(NH4+)/c(Cl-)的值一定减小,选项A正确;B、0.1 mol·L-1的盐酸(pH=1)和0.1 mol·L-1的弱酸HA(pH>1)溶液分别加水稀释10倍后,盐酸的pH=2,HA的pH>2,pH(HA) > pH(盐酸),选项B正确;C、根据HA![]() H++A-,Ka=
H++A-,Ka=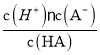 =6.25×10-5,故当溶液的pH为5.0时,c(H+)=10-5 mol·L-1,HA溶液中
=6.25×10-5,故当溶液的pH为5.0时,c(H+)=10-5 mol·L-1,HA溶液中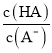 =
=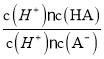 =
=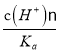 =
=![]() =0.16,选项C正确;D、依据溶液中电荷守恒和物料守恒计算分析,某二元弱酸的酸式盐NaHA溶液中电荷守恒c(H+)+c(Na+)=c(OH-)+c(HA-)+2c(A2-),物料守恒c(Na+)=c(H2A)+c(HA-)+c(A2-),计算得到c(OH-)+c(A2-)=c(H+)+c(H2A),选项D错误。答案选D。
=0.16,选项C正确;D、依据溶液中电荷守恒和物料守恒计算分析,某二元弱酸的酸式盐NaHA溶液中电荷守恒c(H+)+c(Na+)=c(OH-)+c(HA-)+2c(A2-),物料守恒c(Na+)=c(H2A)+c(HA-)+c(A2-),计算得到c(OH-)+c(A2-)=c(H+)+c(H2A),选项D错误。答案选D。
【题型】单选题
【结束】
24
【题目】有关锌-稀硫酸-铜构成的原电池的一些说法中,正确的是( )
A. 锌片为正极,且锌片逐渐溶解
B. 铜片为负极,且铜片上有气泡
C. 溶液中的H+移向铜极
D. 该电池工作的过程中溶液的酸性始终不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知A、B、C、D和E是原子序数依次增大前20号元素。A原子价电子层p轨道中只有1个电子;B、C、D元素的基态原子具有相同的能层数,B、D元素原子的p能级上都有1个未成对电子,D原子得一个电子填入3p轨道后,3p轨道已充满,C原子的p轨道中有3个未成对电子;E是同周期第一电离能最小的元素。回答下列问题:
(1)B3+的结构示意图为______,C的最高价氧化物对应水化物与E的最高价氧化物对应水化物按物质的量1:1反应的离子方程式为__________。
(2)上述五种元素中碱性最强物质的电子式为_________; D所在周期第一电离能最大的元素是________;AD3是_________分子(填“极性”或“非极性”)
(3)B单质为面心立方晶体,晶胞中B原子的配位数为_________.
(4)石墨具有平面层状结构,同一层中的原子构成许许多多的正六边形,它与熔融的E单质相互作用,形成某种青铜色的物质(其中的元素E用“●”表示),原子分布如图所示,该物质的化学式为_________________。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在2 L密闭容器内,t℃时发生反应:N2(g)+3H2(g)![]() 2NH3(g),在体系中,n(N2)随时间的变化如下表:
2NH3(g),在体系中,n(N2)随时间的变化如下表:
时间(min) | 0 | 1 | 2 | 3 | 4 | 5 |
N2的物质的量(mol) | 0.20 | 0.10 | 0.08 | 0.06 | 0.06 | 0.06 |
(1)上述反应在第5min时,N2的转化率为_______________________;
(2)用H2表示从0~2 min内该反应的平均速率v(H2)=_____________;
(3)t℃时,在4个均为2L密闭容器中不同投料下进行合成氨反应。根据在相同时间内测定的结果,判断该反应进行快慢的顺序为______________。(用字母填空,下同);
a.v(NH3)=0.05 mol·L-1·min-1 b.v(H2)=0.03 mol·L-1·min-1
c.v(N2)=0.02 mol·L-1·min-1 d.v(H2)=0.00 l mol·L-1·s-1
(4)下列表述能作为反应达到化学平衡状态的标志是_____________。
a.反应速率v(N2):v(H2):v(NH3)=1:3:2
b.各组分的物质的量浓度不再改变
c.混合气体的平均相对分子质量不再改变
d.混合气体的密度不变
e.单位时间内生成n mol N2的同时,生成3n mol H2
f.v(N2)消耗=2v(NH3)消耗
g.单位时间内3mol H—H键断裂的同时2mol N—H键也断裂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验操作或对实验事实的叙述不正确的是( )
A. 可用稀硝酸清洗做过银镜反应实验的试管
B. 用NaOH溶液可鉴别分别含Na+、Mg2+、Al3+、Fe2+、Fe3+、NH4+阴离子的溶液
C. 向沸腾的NaOH稀溶液中逐滴滴加FeCl3饱和溶液,可制备Fe(OH)3胶体
D. 配制浓硫酸和浓硝酸的混合酸时,应将浓硫酸沿器壁慢慢加入到浓硝酸中,并不断搅拌
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com