
【题目】已知:①CH4(g)+2O2(g)===CO2(g)+2H2O(l) ΔH1=-Q1
②H2(g)+![]() O2(g)===H2O(g) ΔH2=-Q2
O2(g)===H2O(g) ΔH2=-Q2
③H2(g)+![]() O2(g)===H2O(l) ΔH3=-Q3
O2(g)===H2O(l) ΔH3=-Q3
常温下取体积比为4∶1的甲烷和氢气的混合气体11.2 L(已折合成标准状况)经完全燃烧恢复到常温,放出的热量为
A. 0.4Q1+0.05Q2 B. 0.4Q1+0.1Q2
C. 0.4Q1+0.05Q3 D. 0.4Q1+0.1Q3
科目:高中化学 来源: 题型:
【题目】W、X、Y、Z是原子序数依次增大的短周期主族元素。已知W原子的最外层电子数是电子层数的2倍,Y原子次外层电子数与其它各层电子总数相等,W和X的原子序数之和等于Z的原子序数。下列说法正确的是
A. 含氧酸的酸性:Z>W
B. 在一定条件下W的单质能与Y的最高价氧化物对应的水化物反应
C. 四种元素均能与氢元素形成共价键
D. 简单离子半径:X>Y>Z
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质的性质比较,正确的是( )
A. 酸性:H2SO4>HClO4>HBrO4 B. 碱性:NaOH>KOH>RbOH
C. 非金属性:P>S>Cl D. 气态氢化物稳定性:HF>HCl>H2S
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】C、Q、Y、Z四种元素在周期表中的相对位置如图所示,C的简单氢化物可使湿润的红色石蕊试纸变蓝。下列说法正确的是( )
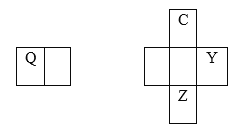
A. C只有两种氧化物
B. Q的单质在常温下可与水迅速反应
C. Y在阴暗处即可与H2剧烈反应并爆炸
D. Z的最高正价与最低负价的代数和为4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】W、X、Y、Z是原子序数依次增大的短周期主族元素。已知W原子的最外层电子数是电子层数的2倍,Y原子次外层电子数与其它各层电子总数相等,W和X的原子序数之和等于Z的原子序数。下列说法正确的是
A. 含氧酸的酸性:Z>W
B. 在一定条件下W的单质能与Y的最高价氧化物对应的水化物反应
C. 四种元素均能与氢元素形成共价键
D. 简单离子半径:X>Y>Z
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2016年7月报道,南开大学科研团队在“可充室温钠-二氧化碳电池”的研究中取得突破进展,该电池放电时工作情况如图所示。下列说法错误的是

A. 金属Na为电池的负极
B. 放电时,电解液中Na+向碳电极移动
C. 充电时,碳电极发生的反应为:4Na++4e-+3CO2== 2Na2CO3+C
D. 放电时,每转移2 mol电子,消耗标准状况下的CO2 33.6 L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某实验小组为了证明SO2和Cl2的漂白性,设计了如图所示的实验装置:
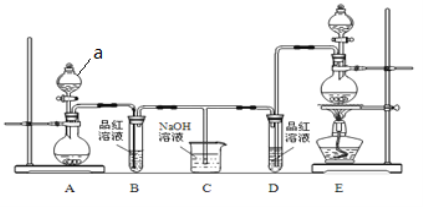
(1)仪器a的名称是____。
(2)利用图中A装置进行实验室制备SO2的化学方程式是____。
(3)反应开始后,发现B、D两个试管中的品红溶液都褪色。停止通气后,给B、D两支试管中的液体加热,试管中现象是:B__;D___。据此,说明SO2的漂白特点是_____。
(4)装置C的作用是_______。
(5)将等物质的量的SO2和Cl2同时通入水中,所得水溶液没有漂白性的原因是(用离子方程式表示)________。要检验此时溶液中生成的负一价阴离子,方法是_____(要求答出具体实验操作、现象及结论)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氟他胺G是一种可用于治疗肿瘤的药物。实验室由芳香烃A制备G的合成路线如下:

回答下列问题:
(1)A的结构简式为____________。C的化学名称是______________。
(2)③的反应试剂和反应条件分别是____________________,该反应的类型是__________。
(3)⑤的反应方程式为_______________。吡啶是一种有机碱,其作用是____________。
(4)G的分子式为______________。
(5)H是G的同分异构体,其苯环上的取代基与G的相同但位置不同,则H可能的结构有______种。
(6)4-甲氧基乙酰苯胺(![]() )是重要的精细化工中间体,写出由苯甲醚(
)是重要的精细化工中间体,写出由苯甲醚(![]() )制备4-甲氧基乙酰苯胺的合成路线___________(其他试剂任选)。
)制备4-甲氧基乙酰苯胺的合成路线___________(其他试剂任选)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com