
(15分)CoCl2·6H2O是一种饲料营养强化剂。一种利用水钻矿(主要成分为CO2O3、Co
(OH)3,还含少量Fe2O3、Al2O3、MnO等)制取CoCl2·6H2O的工艺流程如下:
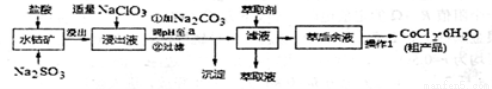
已知:①浸出液含有的阳离了主要有H+、CO2+、Fe2+、Mn2+、Al3+等:
②部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:(金属离子浓度为:0.01 mo1·L-l)

③CoCl2·6H2O熔点为86℃,加热至110~120℃时,失去结晶水生成无水氯化钴。
(1)写出浸出过程中Co2O3发生反应的离子方程式 。
(2)写出NaC1O3发生反应的主要离子方程式 ;若不慎向“浸出液”中加过量NaClO3时,可能会生成有毒气体,写出生成该有毒气体的离子方程式 。
(3)“加Na2CO3调pH至a'’,过滤所得到的沉淀成分为____ 。
(4)萃取剂对金属离子的萃取率与pH的关系如图。向“滤液”中加入萃取剂的目的是 :其使用的最佳pH范围是____ 。

A.2.0~2.5 B.3.0~3.5 C.4.0~4.5 D.5.0~5.5
(5)“操作l”中包含3个基本实验操作,它们依次是 、 和过滤。制得的CoC12·6H2O在烘干时需减压烘干的原因是 。
(6)为测定粗产品中CoCl2·6H2O含量,称取一定质量的粗产品溶于水,加入足量AgNO3溶液,过滤、洗涤,将沉淀烘干后称其质量。通过计算发现粗产品中CoCl2·6H2O的质量分数大于100%,其原因可能是 。(答一条即可)
27.(15分)(1)Co2O3+SO32-+4H+=2Co2++SO42-+2H2O (2分)
(2)ClO3-+6Fe2++6H+=Cl-+6Fe3++3H2O (2分) ClO3-+5Cl-+6H+=3Cl2↑+3H2O (2分)
(3)Fe(OH)3 Al(OH)3 (2分)
(4)除去溶液中的Mn2+ (1分) B (1分)
(5)蒸发(浓缩)、冷却(结晶) (2分) 降低烘干温度,防止产品分解(1分)
(6)粗产品含有可溶性氯化物或晶体失去了部分结晶水 (2分)
【解析】
试题分析:(1)亚硫酸钠常作为还原剂,水钻矿中的CO2O3需转化成Co2+,故CO2O3在酸性条件下和亚硫酸根离子发生氧化还原反应,故为:Co2O3+SO32-+4H+=2Co2++SO42-+2H2O;(2)浸出液Fe2+,需将亚铁离子氧化为铁离子,再通过调节pH而除去,故氯酸钠的作用是将亚铁离子氧化为铁离子,故为:ClO3-+6Fe2++6H+=Cl-+6Fe3++3H2O;氯酸根离子和氯离子在酸性条件下会生成氯气;(3)调节pH目的是除去杂质,根据表格信息和流程图可知,通过调节pH除去铁离子和铝离子,故沉淀为氢氧化铁和氢氧化铝;(4)通过分析流程图可知还需要除去Mn2+,根据题目信息可知,加入萃取剂的目的就是除去锰离子;由萃取剂对金属离子的萃取率与pH的关系可知,调节溶液PH在3.0~3.5之间,可使Mn2+完全沉淀,并防止Co2+转化为Co(OH)2沉淀;(5)由溶液得到结晶水合物的基本操作为蒸发浓缩、冷却结晶;减压烘干的目的是防止水合物分解;(6)根据CoCl2?6H2O的组成分析,造成产品中CoCl2?6H2O的质量分数大于100%的原因可能是:1、含有杂质,导致氯离子含量大,2、结晶水化物失去部分水,导致相同质量的固体中氯离子含量变大。
考点:。


 口算小状元口算速算天天练系列答案
口算小状元口算速算天天练系列答案科目:高中化学 来源:2013-2014河南省洛阳市高三下学期统考二练理综化学试卷(解析版) 题型:填空题
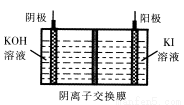
碘被称为“智力元素”,科学合理地补充碘可防止碘缺乏病,KI、KIO3曾先后用于加碘盐中。
(1)工业上可以通过铁屑法生产KI,其工艺流程如下:

①反应I生成铁与碘的化合物,若该化合物中铁元素与碘元素的质量比为21:127,则加入足量碳酸钾时,反应Ⅱ的化学方程式为 。
②操作A包括 ;用冰水洗涤的目的是 。
(2)KIO3可以通过H2O2氧化I2先制得HIO3,然后再用KOH中和的方法进行生产。
①烹饪时,含KIO3的食盐常在出锅前加入,其原因是 。
②若制得1284 kg KIO3固体,理论上至少需消耗质量分数为30%的双氧水 kg。
③KIO3还可通过下图所示原理进行制备。电解时总反应的离子方程式为 。若忽略溶液体积的变化,则电解结束后阴极区的pH与电解前相比 (选填“增大”、“减小”或“不变”)。
查看答案和解析>>
科目:高中化学 来源:2013-2014河南省高二上学期期末考试化学试卷(解析版) 题型:选择题
相同温度下,体积均为0.25L的两个恒容密闭容器中发生可逆反应:
X2(g) + 3Y2(g)  2XY3(g) △H=-92.6 kJ·mol-1
2XY3(g) △H=-92.6 kJ·mol-1
实验测得反应在起始、达到平衡时的有关数据如下表所示:
容器 编号 | 起始时各物质物质的量/mol | 达平衡时体系能量的变化 | ||
X2 | Y2 | XY3 | ||
① | 1 | 3 | 0 | 放热 23.15 kJ |
② | 0.6 | 1.8 | 0.8 | Q(Q>0) |
下列叙述不正确的是
A.容器①、②中反应的平衡常数相等
B.容器②中反应达到平衡时放出的热量Q为23.15kJ
C.达平衡时,两个容器中XY3的物质的量浓度均为2 mol·L-1
D.若容器①体积为0.20 L,则达平衡时放出的热量大于23.15 kJ
查看答案和解析>>
科目:高中化学 来源:2013-2014河南省安阳市高三毕业班第二次模拟理综化学试卷(解析版) 题型:简答题
溴化锂常用于制冷工业,可用尿素、碳酸锂及溴为原料生产溴化锂,其原理是
3Br2+3Li2CO3+CO(NH2)2 6LiBr+2H2O+N2↑+4CO2↑其主要工艺流程如下:
6LiBr+2H2O+N2↑+4CO2↑其主要工艺流程如下:
(1)溴化时,pH过小对反应不利,一方面是因为碳酸锂会反应生成_____________,另一方面使溴单质和水的反应平衡向_______移动,温度不宜超过60℃的原因是_______。
(2)反应过程中,若pH>6,产品中会有溴酸盐,其原因是BrO-发生了自身的氧化还原反应,写出反应的离子方程式:________________。
(3)试剂X的化学式为_____________,加活性炭处理的目的是________________。
(4)若直接用氨水代替尿素也可生产溴化锂,同时生成水、二氧化碳和氮气,该反应的化学方程式为_________________。
(5)用惰性电极电解熔融碳酸锂可得到金属锂,则阳极的电极方程式为______________。
(6)若原料中碳酸锂的质量为mg,最终得到溴化锂的质量为ng,据此能不能计算出溴化锂的产率?若能请写出其表达式(含m、n的表达式);若不能,请说明理由______________。
查看答案和解析>>
科目:高中化学 来源:2013-2014河南省安阳市高三毕业班第二次模拟理综化学试卷(解析版) 题型:选择题
硼化钒-空气电池是目前储电能力最高的电池,电池示意图如下图所示,该电池工作时的反应为:4 VB2+11O2===4B2O3+2V2O5,下列说法正确的是

A.电极a是电源负极
B.溶液中的OH-向a极移动
C.电子由VB2极经KOH溶液流向电极a
D.VB2极发生的电极反应为:
2 VB2+22OH-===V2O5+2B2O3+11H2O+22e-
查看答案和解析>>
科目:高中化学 来源:2013-2014河南省商丘市高三第三次模拟考试理综化学试卷(解析版) 题型:选择题
下列关于甲、乙、丙、丁四个图像的说法中,正确的是

A.甲是亚硫酸氢钠粉末投入稀硝酸溶液中有关图像
B.乙是等pH的HA和HB两种弱酸溶液稀释时pH变化图,由此可知HA的酸性弱于HB
C.由丙可知,双氧水在有催化剂存在时的热化学方程式为
2H2O2(1)=2H 2O(l)+O2(g) △H=-2(Ea2’-Ea2) kJ·mol-l
D.丁是向硝酸银溶液中滴加氨水时,沉淀质量与氨的物质的量的关系图
查看答案和解析>>
科目:高中化学 来源:2013-2014河南省周口市高一下学期期末考试化学试卷(解析版) 题型:填空题
五种短周期元素D、E、F、X、Y、Z的原子序数依次增大,D、E两元素最高正价与最低负价之和均为0,E元素的一种同位素常用于考古断代,D和X同主族,F和Y同主族,F的多种化合物可用作化肥,豆科植物的根瘤菌可将其单质转化为化合物,X和Z形成的二元化合物是厨房常用的调味品。回答下列问题:
(1)①E元素在元素周期表中的位置是_______________。
②由D和F,Y,Z所形成的最简单常见共价型化合物中,热稳定性最差的是__________(用化学式表示,下同);还原性最强的是_____________。
③F、X、Z形成的简单离子半径从大到小顺序为_________________(用离子符号表示)
④D、F、Z形成一种离子化合物,写出它的电子式________________________。
(2)①2012年,罗马大学科学家制造出F4分子,则F4和F2两种单质的关系是____________。
②F、X形成的一种二元离子化合物具有非常强的爆炸性,该物质中X的质量分数是35.38%,,则该物质的化学式为___________。
③Z单质和FD3发生置换反应,观察到有大量白烟生成,写出该反应化学方程式__________,反应中氧化剂和还原剂物质的量之比为____________________。
查看答案和解析>>
科目:高中化学 来源:2013-2014河南省周口市高二下学期6月联考化学试卷(解析版) 题型:填空题
已知物质A分子式为C3H4O2,显酸性。F为由七个原子组成的环状结构,分子式为C6H8O4。请根据以下框图回答问题:
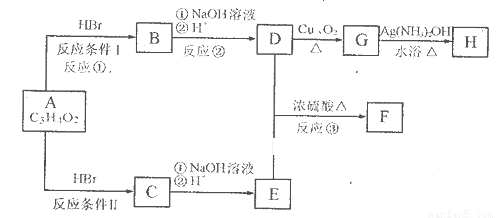
(1)A的结构简式为________________________________。
(2)反应①的反应类型为__________________________。
(3)化合物B中含氧官能团的名称是______________________________。
(4)D和E生成F的化学方程式__________________________________。
D和E按照1:1反应也可生成高聚物,请写出生成该高聚物的化学反应方程式=______
________________________________________________________________________。
(5)G生成H的化学方程式________________________________________________。
(6)写出C的同分异构体中属于酯类物质的结构简式_______________________、
________________________、____________________________________(至少写3个)
查看答案和解析>>
科目:高中化学 来源:2013-2014河南省周口市高一下学期6月联考化学试卷(解析版) 题型:选择题
已知2 mol H2(g)燃烧生成液态水放出的热量为571.6 lkJ,而2 molH2 (g)完全燃烧生成气态水放的热量为483. 6 kJ。下列说法正确的是
A. l molH2O (I)变成lmolH2O (g),向外界释放能量
B.1 molH2O (g)分解成H2(g)和O2(g),吸收241. 8 kJ能量
C.2 mol H2(g)和l mol O2(g)的总能量小于2 molH2O(1)的能量
D.断裂2 molH2O (g)中所有的O-H键,吸收483. 6 kJ能量
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com