
碘被称为“智力元素”,科学合理地补充碘可防止碘缺乏病,KI、KIO3曾先后用于加碘盐中。
(1)工业上可以通过铁屑法生产KI,其工艺流程如下:

①反应I生成铁与碘的化合物,若该化合物中铁元素与碘元素的质量比为21:127,则加入足量碳酸钾时,反应Ⅱ的化学方程式为 。
②操作A包括 ;用冰水洗涤的目的是 。
(2)KIO3可以通过H2O2氧化I2先制得HIO3,然后再用KOH中和的方法进行生产。
①烹饪时,含KIO3的食盐常在出锅前加入,其原因是 。
②若制得1284 kg KIO3固体,理论上至少需消耗质量分数为30%的双氧水 kg。
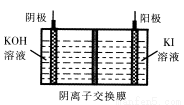
③KIO3还可通过下图所示原理进行制备。电解时总反应的离子方程式为 。若忽略溶液体积的变化,则电解结束后阴极区的pH与电解前相比 (选填“增大”、“减小”或“不变”)。
(1)① Fe3I8 + 4K2CO3 = Fe3O4 + 8KI + 4CO2↑ (2分)
② 加热浓缩、冷却结晶、过滤 (2分)
洗涤除去表面可溶性杂质,同时减少KI的溶解损失 (2分)
(2)① 在较高温度下KIO3易分解(2分) ②1700 (2分)
③ I一+ 3H2O通电IO3- + 3H2↑ (2分) 不变(2分)
【解析】
试题分析:(1)①反应I生成铁与碘的化合物,铁元素与碘元素的质量比为21:127,即物质的量比是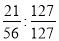 =3:8,故反应方程式是Fe3I8 + 4K2CO3 = Fe3O4 + 8KI + 4CO2↑。
=3:8,故反应方程式是Fe3I8 + 4K2CO3 = Fe3O4 + 8KI + 4CO2↑。
②用冰水洗涤的目的是洗涤除去表面可溶性杂质,同时减少KI的溶解损失;
(2)①烹饪时,含KIO3的食盐常在出锅前加入,其原因是在较高温度下KIO3易分解;
②因为H2O2氧化I2先制得HIO3:5H2O2+I2==2HIO3+4H2O,即5H2O2~2IO3-,1284 kg KIO3固体为6k mol,故m(H2O2)= 5/2×6kmol×34g·mol-1/30%=1700kg。
③ 虽然阴极区有大量氢氧根离子生成,但阳极区反应消耗氢氧根离子,氢氧根离子通过阴离子交换膜到阳极区反应,总反应中没有酸或碱生成以及消耗。故而阴极区反应前后pH没有变化。当然,如果题目没有“忽略溶液体积变化“的说明,情况就不同了,随着电解的进行,总反应耗水,阴极区pH会增大。
考点:官能团为酯键的芳香化合物的性质。


科目:高中化学 来源:2013-2014河南省濮阳市高二下学期升级考试化学试卷(解析版) 题型:选择题
物质的量浓度相同的下列物质中,含粒子种类最多的是
A.CaCl2 B.CH3COONa C.K2S D.NH3
查看答案和解析>>
科目:高中化学 来源:2013-2014河南省濮阳市高一下学期升级考试化学(A卷)试卷(解析版) 题型:选择题
山梨酸是一种常见的食物添加剂,它是一种无色针状晶体或白色粉末,它的结构简式为CH3—CH=CH—CH=CH—COOH。下列关于山梨酸的叙述不正确的是
A.山梨酸易溶于乙醇
B.山梨酸能与氢气发生加成反应
C.山梨酸能和乙醇反应生成酯
D.1mol山梨酸能和金属钠反应生成1mol氢气
查看答案和解析>>
科目:高中化学 来源:2013-2014河南省洛阳市高三年级第三次考试理综化学试卷(解析版) 题型:选择题
下列有关说法正确的是
A.0.1 mol/L NH4C1溶液加蒸馏水稀释,溶液的pH不断减小
B.常温下,pH=2的CH3COOH溶液与pH=12的NaOH溶液等体积混合后,溶液的pH<7
C. 水的离子积常数Kw随着温度的升高而增大,说明水的电离是放热反应
D.0.1 mol/L的NaHA溶液,其pH=4: c(HA-) > c(H+)> c(H2A) > c(A2-)
查看答案和解析>>
科目:高中化学 来源:2013-2014河南省洛阳市高三年级第三次考试理综化学试卷(解析版) 题型:选择题
下列实验设计方法正确的是
A. 向卤代烃加硝酸酸化的硝酸银来检验其中的卤族素元素
B. 实验用NH4Cl固体受热分解来制备NH3
C. 用盐酸和澄清石灰水来检验某物质是否含有CO32-
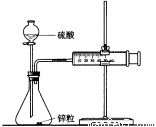
D. 可用下图所示的装置和药品来研究反应物浓度对反应速率的影响
查看答案和解析>>
科目:高中化学 来源:2013-2014河南省洛阳市高三下学期统考二练理综化学试卷(解析版) 题型:选择题
如图表示水中c(H+)和c(OH-)的关系,下列判断错误的是

A.两条曲线间任意点均有c(H+)·c(OH-)=Kw
B.M区域内任意点均有c(H+)<c(OH-)
C.图中T1<T2
D.XZ线上任意点均有pH=7
查看答案和解析>>
科目:高中化学 来源:2013-2014河南省洛阳市下学期期中考试高二化学试卷(解析版) 题型:填空题
(10分)如图是用于简单有机化合物的制备、分离、性质比较等的常见简易装置。请
根据该装置回答下列问题:

(1)若用乙醇与乙酸反应制取乙酸乙酯,则烧瓶A
中加入的试剂在混合时的操作方法是___________,反
应的化学方程式为___________ ,试管B中应
加入___________ 。虚线框中的导管除用于导气
外,还兼有___________ 作用。
(2)若用该装置分离乙酸和1-丙醇,则在烧瓶A
中除加入1-丙醇与乙酸外,还应先加入适量的试剂
___________,加热到一定温度,试管B中收集到的是(填写化学式)___________。冷却后,再向烧瓶中加入试剂___________再加热到一定温度,试管B中收集到的是___________(填写化学式)。
若用该装置(不用加热)证明酸性:醋酸>碳酸>苯酚,则在烧瓶A中加入___________ ,试管B中应加入___________。
查看答案和解析>>
科目:高中化学 来源:2013-2014河南省洛阳市下学期期中考试高二化学试卷(解析版) 题型:选择题
不能在有机物分子中直接引入官能团羟基的反应类型是
A.取代反应 B.消去反应 C.加成反应 D.水解反应
查看答案和解析>>
科目:高中化学 来源:2013-2014河南省商丘市高三第三次模拟考试理综化学试卷(解析版) 题型:实验题
(15分)CoCl2·6H2O是一种饲料营养强化剂。一种利用水钻矿(主要成分为CO2O3、Co
(OH)3,还含少量Fe2O3、Al2O3、MnO等)制取CoCl2·6H2O的工艺流程如下:
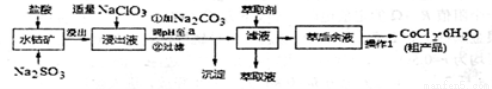
已知:①浸出液含有的阳离了主要有H+、CO2+、Fe2+、Mn2+、Al3+等:
②部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:(金属离子浓度为:0.01 mo1·L-l)

③CoCl2·6H2O熔点为86℃,加热至110~120℃时,失去结晶水生成无水氯化钴。
(1)写出浸出过程中Co2O3发生反应的离子方程式 。
(2)写出NaC1O3发生反应的主要离子方程式 ;若不慎向“浸出液”中加过量NaClO3时,可能会生成有毒气体,写出生成该有毒气体的离子方程式 。
(3)“加Na2CO3调pH至a'’,过滤所得到的沉淀成分为____ 。
(4)萃取剂对金属离子的萃取率与pH的关系如图。向“滤液”中加入萃取剂的目的是 :其使用的最佳pH范围是____ 。

A.2.0~2.5 B.3.0~3.5 C.4.0~4.5 D.5.0~5.5
(5)“操作l”中包含3个基本实验操作,它们依次是 、 和过滤。制得的CoC12·6H2O在烘干时需减压烘干的原因是 。
(6)为测定粗产品中CoCl2·6H2O含量,称取一定质量的粗产品溶于水,加入足量AgNO3溶液,过滤、洗涤,将沉淀烘干后称其质量。通过计算发现粗产品中CoCl2·6H2O的质量分数大于100%,其原因可能是 。(答一条即可)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com