
【题目】将0.1 mol的MnO2和40 mL 10 mol·L-1的浓盐酸混合后加热,充分反应后,向所得溶液中加入足量的AgNO3溶液。在此过程中:
(1)产生的Cl2在标准状况下的体积V(Cl2)为(可填写体积范围);
(2)产生的AgCl沉淀的物质的量为(假设盐酸不挥发,且产生的Cl2的物质的量为a mol)。
【答案】
(1)0<V(Cl2)<2.24 L
(2)(0.4-2a) mol
【解析】由题意可知,盐酸的物质的量为0.4 mol,理论上由方程式MnO2+4HCl(浓)![]() MnCl2+Cl2↑+2H2O可知,0.4 mol盐酸能恰好和0.1 mol MnO2反应。但实际过程中,随盐酸浓度的降低,只有部分HCl能够参加反应,当浓盐酸变成稀盐酸后,反应便会停止,故0<V(Cl2)<2.24 L。求AgCl沉淀的量时要注意运用守恒思想,根据氯原子总数守恒,计算出溶液中剩余Cl-的物质的量为(0.4-2a) mol,即产生的AgCl物质的量为(0.4-2a) mol。
MnCl2+Cl2↑+2H2O可知,0.4 mol盐酸能恰好和0.1 mol MnO2反应。但实际过程中,随盐酸浓度的降低,只有部分HCl能够参加反应,当浓盐酸变成稀盐酸后,反应便会停止,故0<V(Cl2)<2.24 L。求AgCl沉淀的量时要注意运用守恒思想,根据氯原子总数守恒,计算出溶液中剩余Cl-的物质的量为(0.4-2a) mol,即产生的AgCl物质的量为(0.4-2a) mol。
【考点精析】解答此题的关键在于理解氯气的化学性质的相关知识,掌握氯气的化学性质:与金属反应将金属氧化成高价态;非金属反应;与水反应;与碱反应;与还原性物质反应.


科目:高中化学 来源: 题型:
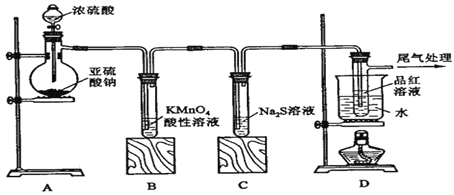
【题目】某化学兴趣小组为探究SO2的性质,按下图所示装置进行实验。
请到答F列问题:
(1)装置A中盛放亚硫酸钠的仪器名称是______________,其中发生反应的化学方程式为_______________________________________________________________;
(2)实验过程中,装置B、C中发生的现象分别是___________、___________,这些现象分别说明SO2具有的性质是__________和___________;装置B中发生反应的离子方程式为_______________________________________________________________;
(3)装置D的目的是探究SO2与品红作用的可逆性,请写出实验操作及现象_____________________________;
(4)尾气可采用_____________溶液吸收。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用铝箔包裹4.6 g金属钠,用针扎一些小孔,放入水中,用排水取气法收集产生的气体,则收集到的气体为( )
A. O2和H2的混合气体 B. 0.1 mol H2 C. 大于0.1 mol H2 D. 小于0.1 mol H2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将下列各组物质,按酸、碱、盐顺序排列正确的是( )
A. 硫酸、纯碱、食盐 B. 氢硫酸、烧碱、硫酸铜
C. 碳酸、氧化铜、碳酸钠 D. 醋酸、熟石灰、苛性钠
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室用下列有关装置先制取干燥、纯净的氯气,后进行有关性质实验。试回答下列问题。
(1)上述装置中各仪器从左至右的连接顺序为接接接接接接。
(2)E装置的作用是 , G装置的作用是 , D中的现象为 , B中的现象为。
(3)写出下列反应的离子方程式:B中 , G中。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于物质氧化性及还原性的强弱,下列说法中正确的是( )
A. 物质越易失电子,还原性越强
B. 原子失电子越多,还原性越强
C. 元素化合价降低越多,氧化性越强
D. 物质越易被氧化,氧化性越强
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】HO2(超氧酸)是一种弱酸,具有极高的活性。一定条件下,铜与盐酸、氧气发生如下反应可生成HO2:Cu+HCl+O2===CuCl+HO2 , 下列说法正确的是( )
A.上述反应中,O2发生了氧化反应
B.HO2在碱溶液中能稳定存在
C.上述反应中HO2是还原产物
D.上述反应的离子方程式为Cu+Cl-+O2===CuCl+O
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com