
【题目】按要求回答下列问题:
(1)Ni是元素周期表中第28号元素,第二周期基态原子未成对电子数与Ni相同且电负性最小的元素是____。
(2)前3周期元素中,基态原子中未成对电子数与其所在周期数相同的元素有____种。
(3)依据第二周期元素第一电离能的变化规律,参照如图中B、F元素的位置,用小黑点标出C、N、O三种元素的相对位置。____

【答案】C或碳 4 
【解析】
⑴Ni是元素周期表中第28号元素,电子排布式为1s22s22p63s23p63d84s2,有2个未成对电子,第二周期基态原子未成对电子数有2对的是C、O,电负性最小的元素是C,
故答案为:C或碳;
⑵前3周期元素中,基态原子中未成对电子数与其所在周期数相同的元素,第一周期为H,第二周期有1s22s22p2、1s22s22p4为C、O;第三周期有1s22s22p63s23p3为P;因此共有4种,
故答案为:4;
⑶依据第二周期元素第一电离能的变化规律,第二周期从左向右元素的第一电离能呈增大趋势,但氮元素因为p层电子为半充满状态,其第一电离能大于氧,C、N、O三种元素的相对位置, ,
,
故答案为: 。
。


科目:高中化学 来源: 题型:
【题目】通常状况下,稀强酸、稀强碱反应生成1mol水时放出![]() 的热
的热
(1)实验室中可用稀盐酸和氢氧化钡稀溶液反应来测定中和热。请写出能表示该反应中和热的热化学方程式 ______ ;
(2)分别取100mL![]() 盐酸与100mL
盐酸与100mL![]() NaOH溶液进行中和反应。通过测定反应过程中所放出的热量可计算中和热。假设盐酸和氢氧化钠溶液的密度都是
NaOH溶液进行中和反应。通过测定反应过程中所放出的热量可计算中和热。假设盐酸和氢氧化钠溶液的密度都是![]() ,中和后生成溶液的比热容
,中和后生成溶液的比热容![]() 实验时,测得反应前盐酸与NaOH溶液的平均温度为
实验时,测得反应前盐酸与NaOH溶液的平均温度为![]() ,反应后混合溶液的温度为
,反应后混合溶液的温度为![]() 则实验测得的中和热
则实验测得的中和热![]() ______
______ ![]() 保留1位小数
保留1位小数![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】0.1 mol某烃在足量的氧气中完全燃烧,生成的CO2和水各0.6 mol。
(1)则该烃的分子式为 _________ 。若该烃不能使溴水或高锰酸钾溶液褪色,但在一定条件下,可以和溴蒸汽发生取代反应,其一溴取代物只有一种,则此烃属于_______ 烃,结构简式为 ____________,名称是____________。
(2)若该烃能使溴水褪色,且能在催化剂作用下与H2发生加成反应,生成2,2—二甲基丁烷,则此烃属于______烃,结构简式为__________,名称是___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】磷酸氯喹能有效抑制新型冠状病毒2019—nCoV的感染,其结构如图所示。下列关于该物质的说法正确的是( )
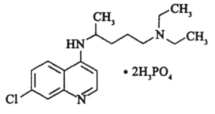
A.分子中N原子均为sp2杂化
B.分子中只含有1个手性碳原子
C.能发生取代反应和消去反应
D.1mol磷酸氯喹最多能与4molH2发生加成反应
查看答案和解析>>
科目:高中化学 来源: 题型:
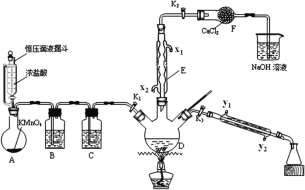
【题目】如图是某小组设计的用干燥氯气和甲苯合成一氯化苄(C6H5CH2Cl,其中C6H5-表示苯基)并分离产物的实验装置。甲苯及各种氯化苄的物理性质如表所示。
物理性质 | 熔点℃ | 沸点℃ | 密度gcm-3 |
甲苯 | -95 | 110 | 0.86 |
一氯化苄(C6H5CH2Cl) | -45 | 179 | 1.10 |
二氯化苄(C6H5CHCl2) | -17 | 205 | 1.26 |
三氯化苄(C6H5CCl3) | -4.4 | 221 | 1.37 |
回答下列问题:
(1)仪器F的名称是__________;
(2)瓶B和C中盛放的试剂应分别为__________(填序号);
a.蒸馏水;浓硫酸 b.饱和食盐水;浓硫酸
c.浓硫酸;酸性KMnO4溶液 d.饱和NaHCO3溶液;浓硫酸
(3)两处冷凝水的进水口应分别为__________(填序号);
A . x1、y1 B. x1、y2 C. x2、y1 D.x2、y2
(4)在回流反应的过程中,由于温度控制不当,部分产物从K2处被蒸出。取烧杯中的少量吸收液于试管中,滴入新制氢氧化铜悬浊液并加热,观察到有砖红色沉淀生成。则在吸收液中发生反应的化学方程式为______________________;
(5)反应结束后,撤去E、F及尾气吸收装置,插上玻璃塞。保持K1关闭,打开K3,加热三颈烧瓶,分馏出一氯化苄,应选择的温度范围是__________;
(6)由于某同学操作时不慎将含铁的沸石加入三颈烧瓶,在分馏时得到了异常馏分X。用质谱法测得X的相对分子质量与二氯化苄相同,核磁共振氢谱显示X中有3种不同化学环境的氢。已知苯环上存在甲基或氯甲基是,后续取代苯环的基团主要引入其邻位或对位,X的结构简式可能为__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】反应C(s)+H2O(g)![]() CO(g)+H2(g)在一密闭容器中进行,则下列说法或结论中,正确是( )
CO(g)+H2(g)在一密闭容器中进行,则下列说法或结论中,正确是( )
A.保持压强不变,充入少量氦气,反应速率会减小
B.若v(CO)=v(H2O),则反应达平衡状态
C.其他条件不变,适当增加C(s)的质量会使反应速率增大
D.其他条件不变,仅将容器的体积缩小一半,反应速率减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知X、Y、Z、W、R都是周期表中前四周期的元索,它们的核电荷数依次增大。X原子有1个2p空轨道,Y原子最外层电子数等于X原子核外电子总数,Z与X同主族,W原子3p轨道只有一个单电子,R3+的3d轨道为半充满状态。回答下列问题:
(1)元素X、Y、Z的电负性由大到小的顺序是__(用元素符号表示)。
(2)元素X、Z的最简单气态氢化物的沸点由高到低的顺序是__(用化学式表示)。
(3)元素X、Y形成的一种化合物在高温高压下所形成的晶体其晶胞如图所示,则该晶体类型属于__晶体,1个晶胞中含有__个X原子。

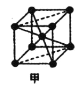
(4)R的一种晶体如甲、乙所示,若按甲虚线方向切乙得到的图A~D中正确的是__(填字母标号)。
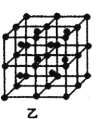
A.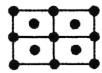 B.
B. C.
C.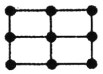 D.
D.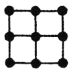
假设R原子的半径是apm,则该晶体的密度的计算式是__g·cm-3(用含a的式子表示,设阿伏加德罗常数的值为NA)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向某密闭容器中加入0.3molA、0.1molC和一定量B三种气体。一定条件下发生反应,各物质浓度随时间变化如图甲所示[t0~t1阶段c(B)未画出]。图乙为t2时刻后改变条件,平衡体系中反应速率随时间变化的情况,且四个阶段都各改变一种条件并且所用条件均不相同。已知t3~t4阶段为使用催化剂。下列说法正确的是( )
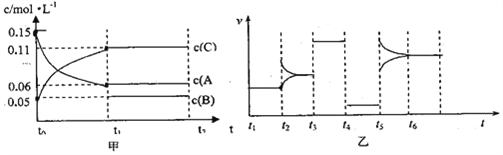
A. 若t1等于15s,生成物C在t0~t1时间段的平均反应速率为0.004mol/(Ls)
B. t4~t5阶段改变的条件为降低反应温度
C. B的起始的物质的量为0.02mol
D. t5~t6阶段可能是增大压强
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氢气与氧气生成水的反应是氢能源应用的重要途径。下列有关说法正确的是
A. 一定温度下,反应2H2(g)+O2(g) ![]() 2H2O(g)能自发进行,该反应的ΔH<0
2H2O(g)能自发进行,该反应的ΔH<0
B. 氢氧燃料电池的负极反应为O2+2H2O+4e![]() 4OH
4OH
C. 常温常压下,氢氧燃料电池放电过程中消耗11.2 L H2,转移电子的数目为6.02×1023
D. 反应2H2(g)+O2(g) ![]() 2H2O(g)的ΔH可通过下式估算:
2H2O(g)的ΔH可通过下式估算:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com