
【题目】下列关于硫酸的叙述正确的是
A. 浓硫酸具有吸水性 B. 稀硫酸可用铁罐贮存
C. 稀硫酸能使蔗糖脱水 D. SO2溶于水,可得到稀硫酸
 步步高口算题卡系列答案
步步高口算题卡系列答案 点睛新教材全能解读系列答案
点睛新教材全能解读系列答案 小学教材完全解读系列答案
小学教材完全解读系列答案科目:高中化学 来源: 题型:
【题目】实验室制取氯气的化学方程式为:MnO2+4HCl(浓)![]() MnCl2+Cl2↑+2H2O。请分别用双线桥法和单线桥法分析该反应中电子转移的方向和数目:
MnCl2+Cl2↑+2H2O。请分别用双线桥法和单线桥法分析该反应中电子转移的方向和数目:
双线桥:MnO2+4HCl(浓)![]() MnCl2+Cl2↑+2H2O。
MnCl2+Cl2↑+2H2O。
__________________________________________
单线桥:MnO2+4HCl(浓)![]() MnCl2+Cl2↑+2H2O。
MnCl2+Cl2↑+2H2O。
___________________________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z、R、M、N为六种短周期元素,其原子半径和最外层电子数之间的关系如图所示。
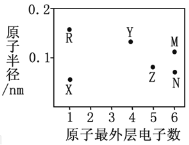
(1)M元素的原子核外有__________种能量不同的电子,有__________个未成对电子;Z元素在元素周期表中的位置是第______周期________族。
(2)N、R、X三种元素的原子可构成一种强碱性物质,该物质的电子式是___________;Y元素的氧化物是制造光纤的主要材料,该氧化物是________晶体(填晶体类型)。某化工生产的核心环节的反应为:2MN2(g) + N2(g) 2 MN3(g) + Q(Q>0)
(3)该反应的平衡常数表达式![]() __________________________;欲使K值变大,可采取的措施是__________________________。
__________________________;欲使K值变大,可采取的措施是__________________________。
(4)该反应达到平衡后,在其他条件不变的情况下,若使得容器的体积扩大为原来的两倍,则平衡____________________。(选填“正向移动”、“逆向移动”或“不移动”)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某实验过程如图所示:则图③的试管中的现象是
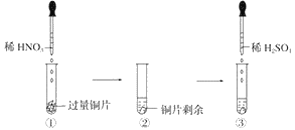
A. 无明显现象,因稀硫酸不与铜反应
B. 铜片溶解,产生无色气体,该气体遇到空气不变色
C. 铜片溶解,放出红棕色有刺激性气味的气体
D. 铜片溶解,产生无色气体,该气体在试管口变为红棕色
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】小刚同学探究二氧化硫分别与BaCl2溶液、Ba(OH)2溶液反应的实验。
(1)少量SO2通入到Ba(OH)2溶液中的离子反应方程式为
________________________________________________________________________,
过量的SO2通入到Ba(OH)2溶液中的离子反应方程式为
________________________________________________________________________。
(2)请回答有关问题。小刚同学将SO2通入到BaCl2溶液中,出现了异常现象,看到了明
显的白色沉淀,为探究该白色沉淀的成分,他设计了如下实验流程:
![]()
![]()
![]()
![]()
![]()
则操作①的名称为________,试剂A的化学式为________。
(3)实验表明,小刚加入试剂A后,白色沉淀未见溶解,则该白色沉淀的成分是________(填化学式),产生该白色沉淀的离子方程式是_________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某学习小组通过查阅资料得知,CO2与Na2O2的反应需要在一定量水蒸气存在的条件下才能进行,于是他们设计了如图所示的装置对此问题进行探究,同时验证Na2O2与CO2反应的气体产物。

(1)写出装置A中有关反应的离子方程式:_________________,装置B中的试剂是____,装置E的作用是_____________。
(2)U形管C中的试剂是____。若要求根据装置D中的现象来确定CO2与Na2O2之间的反应是否需要在潮湿的条件下才能进行,对两个止水夹的操作方式为先打开K1,关闭K2,D中无明显现象;当打开K2,关闭K1,D中的现象为 ______________,则说明反应需要在潮湿条件下进行。
(3)检验气体产物的方法:用玻璃片在水里盖住集气瓶口,将集气瓶从水中取出,正放在实验台上,_______________。
(4)有人认为,经过较长时间反应后,装置D中生成的物质只有Na2CO3而没有NaOH。请设计一个方案证明此结论是正确的:______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知X、Y的核电荷数分别是a和b,它们的离子Xn+和Ym-的核外电子排布相同,则下列关系式中正确的是( )
A. a=b+m+n B. a=b-m+n
C. a=b+m-n D. a=b-m-n
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】亚氯酸钠(NaClO2)是一种高效的漂白剂和消毒剂,它在酸性条件下生成NaCl并放出C1O2,C1O2有类似Cl2的性质。某兴趣小组探究亚氯酸钠的制备与性质。

Ⅰ.制备亚氯酸钠
关闭止水夹②,打开止水夹①,从进气口通入足量C1O2,充分反应。
(1)仪器a的名称为_______,仪器b的作用是_____。
(2)装置A中生成NaC1O2的离子方程式为_______。
(3)若从装置A反应后的溶液中获得NaClO2晶体,则主要操作有减压蒸发浓缩、降温结晶______、_____干燥等。
Ⅱ.探究亚氯酸钠的性质
停止通ClO2气体,再通入空气一段时间后,关闭止水夹①,打开止水夹②,向A中滴入稀硫酸。
(4)开始时A中反应缓慢,稍后产生气体的速率急剧加快,请解释可能的原因_________。
(5)B中现象为_________ 。
(6)实验完成后,为防止装置中滞留的有毒气体污染空气,可以进行的操作是:再次打开止水夹①,_______。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com