
【题目】CuCl广泛应用于有机合成催化。例如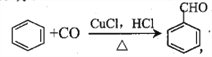 回答下列问题:
回答下列问题:
(1)CuCl中Cu+核外电子排布式为______________,Cu与Cl相比,第一电离能较大的是______________。
(2)已知![]() 为平面分子,则-CHO中碳原子的杂化方式为______________。
为平面分子,则-CHO中碳原子的杂化方式为______________。
(3)写出与CO互为等电子体的非极性分子的电子式______________,14gCO中含______________molπ键。合成氨工业中用铜洗液吸收CO,形成配合物[Cu(NH3)3CO]Ac(HAc代表醋酸),其中______________ (填粒子符号)接受孤对电子形成配位键,配位数是______________。
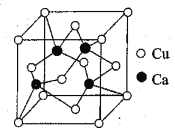
(4)铜钙可形成合金,单质铜的熔点比单质钙高,其原因是____________________________,其中一种合金的晶胞结构构如图所示,已知:该晶体的密度为ρg·cm-3,NA是阿伏加德罗常数的值,则其中两个Ca原子核之间距离为______________。
【答案】 [Ar]3d10 Cl sp2 ![]() 1 Cu+ 4 铜晶体中的金属键比钙晶体中的金属键强度大(合理即可)
1 Cu+ 4 铜晶体中的金属键比钙晶体中的金属键强度大(合理即可) ![]()
【解析】(1)考查电子排布式的书写、第一电离能规律,Cu位于第四周期IB,核外电子排布式为 [Ar]3d10;Cl属于非金属,Cu属于金属,因此Cl的第一电离能大于Cu;(2)考查杂化类型判断,醛基中C有3个σ键,无孤电子对,因此杂化类型为sp2;(3)考查等电子体、化学键、配位键,根据等电子体的定义,符合条件的是N2,即N2的电子式为![]() ;C与O之间共用叁键,1molCO中含有2molπ键,因此14gCO含有π键物质的量为14×2/28mol=1mol,根据配合物组成,Cu+为接受孤对电子,配位数为4;(4)考查晶体熔沸点高低判断、晶胞的计算,金属晶体熔沸点高低判断,需要比较金属键强弱,金属键越强,熔沸点越高,因此有铜晶体中的金属键比钙晶体中的金属键强度大;晶胞的质量为
;C与O之间共用叁键,1molCO中含有2molπ键,因此14gCO含有π键物质的量为14×2/28mol=1mol,根据配合物组成,Cu+为接受孤对电子,配位数为4;(4)考查晶体熔沸点高低判断、晶胞的计算,金属晶体熔沸点高低判断,需要比较金属键强弱,金属键越强,熔沸点越高,因此有铜晶体中的金属键比钙晶体中的金属键强度大;晶胞的质量为 ,根据晶胞的密度的定义,晶胞棱长为
,根据晶胞的密度的定义,晶胞棱长为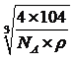 cm,根据晶胞的结构,相邻的两个Ca2+距离是面对角线的一半,即距离为
cm,根据晶胞的结构,相邻的两个Ca2+距离是面对角线的一半,即距离为![]() 。
。


 新课标快乐提优暑假作业陕西旅游出版社系列答案
新课标快乐提优暑假作业陕西旅游出版社系列答案 暑假衔接培优教材浙江工商大学出版社系列答案
暑假衔接培优教材浙江工商大学出版社系列答案 欣语文化快乐暑假沈阳出版社系列答案
欣语文化快乐暑假沈阳出版社系列答案科目:高中化学 来源: 题型:
【题目】下列反应属于氧化还原反应的是
A. CaCO3+2HCl=CaCl2+CO2↑+ H2O
B. CaO+H2O=Ca(OH)2
C. 2H2O2![]() 2H2O+O2↑
2H2O+O2↑
D. CaCO3![]() CaO+CO2↑
CaO+CO2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某一反应体系有反应物和生成物共七种物质:O2,KMnO4,MnSO4,H2SO4,H2O,H2O2,K2SO4,已知H2O2只发生反应H2O2→O2,回答下列问题:
(1)该反应的氧化剂是________。
(2)氧化剂与还原剂的物质的量之比______________。
(3)若反应转移了0.3mol电子,则在标况下生成气体体积___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】混合物分离和提纯常用下图装置进行,按要求回答下列问题:
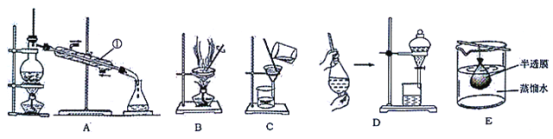
(1)仪器①的名称__________。
(2)明胶是水溶性蛋白质混合物,溶于水形成胶体。分离明胶的水溶液与Na2CO3、Na2SO4的混合溶液应选用装置的为(用上图字母填写)_____。如何证明SO42-已分离出来_____。
(3)在装置D中加入10 mL碘水,然后再注入4 mL CCl4,盖好玻璃塞,按操作规则反复振荡后静置观察到的现象是:___________________________________。操作完毕后,为得到碘并回收CCl4可用________法。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】自然界中金属硫化物之间存在原电池反应。下图所示装置中电极Ⅰ为方铅矿(PbS),电极Ⅱ为含有方铅矿的硫铁矿,当有电解质溶液按如图所示方向流经该装置时,电流表指针偏转。若电极Ⅱ质量不断减少,a处溶液中加入KSCN溶液未出现红色,加入CuSO4溶液未出现黑色沉淀。下列有关说法中正确的是( )
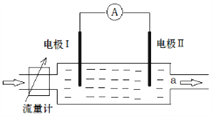
A.工业上利用该原理富集铁
B.电极Ⅱ作正极
C.溶液流经该装置后pH增大
D.该装置负极的电极反应为FeS2—15e—+8H2O=Fe3++2SO42—+16H+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图甲池和乙池中的四个电极都是铂电极,乙池溶液分层,上层溶液为盐溶液,呈中性。请根据图示判断下列有关说法正确的是:( )
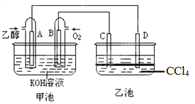
A. 甲池的电解池,乙池是原电池
B. 通入乙醇的铂电极反应式为C2H5OH+16OH-+12e-=2CO32-+11H2O
C. 反应一段时间后,两池溶液的pH均未变化
D. 假如乙池中加入NaI溶液,则在乙池反应过程中,可以观察到C电极周围的溶液呈现棕黄色,反应完毕后,用玻璃棒搅拌溶液,则下层溶液呈现紫红色,上层接近无色
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列浓度关系正确的是
A.0.1 mol/L的NH4HSO4溶液中滴加0.1 mol/L的Ba(OH)2溶液至沉淀刚好完全:c (NH4+)>c (OH-)>c (SO42-)>c (H+)
B.0.1 mol/L的KOH溶液中通入标准状况下的CO2气体3.36 L,所得溶液中:c (K+)+c (H+)=c (CO32-)+c (HCO3-)+c (OH-)
C.0.1 mol/L的NaOH溶液与0.2 mol/L的HCN溶液等体积混合,所得溶液呈碱性:c (HCN)>c (Na+)>c (CN-)>c (OH-)>c (H+)
D.pH相同的NaOH溶液、CH3COONa溶液、Na2CO3溶液、NaHCO3溶液的浓度:c (NaOH)<c (CH3COONa)<c (NaHCO3)<c (Na2CO3)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图为配制480 mL 0.2 mol·L-1 NaCl溶液的示意图。

回答下列问题:
(1)在容量瓶的使用方法中,下列操作不正确的是________(填字母)。
A.使用容量瓶前检查它是否漏水
B.容量瓶用蒸馏水洗净后,再用待配溶液润洗
C.配制溶液时,如果试样是固体,把称好的试样用纸条小心倒入容量瓶中,缓慢加入蒸馏水到接近刻度线1~2 cm处,用胶头滴管滴加蒸馏水到刻度线
D.溶解过程中,要等烧杯中溶液冷却到室温再转入容量瓶
(2)①中应称NaCl________ g;②选择容量瓶的规格____________。
(3)玻璃棒在②、③两步中的作用分别是____________________________、____________________________。
(4)若出现如下情况,对所配溶液浓度有何影响?(填“偏高”“偏低”或“无影响”)
A.某同学在第①步称量时物品和砝码放反了 ________。
B.某同学在第⑧步观察液面时仰视________;
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com