
【题目】随原子序数的递增,八种短周期元素(用字母表示)原子半径的相对大小、最高正价或最低负价的变化如下图所示。
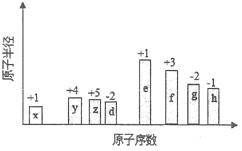
根据判断出的元素回答问题
(1)g的原子结构示意图为______________.
(2)比较e、h 简单离子的半径大小(用化学式表示,下同),_______>_________ .
比较g 、h 的最高价氧化物对应的水化物的酸性强弱是:_________>____________.
(3)任选上述元素组成一种四原子共价化合物,写出其电子式__________ .
(4)己知lmole的单质在足量d2中燃烧,恢复至室温,放出255.5kJ热量,写出表示e 的单质燃烧热的热化学方程式:__________________________.
(5)上述元素可组成常见的碱性气体R。回答下列问题:
①.R极易溶于水的原因是(任意写出两点):
A.__________________________.
B.__________________________.
② 用方程式表示R 的溶液显碱性的原因:______________________.
③ 对pH =" 10" 的R 溶液进行下列操作,能使R 的电离平衡逆移的是____________.
A.加入少量 NaCl溶液 B.加入少量1mol.L-1的NH4Cl溶液
C.加入少量MgSO4固体 D.加入少量1mol.L-1 的NaOH溶液
【答案】(1).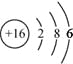 ;
;
(2).Cl->Na+ ,HClO4>H2SO4 ;
(3).![]() ( 或
( 或![]() ,
,![]() )
)
(4).2Na(s)+![]() O2(g)=Na2O2(s) △H=-255.5 kJ/mol-1
O2(g)=Na2O2(s) △H=-255.5 kJ/mol-1
(5).①NH3与H2O能形成分子间氢气键、NH3与H2O能发生反应;
②NH3·H2O![]() NH4++OH-;③BD;
NH4++OH-;③BD;
【解析】试题分析:从图中的化合价、原子半径的大小及原子序数,可知x是H元素,y是C元素,z是N元素,d是O元素,e是Na元素,f是Al元素,g是S元素,h是Cl元素。
(1)S原子的结构示意图为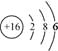 ,故答案为:
,故答案为: ;
;
(2)钠离子核外有2个电子层,氯离子核外有3个电子层,离子半径Cl->Na+,元素的非金属性越强,最高价氧化物对应的水化物的酸性越强,非金属性Cl>S,最高价氧化物对应的水化物的酸性HClO4>H2SO4 ,故答案为:Cl->Na+ ,HClO4>H2SO4;
(3)上述元素组成一种四原子共价化合物可能是氨气,双氧水或乙炔等,电子式为![]() ( 或
( 或![]() ,
,![]() ),故答案为:
),故答案为:![]() ( 或
( 或![]() ,
,![]() );
);
(4)lmol钠在足量氧气中燃烧,恢复至室温,放出255.5kJ热量,钠燃烧热的热化学方程式为2Na(s)+![]() O2(g)=Na2O2(s) △H=-255.5 kJ/mol-1,故答案为:2Na(s)+
O2(g)=Na2O2(s) △H=-255.5 kJ/mol-1,故答案为:2Na(s)+![]() O2(g)=Na2O2(s) △H=-255.5 kJ/mol-1;
O2(g)=Na2O2(s) △H=-255.5 kJ/mol-1;
(5)上述元素可组成常见的碱性气体R为氨气。①NH3与H2O能形成分子间氢气键、NH3与H2O能发生反应,使得氨气极易溶于水,故答案为:NH3与H2O能形成分子间氢气键、NH3与H2O能发生反应;
② 氨与水反应生成的一水合氨能够电离出氢氧根离子,溶液显碱性,离子电离方程式为NH3·H2O![]() NH4++OH-,故答案为:NH3·H2O
NH4++OH-,故答案为:NH3·H2O![]() NH4++OH-;
NH4++OH-;
③ 氨水中存在NH3·H2O![]() NH4++OH-。A.加入少量 NaCl溶液,相当于对溶液碱性稀释,促进氨水的电离,错误;B.加入少量1mol.L-1的NH4Cl溶液,增大了铵根离子的浓度,平衡逆向移动,正确;C.加入少量MgSO4固体生成氢氧化镁沉淀,使得氢氧根离子浓度减小,平衡正向移动,错误;D.加入少量1mol/L的NaOH溶液,增大了氢氧根离子浓度,平衡逆向移动,正确;故选BD。
NH4++OH-。A.加入少量 NaCl溶液,相当于对溶液碱性稀释,促进氨水的电离,错误;B.加入少量1mol.L-1的NH4Cl溶液,增大了铵根离子的浓度,平衡逆向移动,正确;C.加入少量MgSO4固体生成氢氧化镁沉淀,使得氢氧根离子浓度减小,平衡正向移动,错误;D.加入少量1mol/L的NaOH溶液,增大了氢氧根离子浓度,平衡逆向移动,正确;故选BD。


 手拉手全优练考卷系列答案
手拉手全优练考卷系列答案科目:高中化学 来源: 题型:
【题目】在接触法制硫酸的生产中,SO2转化成SO3转化率的大小直接决定生产效率。某研究小组用下图装置模拟生产过程中测定SO2转化成SO3的转化率。已知SO3的熔点是16.8℃,沸点是44.8℃。发生装置中所涉及反应的化学方程式为:Na2SO3(s)+H2SO4(75%)=Na2SO4+SO2↑+H2O

(1)Ⅱ中的试剂是 ,仪器Ⅵ的名称为 。
(2)根据实验需要,应该在Ⅳ、Ⅴ处连接合适的装置。请从下图A~D装置中选择最适合装置并将其序号填入下面的空格中,Ⅳ、Ⅴ处连接的装置分别是 、 。
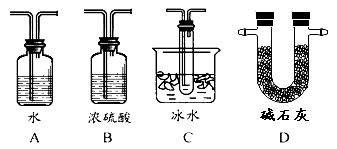
(3)为了提高SO2的转化率,实验时在:①滴加浓硫酸;②加热催化剂的步骤中,应采取的操作是先_______后_________(填编号)。
(4)实验结束后,如果把收集SO3的试管敞口露置于空气中,能够看到管口有大量的白雾,产生此现象的原因是 。
(5)用12.6gNa2SO3粉末与足量较浓的硫酸进行此实验,当反应结束时,继续通入O2一段时间后测得装置Ⅴ增重了4.48g,则实验测得SO2的转化率为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值,下列说法不正确的是( )
A.4.6g金属钠与足量O2充分反应后,所得固体中阴、阳离子的总数为0.3NA
B.1L 0.5 mol/L的FeCl3溶液充分水解后,所得Fe(OH)3胶粒的数目为0.5NA
C.2.0g H218O与D2O的混合物中所含中子数为NA
D.1L含NA个Al3+的Al(NO3)3液中,NO3﹣物质的量浓度大于3 mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有关实验操作正确的是( )
A. 加热蒸发皿时垫上石棉网
B. 将氢氧化钠固体放入烧杯中称量
C. 在量筒中溶解氯化钠固体
D. 将pH试纸浸入待测液中测定pH
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(原创)下列事实能用勒夏特列原理解释的是
A.使用催化剂,在单位时间内提高合成氨产率
B.对于2HI(g) ![]() H2(g)+2CO(g),达平衡后.缩小容器体积可使体系颜色变深
H2(g)+2CO(g),达平衡后.缩小容器体积可使体系颜色变深
C.对于2CaO2(s) ![]() 2CaO(s)+O2(g),达平衡后增大压强,再次平衡后O2的浓度保持不变
2CaO(s)+O2(g),达平衡后增大压强,再次平衡后O2的浓度保持不变
D.溴水中有下列平衡:Br(aq)+ H2O(l) ![]() HBr(aq)+HBrO(aq)当加入硝酸银溶液后,溶液颜色变浅
HBr(aq)+HBrO(aq)当加入硝酸银溶液后,溶液颜色变浅
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】汽车剧烈碰撞时,安全气囊中发生反应10NaN3+2KNO3→K2O+5Na2O+16N2↑。若氧化产物比还原产物多1.75 mol,则下列判断正确的是( )
A.生成42.0 L N2(标准状况)
B.有0.250 mol KNO3被氧化
C.转移电子的物质的量为2.25 mol
D.被氧化的N原子的物质的量为3.75 mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】己知下列反应的热化学方程式:
6C(s)+5H2(g)+3N2(g)+9O2(g)=2C3H5 △H1
2H2(g)+O2(g)=2H2O(g)△H2
C(s)+O2(g)=CO2(g)△H3
则反应4C3H5(ONO2)3(l)=12CO2(g)+10H2O(g)+O2(g)+6N2(g)的△H为______(用△H1、△H2、△H3表示)
A.12△H3+5△H2-2△H1 B.2△H1 -5△H2- 12△H3
C.12△H3-5△H2-2△H1 D.△H1 -5△H2 -12△H3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对下列各组中的实验步骤和现象,分析正确的一项是
选项 | 实验现象 | 原因分析 |
A | 证明酸性条件下H2 O2氧化性比I2强10.关于下列各装置的叙述正确的是( )A.装置①可用于实验室制备NO气体B.装置②可肜于模拟海水蒸馏 C.装置③可用于探究碳酸氢钠的热稳定性 D.装置④为配制溶液过程中的定容操作 11.下列说法正确的是( ) A.将铁粉加入FeCl3、Cucl2混合溶液中,充分反应后剩余的固体中必有铁 B.CO2和SO2混合气体分别通入BaCl2溶液、Ba(NO3)2溶液中,最终都有沉淀生成 C.钠、镁着火时,不可用泡沫灭火器灭火 D.用加热分解的方法可将NH4Cl固体和Ca(OH)2固体的混合物分离 12.对下列各组中的实验 | 碘化钠溶液 |
B | 新制氯水中滴加石蕊试液,溶液先变红,后褪色 | 氯气与水反应生成HCl、HClO,HCl、HClO显酸性,使石蕊变红,Cl2具有强氧化性,使褪色 |
C | SO2通入溴水中,溴水褪色 | SO2具有漂白性,使其褪色 |
D | 向湿润蔗糖中加入浓硫酸,固体迅速变黑,后体积急剧膨胀 | 在浓硫酸脱水作用下,蔗糖被炭化,炭与浓硫酸反应生成CO2、SO2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是(NA表示阿伏加德罗常数的值):( )
①28g氮气所含有的原子数目为NA
②4g金属钙变成钙离子时失去的电子数目为0.1NA
③在常温常压下,11.2LN2含有的分子数为0.5NA
④在标准状况下,1mol氦气含有的原子数为NA
⑤常温常压下,32g氧气和32g臭氧都含有2NA个氧原子
⑥标准状况下,1L水所含分子数为1/22.4NA
⑦17g氨气所含电子数目为10NA
A.①②⑤⑥⑦ B.①②④⑤⑥ C.⑤⑦ D.④⑤⑦
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com