
【题目】以黄铁矿为原料制硫酸产生的硫酸渣中含Fe2O3、SiO2、Al2O3、MgO等。实验室模拟工业以硫酸渣制备铁红(Fe2O3),过程如下:
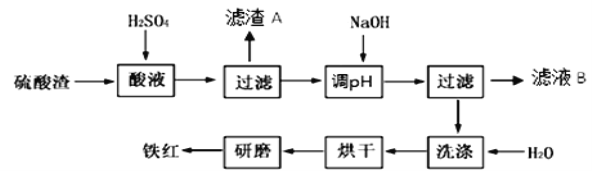
(1)硫酸渣的成分中既能与酸又能与碱反应的是 ,写出酸溶过程Fe2O3与稀硫酸反应的离子反应方程式: 。
(2)生产过程中,为了确保铁红的纯度,氧化过程需要调节溶液的pH的范围是
(部分阳离子以氢氧化物形式沉淀时溶液的pH见下表)
沉淀物 | Fe(OH)3 | Al(OH)3 | Fe(OH)2 | Mg(OH)2 |
开始沉淀 | 2.7 | 3.8 | 7.5 | 9.4 |
完全沉淀 | 3.2 | 5.2 | 9.7 | 12.4 |
(3)滤渣A的主要成分为 ,滤液B含有的主要物质有 。
(4)如何证明洗涤环节充分洗净 。
(5)已知硫酸渣质量为a kg,假设铁红制备过程中铁元素损耗25%,最终得到铁红的质量为b kg,则原来硫酸渣中铁元素质量分数为 。(用题中所给数据计算并用最简整数比表示结果)
【答案】(1) Al2O3 Fe2O3 + 6H+ ==2Fe3+ + 3H2O
(2)3.2—3.8 (3) SiO2 Na2SO4、MgSO4、Al2(SO4)3
(4)取少许最后一次洗涤滤液,滴入1~2滴Ba(NO3)2溶液,若不出现白色浑浊,表示已洗涤完全(合理即可)
(5)铁红制备过程中铁元素的质量为(b×112/160)÷75%=14b/15,则原来硫酸渣中铁元素质量分数为14b/15a。
【解析】
试题分析:(1)Al2O3为两性氧化物,硫酸渣的成分中属于两性氧化物的是Al2O3;Fe2O3与稀硫酸反应生成Fe2(SO4)3和H2O,离子方程式为:Fe2O3 + 6H+ ==2Fe3+ + 3H2O。
(2)根据题目所给表中数据可以看出,Fe3+完全沉淀而其它离子还未沉淀的pH范围是:3.2—3.8。
(3)硫酸渣中SiO2不与H2SO4反应,所以滤渣A的主要成分为SiO2;加入NaOH调节pH后,Fe3+转化为Fe(OH)3沉淀,其它离子仍为硫酸盐,所以滤液B可以回收的物质有: Na2SO4 Al2(SO4)3 MgSO4
(4)用蒸馏水洗涤沉淀的方法为:沿玻璃棒向漏斗(过滤器)的沉淀加蒸馏水至淹没沉淀,静置使液体自然流出,重复操作数次(3次)至沉淀洗涤干净。
(5)m kg铁红含铁元素:b×112/160, 原来硫酸渣中铁元素质量分数为: b×112/160÷(1-25%)÷a=14b/15a。


科目:高中化学 来源: 题型:
【题目】下列说法中,不正确的是
A. 乙烯可以作水果的催熟剂
B. 石油分馏属于化学变化
C. 苯燃烧时火焰明亮,伴有浓烟
D. 冶炼金属是将金属从其化合物中还原出来
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ.CO可用于合成甲醇。在压强为0.1MPa条件下,在体积为bL的密闭容器中充入a mol CO和2a mol H2,在催化剂作用下合成甲醇:
CO(g)+2H2(g)![]() CH3OH(g)平衡时CO的转化率与温度、压强的关系如下图:
CH3OH(g)平衡时CO的转化率与温度、压强的关系如下图:
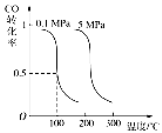
(1)该反应属于 反应(填“吸热”或“放热”)。
(2)100℃时,该反应的平衡常数:K= (用a、b 的代数式表示)。
(3)在温度和容积不变的情况下,再向平衡体系中充入a mol CO,2a mol H2,达到平衡时CO转化率
(填“增大”“不变”或“减小”)
Ⅱ.T ℃时,纯水中c(OH-)为10-6 mol·L-1,则该温度时
(1)将pH=3 的H2SO4溶液与pH=10的NaOH溶液按体积比9:2 混合,所得混合溶液的pH为 。
(2)若1体积pH1=a的某强酸溶液与10体积pH2=b的某强碱溶液混合后溶液呈中性,则混合前,该强酸的pH1与强碱的pH2之间应满足的关系是 。
Ⅲ. 在25mL的氢氧化钠溶液中逐滴加入0. 2 mol/ L醋酸溶液,滴定曲线如图所示。
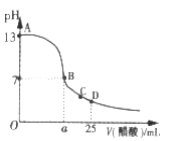
(1)该氢氧化钠溶液浓度为________________。
(2)在B点,a_________12.5 mL(填“<”“>”或“=”)。
(3)在D点,溶液中离子浓度大小关系为_____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学设计如下实验装置用于制取纯净的无水FeCl3.
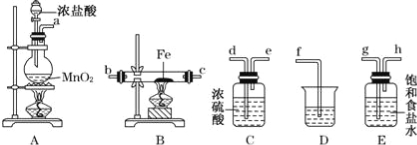
(1)图中盛放浓盐酸的实验仪器的名称为 ,A中发生反应的化学方程式为
(2)各装置的正确连接顺序为:a → → → → → → c → (填字母代号),
(3)装置E的作用是 ,装置C的作用是 。
(4)装置D中所发生反应的离子方程式为 .
(5)装置A中,如果反应产生氯气的体积为2.24L(标准状况),则反应中被氧化的HCl的质量为 ___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某酸溶液的pH=3,则该酸溶液的物质的量浓度为( )
A.一定大于0.001 mol·L-1 B.一定等于0.001 mol·L-1
C.一定小于0.001 mol·L-1 D.以上说法均欠妥
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A.要除去CO2中混有少量的SO2,可用饱和的碳酸氢钠溶液
B.SO2与Cl2混合后溶于水漂白性增强
C.因常温下铁与浓硝酸不反应,故可在常温下用铁制贮罐贮运浓硝酸
D.碱石灰和无水CaCl2都可以用于干燥NH3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于如图所示转化关系(X代表卤素),说法正确的是

A.H2(g)+ X2(g)===2H(g)+ 2X(g) △H2>0
B.生成HX的反应热与途径有关,所以△H1≠△H2 + △H3
C.若X分别表示Cl,Br,I,则过程Ⅱ吸收的热量依次增多
D.△H1代表H2的燃烧热
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com