
【题目】如图所示,某化学兴趣小组设计了一个燃料电池,并探究氯碱工业原理和粗铜精炼原理,其中乙装置中X为阳离子交换膜。根据要求回答相关问题:

(1)通入氧气的电极为_____(填“正极”或“负极”),通氢气一极的电极反应式为_________________;
(2)铁电极为_______(填“阳极”或“阴极”),乙装置中电解反应的化学方程式为_________________。
(3)若在标准状况下,有1.12 L氧气参加反应,丙装置中阴极增重的质量为______g;
(4)某粗铜中含有铁、金、银和铂等杂质,通过电解精制后,为从电解液中制得硫酸铜晶体(CuSO4·5H2O),设计了如下工艺流程:

已知:几种金属阳离子开始沉淀和沉淀完全的pH:
氢氧化物开始沉淀时的pH | 氢氧化物沉淀完全时的pH | |
Fe3+ | 1.9 | 3.2 |
Fe2+ | 7.0 | 9.0 |
Cu2+ | 4.7 | 6.7 |
①步骤I中加入试剂A的目的是_____________________________,试剂A应选择______(填序号);
a.氯气 b.过氧化氢 C.酸性高锰酸钾溶液
选择该试剂的原因_____________________________________________________;
②步骤II中试剂B为_________,调节pH的范围是___________;
③步骤III的操作是加热浓缩、_______、___________。
【答案】正极 H2-2e-+2OH-=2H2O 阴极 2NaCl+2H2O![]() 2NaOH+ C12↑+H2↑ 6.4 将Fe2+氧化为Fe3+ b 过氧化氢是绿色氧化剂,在氧化过程中不引入杂质,不产生污染 CuO或Cu(OH)2或Cu2(OH)2CO3 3.2≤pH<4.7 冷却结晶 过滤
2NaOH+ C12↑+H2↑ 6.4 将Fe2+氧化为Fe3+ b 过氧化氢是绿色氧化剂,在氧化过程中不引入杂质,不产生污染 CuO或Cu(OH)2或Cu2(OH)2CO3 3.2≤pH<4.7 冷却结晶 过滤
【解析】
(1)氢氧燃料电池,氧气做正极,发生还原反应,氢气做负极,在碱性环境下发生氧化反应,极反应式为H2-2e-+2OH-=2H2O,正确答案:正极;H2-2e-+2OH-=2H2O。
(2) 氧燃料电池,氧气做正极,氢气做负极;铁与电源的负极相连,为电解池的阴极,阳极为石墨,电解饱和氯化钠溶液,阴极生成氢气和氢氧化钠,阳极产生氯气;正确答案:
阴极 ; 2NaCl+2H2O![]() 2NaOH+ C12↑+H2↑ ;
2NaOH+ C12↑+H2↑ ;
(3)丙装置为电解精炼铜,粗铜做阳极,溶液中铜离子得电子变为铜,根据电子转移总数相等:O2+4e-+2H2O=4OH-,Cu2++2e-=Cu,1.12 L氧气参加反应,转移电子0.2mol,生成铜0.1 mol,铜的质量6.4 g,正确答案6.4 g。
(4)①电解液中含有Fe2+、Cu2+、SO42-等离子,Fe2+的沉淀的pH 在7-9之间,Cu2+的沉淀的pH 在4.7-6.7之间,直接调整溶液的pH,在保证Fe2+沉淀的同时,Cu2+也变为沉淀,无法进行后续操作,因此需要把将Fe2+氧化为Fe3+,加入氧化剂为过氧化氢,因为过氧化氢是绿色氧化剂,在氧化过程中不引入杂质,不产生污染,正确答案:将Fe2+氧化为Fe3+; b ;过氧化氢是绿色氧化剂,在氧化过程中不引入杂质,不产生污染。
②加入试剂来调整溶液的pH,使溶液的酸性减弱,保证Fe3+沉淀完全,而Cu2+不产生沉淀,这样的试剂要满足不溶于水,能够与酸反应且反应后不引入新的杂质离子等,因此需要加入含有铜元素的化合物:CuO或Cu(OH)2或Cu2(OH)2CO3 等; 根据表中给定的数据得出调节溶液pH的范围3.2≤pH<4.7;正确答案:CuO或Cu(OH)2或Cu2(OH)2CO3; 3.2≤pH<4.7 。
③从硫酸铜溶液中得到硫酸铜固体,需要进行的操作为:配制成高温时的硫酸铜饱和溶液,降低温度,有固体析出,再进行过滤,洗涤、干燥、称重等操作;正确答案:冷却结晶 ;过滤。


科目:高中化学 来源: 题型:
【题目】如图所示是Zn和Cu形成的原电池,某实验兴趣小组做完实验后,在读书卡上的记录如下,则卡片上的描述合理的是( )

实验后的记录:
①Cu为负极,Zn为正极 ②Cu极上有气泡产生,发生还原反应 ③SO42-向Cu极移动 ④若有0.5 mol电子流经导线,则可产生0.25mol气体 ⑤电子的流向是Cu→Zn ⑥正极反应式:Cu-2e-=Cu2+,发生氧化反应
A.①②③B.②④C.②③④D.④⑤⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列比较中,正确的是( )
A. 同温度同物质的量浓度时,HF比HCN易电离,则NaF溶液的pH比NaCN溶液大
B. 0.2 mol·L-1NH4Cl和0.1 mol·L-1NaOH溶液等体积混合后:c(![]() )>c(Cl-)>c(Na+)>c(OH-)>c(H+)
)>c(Cl-)>c(Na+)>c(OH-)>c(H+)
C. 物质的量浓度相等的H2S和NaHS混合溶液中:c(Na+)+c(H+)=c(S2-)+c(HS-)+c(OH-)
D. 同浓度的下列溶液中,①(NH4)2SO4、②NH4Cl、③CH3COONH4、④NH3·H2O;c(![]() )由大到小的顺序是:①>②>③>④
)由大到小的顺序是:①>②>③>④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乙烯水合法合成乙醇分两步完成,反应过程中的能量变化如图所示,对于在密闭容器中进行的合成反应,下列说法不正确的是

A.反应①和反应②均为放热反应
B.反应①为加成反应,反应②为取代反应
C.硫酸是该反应的催化剂
D.总的能量变化为(E1+E2-E3-E4)kJmol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NA为阿伏加德罗常数的值。下列说法正确的是( )
A. 等质量的 D2O和H2O中含有的质子数相同
B. 过氧化钠与水反应时,生成0.1 mol氧气转移的电子数为0.2NA
C. 2 L 0.5 mol·L-1亚硫酸溶液中含有的H+离子数为2NA
D. 密闭容器中2 mol NO与1 mol O2充分反应,产物的分子数为2NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是实验室常用的气体制备、净化和收集装置。若依据反应H2C2O4 CO↑+CO2↑+H2O制取CO,则合理的装置组合为( )
CO↑+CO2↑+H2O制取CO,则合理的装置组合为( )

A. ①⑤⑧B. ③⑤⑦C. ②⑤⑥D. ③④⑧
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学学习小组用酸性KMnO4溶液与H2C2O4(K1 = 5.4 × 10-2)的反应(此反应为放热反应)进行如下实验:
Ⅰ、探究“条件对化学反应速率的影响”,并设计了如下的方案记录实验结果(忽略溶液混合体积变化)。限选试剂和仪器:0.20 molL-1 H2C2O4溶液、0.010 molL-1 KMnO4 溶液(酸性)、蒸馏水、试管、量筒、秒表、恒温水浴槽
物理量 | V(H2C2O4溶液)/mL | V(蒸馏水)/mL | V(KMnO4溶液)/mL | T/℃ | 乙 |
① | 2.0 | 0 | 4.0 | 50 | |
② | 2.0 | 0 | 4.0 | 25 | |
③ | 2.0 | a | 4.0 | 25 |
(1)完成该反应的实验原理: + MnO4- + = CO2↑ + Mn2+ + H2O_______________
(2)上述实验①、②是探究___________对化学反应速率的影响;若上述实验②、③是探究浓度对化学反应速率的影响,则 a 为___________;乙是实验需要测量的物理量,则表格中“乙”应填写_______________。
Ⅱ、测定H2C2O4xH2O中x值。已知:M(H2C2O4) = 90 gmol-1。①称取1.260 g 纯草酸晶体,将草酸制成 100.00 mL 水溶液为待测液; ②取 25.00 mL 待测液放入锥形瓶中,再加入适量的稀 H2SO4; ③用浓度为 0.05 000 molL-1的KMnO4标准溶液进行滴定。
(1)某学生的滴定方式(夹持部分略去)如下,最合理的是________(选填 a、b)。由图可知消耗 KMnO4 溶液体积为________ mL。

(2)滴定终点锥形瓶内现象为__________________________________________________。
(3)通过上述数据,求得 x =______________。
(4)下列操作会造成所测x偏大的是____________(填字母)。
A.滴定终点俯视读数
B.锥形瓶用待测溶液润洗
C.滴定前有气泡,滴定后没有气泡
D.配制100 mL待测溶液时,有少量溅出
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】符合分子式“C6H6”的多种可能结构如图所示,下列说法正确的是
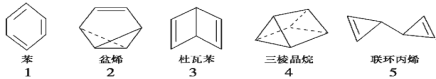
A.1~5 对应的结构中所有原子均可能处于同一平面的有 1 个
B.1~5 对应的结构中一氯取代物只有 1 种的有 3 个
C.1~5 对应的结构中能使溴的四氯化碳溶液褪色的有 4 个
D.1~5 对应的结构均能与氢气在一定条件下发生加成反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】![]() 时,向
时,向![]() 溶液中滴加等浓度的
溶液中滴加等浓度的![]() 溶液,溶液的
溶液,溶液的![]() 与
与![]() 溶液的体积关系如图所示。下列叙述正确的是( )
溶液的体积关系如图所示。下列叙述正确的是( )

A. ![]() 溶液中水的电离程度比
溶液中水的电离程度比![]() 溶液中大
溶液中大
B. ![]() 点溶液中含有
点溶液中含有![]() 和
和![]()
C. ![]() 点,
点,![]()
D. ![]() 点,
点,![]()
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com